Clear Sky Science · de
Glycin‑Synthese durch C−N‑Kopplung von Abfallplastik und Nitrat über einen diatomaren Pd−B‑Katalysator
Müll in die Bausteine des Lebens verwandeln
Plastikflaschen, Lebensmittelbehälter und Polyesterkleidung sind überall – ebenso wie die Abfälle, die sie hinterlassen. Gleichzeitig stoßen viele Fabriken nitratbelastete Abwässer aus, die Flüsse und Meere verschmutzen können. Diese Studie zeigt, wie sich beide Probleme zugleich angehen lassen: mithilfe von Sonnenlicht und einem speziell entwickelten Katalysator werden weggeworfener Kunststoff und Nitrat in Glycin umgewandelt, eine einfache Aminosäure, die in Nahrungsmitteln, Medizin und Landwirtschaft weit verbreitet ist.
Warum Glycin und Abfall wichtig sind
Glycin ist einer der Grundbausteine von Proteinen und wird in Größenordnungen von Hunderttausenden Tonnen pro Jahr hergestellt. Konventionelle industrielle Verfahren, insbesondere der klassische Streckerprozess, setzen toxische Cyanverbindungen und harte Reaktionsbedingungen ein, was Sicherheits- und Umweltfragen aufwirft. Gleichzeitig übersteigt die weltweite Produktion des PET‑Kunststoffs – verwendet in Flaschen, Textilien und Verpackungen – 100 Millionen Tonnen jährlich, wobei mehr als 80 % auf Deponien oder in der Umwelt landen. Wird PET chemisch aufgespalten, entsteht unter anderem Ethylenglykol, eine geringwertige Flüssigkeit, deren Reinigung kostspielig ist. Die Autoren stellen eine einfache Frage: Anstatt Ethylenglykol und Nitrat als Abfall zu betrachten, könnten sie mit nur Sonnenlicht zu Rohstoffen für die Herstellung von wertvollem Glycin werden?
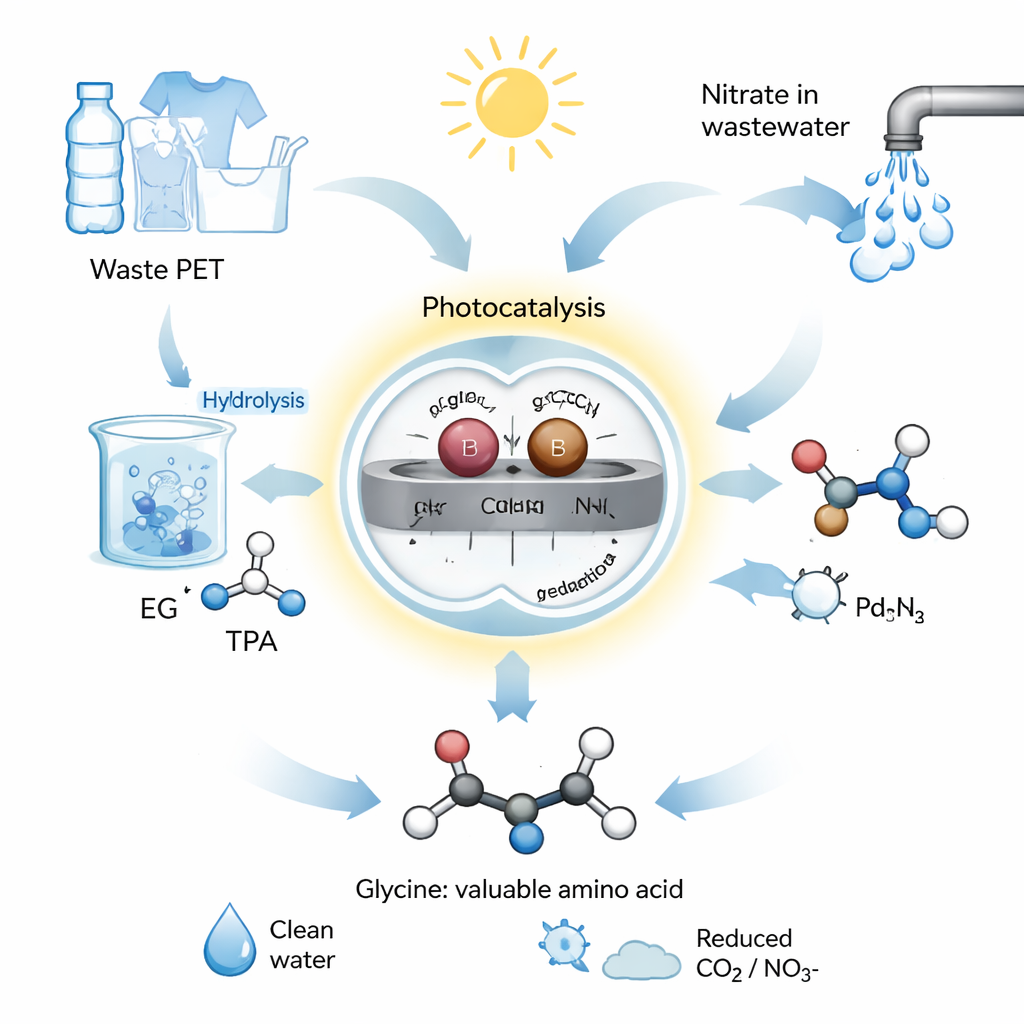
Ein sonnengetriebener chemischer Kurzweg
Das Team entwickelte ein photokatalytisches System, das heißt: Es nutzt Licht, um chemische Reaktionen anzutreiben. Sie bauten einen Katalysator aus graphitischem Kohlenstoffnitrid, einem Halbleiter, und verankerten Paare einzelner Palladium‑ (Pd) und Bor‑ (B) Atome auf seiner Oberfläche. Diese gepaarten Atome wirken wie ein mikroskopisches Zweierteam, das jeweils eine andere Hälfte der Chemie übernimmt. Im Verfahren wird PET‑Abfall zunächst in alkalischem Wasser hydrolysiert – in seine Bestandteile aufgespalten –, wodurch Ethylenglykol freigesetzt wird. Dieses Ethylenglykol und Nitrat aus Abwasser werden dann in Wasser mit dem Pd–B‑Katalysator gegeben und simuliertem oder natürlichem Sonnenlicht ausgesetzt. Unter diesen milden Bedingungen wandelt das System das Gemisch mit hoher Ausbeute und einer Selektivität von über 92 % in Glycin um, das heißt, es entstehen nur sehr wenige unerwünschte Nebenprodukte.
Wie das atomare Duo wirkt
Der Erfolg des Katalysators beruht darauf, wie er kurzlebige Reaktionszwischenprodukte handhabt. Bor‑Stellen auf der Oberfläche sind „lochreich“, das heißt, sie nehmen bei Lichtabsorption bereitwillig positive Ladung auf. An diesen B‑Stellen wird Ethylenglykol schonend oxidiert – von Wasserstoff befreit – und es entsteht Glykolaldehyd, ein instabiles Molekül, das normalerweise weiter zu Säuren oder sogar Kohlendioxid überoxidiert. Palladiumstellen hingegen sind „elektronenreich“. Sie nutzen die lichtgenerierten Elektronen, um Nitrat schrittweise zu Ammonium oder Ammoniak zu reduzieren. Der entscheidende Schritt ist eine C–N‑Kopplung zwischen Glykolaldehyd und diesen Stickstoffspezies zur Bildung von Ethanolamin, das anschließend weiter oxidiert wird, wiederum hauptsächlich an den B‑Stellen, bis Glycin entsteht. Indem das System Glykolaldehyd gerade so lange stabilisiert, dass es reagieren kann, und Elektronen sowie Löcher räumlich trennt, lenkt das Pd–B‑Paar die Chemie weg von verlustreichen Nebenreaktionen hin zum gewünschten Aminosäureprodukt.
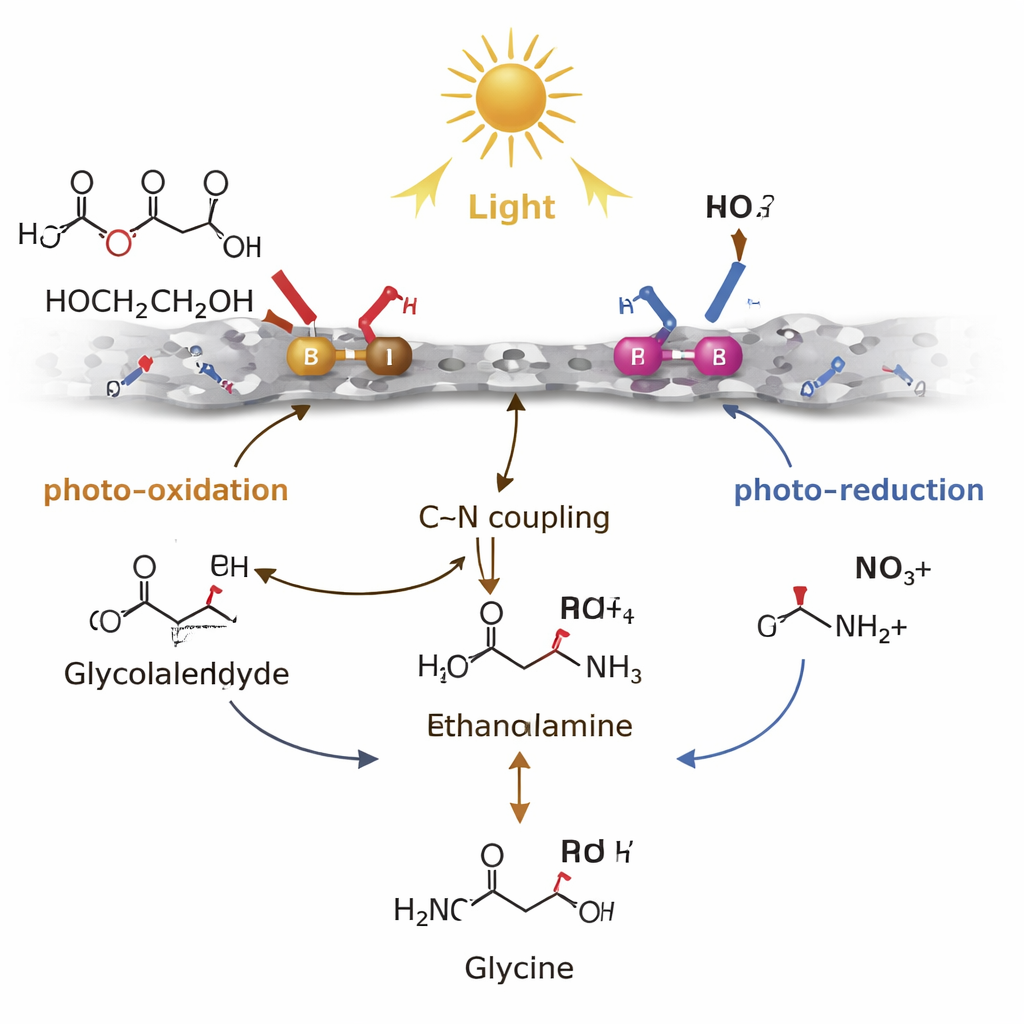
Vom Labormechanismus zum Abfall der realen Welt
Die Forschenden bestätigten jeden Teil dieses Pfads mit einer Reihe von Techniken und verfolgten Radikale, Zwischenprodukte und Stickstoffprodukte in Echtzeit. Sie verglichen verschiedene Katalysatormaterialien und Metalle und fanden heraus, dass g‑C3N4‑Träger mit isolierten Pd–B‑Paaren die beste Leistung zeigten, mit Glycinbildungsraten von 2,9 Millimol pro Gramm Katalysator und Stunde. Der Katalysator blieb über wiederholte Zyklen aktiv und seine Struktur stabil. Wichtig ist, dass das Team über reine Labormaterialien hinausging: Sie demonstrierten die Glycinproduktion im Grammmaßstab aus realen post‑consumer PET‑Abfällen – Pulver, Flaschen, Kleidung, Tüten und mehr – kombiniert mit Nitratlösungen und sogar komplexen Abwässern. Sie zeigten auch, dass verwandte Alkohole aus Biomasse, wie Glycerin, als alternative Kohlenstoffquellen dienen können, was die Relevanz des Ansatzes erweitert.
Eine Win‑Win‑Lösung für Abfall und Klima
Um das Konzept näher an die Anwendung zu bringen, prüften die Autoren ihr Verfahren unter natürlichem Sonnenlicht, das durch eine einfache Fresnel‑Linse fokussiert wurde. Das System produzierte konstant Glycin mit hoher Selektivität, und Modellrechnungen deuten darauf hin, dass ein Hochfahren des Verfahrens erhebliche CO2‑Emissionen vermeiden und Nitrat‑Einträge in die Umwelt verhindern könnte. Einfach ausgedrückt skizziert diese Arbeit einen Weg, Berge von gebrauchtem Kunststoff und verschmutztes Wasser mithilfe von Licht und einem fein abgestimmten Katalysator in eine nützliche Aminosäure zu verwandeln. Zwar bleiben bis zur industriellen Umsetzung ingenieurtechnische Herausforderungen, doch die Studie zeigt, wie ein Katalysatordesign auf atomarer Ebene zwei große Abfallströme in ein wertvolles chemisches Produkt überführen kann.
Zitation: Ya, Z., Li, M., Fu, D. et al. Glycine photosynthesis via C−N coupling of waste plastic and nitrate over diatomic Pd−B catalyst. Nat Commun 17, 1887 (2026). https://doi.org/10.1038/s41467-026-68666-z
Schlüsselwörter: glycin, Plastikrecycling, Photokatalyse, Nitratabwässer, Einzelatomkatalysatoren