Clear Sky Science · de
Niedrige Temperatur und schnelle photothermische Oxidation von flüssigem Gallium zur kreislaufartigen Wasserstoffproduktion
Ein neuer Weg zur Herstellung sauberer Brennstoffe
Wasserstoff wird oft als Brennstoff der Zukunft bezeichnet: Beim Verbrennen entsteht Wasser statt Rauch oder Ruß. Heute wird der meiste Wasserstoff jedoch aus fossilen Brennstoffen oder mit teuren, energieintensiven Anlagen hergestellt. Diese Studie untersucht einen anderen Weg: ein weiches, silbrig schimmerndes Metall namens Gallium in Verbindung mit gewöhnlichem Wasser – sogar Meerwasser – zu nutzen, um Wasserstoff in einem wiederverwendbaren, kreislaufartigen Prozess zu erzeugen, der größtenteils durch Sonnenlicht angetrieben wird.
Wie Licht und Metall zu Brennstoff werden
Die Forschenden entdeckten, dass winzige Tröpfchen flüssigen Galliums mit Wasser reagieren und Wasserstoffgas freisetzen, wenn sie durch Licht erwärmt werden. Gallium schmilzt knapp über Raumtemperatur, sodass es bei milder Erwärmung flüssig wird. Wenn Licht auf die Tröpfchen trifft, absorbieren sie die Energie und erwärmen sich, was ihre Reaktion mit Wasser beschleunigt. Während dieser Reaktion wird das Gallium in eine feste Verbindung namens Galliumoxyhydroxid umgewandelt, während Wasserstoffblasen freigesetzt werden. Da Gallium flüssig ist, blättert die auf seiner Oberfläche entstehende feste Schicht von selbst ab, anstatt das Metall zu versiegeln. So bleibt frisches Metall exponiert und die Reaktion kann schnell weiterlaufen.
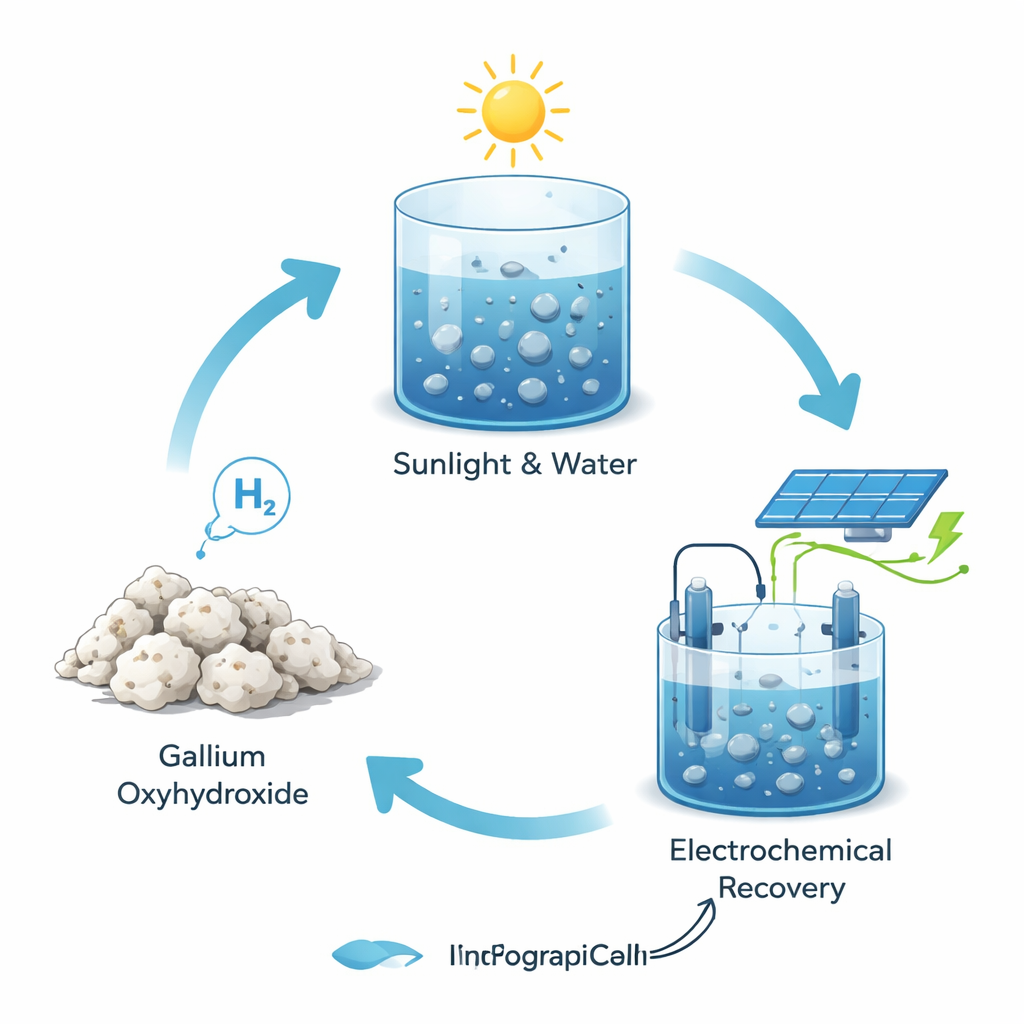
Ein geschlossener Kreislauf statt Einweggebrauch
Die meisten chemischen Reaktionen, die Wasserstoff erzeugen, verbrauchen ihre Metallbestandteile dauerhaft und hinterlassen hartnäckige Abfälle. Im Gegensatz dazu zeigt diese Arbeit, dass das nach der Wasserstoffproduktion verbleibende feste Galliumoxyhydroxid kein Endpunkt ist. Es lässt sich in einer milden Säure auflösen und mit standardmäßiger elektrochemischer Ausrüstung – vereinfacht gesagt einer batterieähnlichen Vorrichtung, die rückwärts betrieben wird – wieder in flüssiges Gallium zurückverwandeln. Angetrieben von Strom, idealerweise aus erneuerbaren Quellen wie Solar- oder Windenergie, regeneriert dieser Rückgewinnungsschritt fast das gesamte ursprüngliche Gallium. Das bedeutet, dass dieselbe Metallcharge immer wieder genutzt werden kann und ein geschlossener Kreislauf für die Wasserstoffproduktion entsteht, statt eines Einwegverfahrens.
Schneller, niedrigtemperaturiger Wasserstoff aus verschiedenen Wasserarten
In praktischen Tests erzeugte das Team Galliumtröpfchen, indem es Schallwellen einsetzte, um geschmolzenes Metall in viele kleine Partikel zu zerteilen. Kleinere Tröpfchen bieten eine größere Oberfläche und nehmen Licht effizienter auf, wodurch die Wasserstoffproduktion schneller und vollständiger verlief. Unter starken, aber realistischen Lichtverhältnissen, die konzentriertem Sonnenlicht entsprechen, konnten 0,2 Gramm Galliumtröpfchen in Wasser in etwa anderthalb Stunden vollständig in das feste Produkt umgewandelt werden, wobei Wasserstoffmengen erzeugt wurden, die dem theoretischen Maximum entsprachen. Wichtig ist, dass diese Leistung nicht nur in gereinigtem Wasser, sondern auch in salzhaltigen Lösungen und in realem Küstenmeerwasser gehalten wurde, ohne dass ein separater Entsalzungsschritt nötig war.
Warum Licht mehr bewirkt als bloßes Erwärmen
Die Wissenschaftler verglichen mehrere Antriebsarten für die Reaktion und stellten fest, dass das direkte Bestrahlen der Tröpfchen mit Licht deutlich wirkungsvoller war als bloßes Erhitzen des Wassers auf dieselbe Temperatur. Licht erfüllt dabei zwei Aufgaben gleichzeitig: Es erwärmt das Gallium und es wechselwirkt mit der dünnen Schicht des festen Materials, die sich auf den Tröpfchen bildet, wodurch elektrische Ladungen über die Grenzfläche transportiert werden. Diese Ladungen erleichtern es dem Metall, weiter mit Wasser zu reagieren. Experimente mit verschiedenen Lampen, einem Solarsimulator und gebündeltem natürlichem Sonnenlicht zeigten alle, dass sichtbares Licht besonders gut geeignet ist, dieses „photothermische“ Verhalten auszulösen, also die Kombination von Licht und Wärme zur Beschleunigung der Wasserstoffproduktion.
Vom Laboransatz zum zukünftigen Energieträger
Aus energetischer Sicht schätzen die Forschenden, dass der vollständige Zyklus – vom Reagieren des Galliums mit Wasser zur Wasserstoffproduktion bis zur Regeneration des Metalls – eine Rundreiseeffizienz von etwa 13 Prozent erreichen könnte, wenn Sonnenlicht als kostenloser Input betrachtet wird. Obwohl Gallium selbst nicht billig ist, ist es wiederverwendbar, relativ ungiftig und als kompakter Energieträger leicht zu transportieren und zu lagern. Die Studie skizziert ein Zukunftsszenario, in dem Gallium an Küstenstandorte verschifft, dort unter Sonnenlicht mit Meerwasser zur bedarfsgerechten Wasserstoffproduktion umgesetzt und anschließend zur Regeneration mit sauberem Strom zurückgebracht wird. Kurz gesagt demonstriert die Arbeit einen vielversprechenden Weg, Sonnenschein und Meerwasser mithilfe eines recyclebaren flüssigen Metalls in einen speicherbaren, sauberen Brennstoff zu verwandeln und rückt die Vision eines wasserstoffbasierten Energiesystems näher.
Zitation: Campos, L.G.B., Allioux, FM., Fimbres Weihs, G. et al. Low temperature and rapid photothermal oxidation of liquid gallium for circular hydrogen production. Nat Commun 17, 1890 (2026). https://doi.org/10.1038/s41467-026-68664-1
Schlüsselwörter: Wasserstoffproduktion, flüssiges Gallium, Sonnenenergie, Meerwasser als Brennstoff, kreisförmige Chemie