Clear Sky Science · de
Regulierung des AP1-Adaptors durch den beidhändigen Chaperon MEA1
Warum dieser verborgene Helfer in der Zelle wichtig ist
In jeder menschlichen Zelle transportieren Tausende kleiner Pakete Proteine dorthin, wo sie gebraucht werden, oder zur zellulären "Recyclingzentrale" für den Abbau. Dieser Verkehr hält unsere Zellen gesund und unsere Immunabwehr im Gleichgewicht. Die hier zusammengefasste Studie enthüllt ein zuvor rätselhaftes Protein namens MEA1, das sich als essenziell für den Aufbau einer der wichtigsten Sortiermaschinen erweist, die diese Pakete belädt. Zu verstehen, wie MEA1 funktioniert, hilft zu erklären, wie Zellen wichtige Frachtstoffe kontrollieren, einschließlich Molekülen, die antivirale Immunantworten ein- und ausschalten.
Verkehrssteuerung im Versandzentrum der Zelle
Ein Großteil des zellulären Versands läuft über den Golgi-Apparat, einen Stapel abgeflachter Säckchen, der wie ein zentrales Postamt wirkt. Vom Golgi aus kann Fracht an die Zelloberfläche geschickt oder an interne Kompartimente zur Vernichtung weitergeleitet werden. Ein Proteinkomplex namens AP1 steht im Zentrum dieser Route. AP1 erkennt Markierungen auf Frachtproteinen, hilft, die Membran zu krümmen, und rekrutiert eine Außenschicht aus Clathrin, um kleine Transportvesikel zu bilden. Ohne korrekt zusammengesetztes AP1 lagern sich entscheidende Frachtstoffe an den falschen Orten ab, und normale Signalwege, einschließlich solcher der Immunität, können gestört werden. 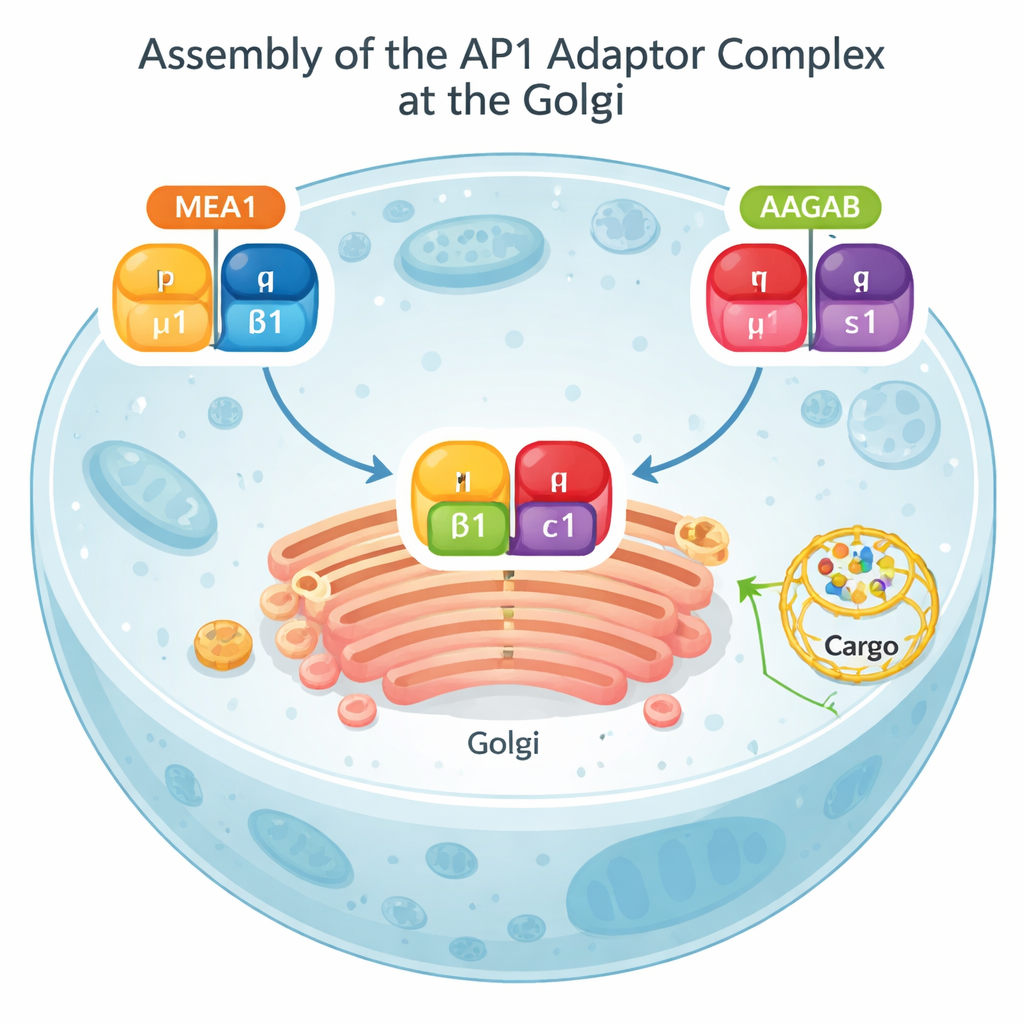
Aufspüren eines fehlenden Montagearbeiters
Die Autorinnen und Autoren suchten nach Proteinen, die physisch mit AP1 assoziieren und beim Zusammenbau helfen könnten. Sie durchkämmten eine große Protein-Interaktionsdatenbank, schlossen Kandidaten aus, die wahrscheinlich nicht mit AP1 zusammenarbeiten, und nutzten dann ein KI-Werkzeug, AlphaFold, um vorherzusagen, wie die verbleibenden Proteine mit einzelnen AP1-Teilen Kontakt aufnehmen könnten. Diese Suche hob MEA1 hervor, ein kleines, zuvor uncharakterisiertes Protein, das in vielen Geweben vorkommt. Nachfolgeexperimente in menschlichen Zellen bestätigten, dass MEA1 an zwei spezifische AP1-Untereinheiten bindet, bekannt als μ1 und β1, sowohl einzeln getestet als auch in ihren natürlichen, unveränderten Formen.
MEA1 erhält AP1 und hält den Frachtverkehr in Gang
Um zu untersuchen, was MEA1 tatsächlich bewirkt, löschten die Forschenden das MEA1-Gen in menschlichen Zelllinien. Fehlt MEA1, waren alle vier AP1-Teile stark reduziert, und charakteristische AP1-Cluster in Golginähe verschwanden nahezu. Dieser Verlust hatte eindeutige funktionelle Folgen. Ein AP1-Frachtstoff, der Folatrezeptor FOLR1, reicherte sich an der Zelloberfläche an, anstatt nach innen geleitet zu werden — ein Kennzeichen defekter AP1-Sortierung. Ein anderer Frachtstoff, das Immun-Signalprotein STING, wurde nicht mehr effizient in Vesikel verpackt, die zu Lysosomen, den Recyclingzentren der Zelle, führen. Infolgedessen blieben aktiviertes STING und seine Partnerkinase TBK1 auf hohem Niveau bestehen, was darauf hinweist, dass der "Aus-Schalter" dieses antiviralen Weges nicht richtig funktionierte. Die Wiedereinführung von MEA1 stellte die AP1-Spiegel wieder her und korrigierte diese Transportdefekte.
Ein beidhändiges Chaperon und ein kollisionsbasierter Aufbauprozess
Biochemische Tests und AlphaFold-Modelle zeigten, dass MEA1 wie ein "beidhändiges" Montagechaperon agiert: sein vorderer Bereich greift die μ1-Untereinheit, während sein hinterer Bereich β1 erfasst. Für sich genommen sind μ1 und β1 instabil und neigen zum Aggregieren oder zum Abbau; an MEA1 gebunden werden sie löslich und montagebereit. Ein weiteres bekanntes Chaperon, AAGAB, erfüllt eine parallele Aufgabe für die verbleibenden zwei AP1-Untereinheiten γ und σ1. Treffen die MEA1–μ1–β1- und AAGAB–γ–σ1-Komplexe aufeinander, verbinden sich ihre Untereinheiten zu einem vollständigen, vierteiligen AP1-Adaptor. In diesem Moment lösen sich beide Chaperone und kehren in das Zellplasma zurück, während das neu gebildete AP1 zu Membranen wandert, um seine Sortierfunktion auszuüben. Dieser "Dual-Chaperon-Kollisions"-Mechanismus zeigt, dass der AP1-Aufbau sorgfältig orchestriert und nicht dem Zufall überlassen ist.
Allgemeinere Lektionen zur zellulären Qualitätskontrolle
Über AP1 hinaus deutet die Studie auf eine allgemeinere Strategie hin, die Zellen möglicherweise zum Aufbau vieler großer Proteinkomplexe verwenden. MEA1 kann auch schwach ein anderes Adaptersystem namens AP2 unterstützen, und zusammen mit AAGAB und einem dritten Chaperon namens CCDC32 veranschaulicht es einen umfassenderen Weg, den die Autorinnen und Autoren als "Chaperon-unterstützte Adapterprotein-Assemblierung" bezeichnen. In diesem Konzept stabilisieren spezialisierte Chaperone fragile Untereinheiten, bringen die richtigen Paare zusammen und blockieren vorübergehend die Frachtbindungsstellen, bis der Komplex vollständig gebildet und sicher einsatzbereit ist. 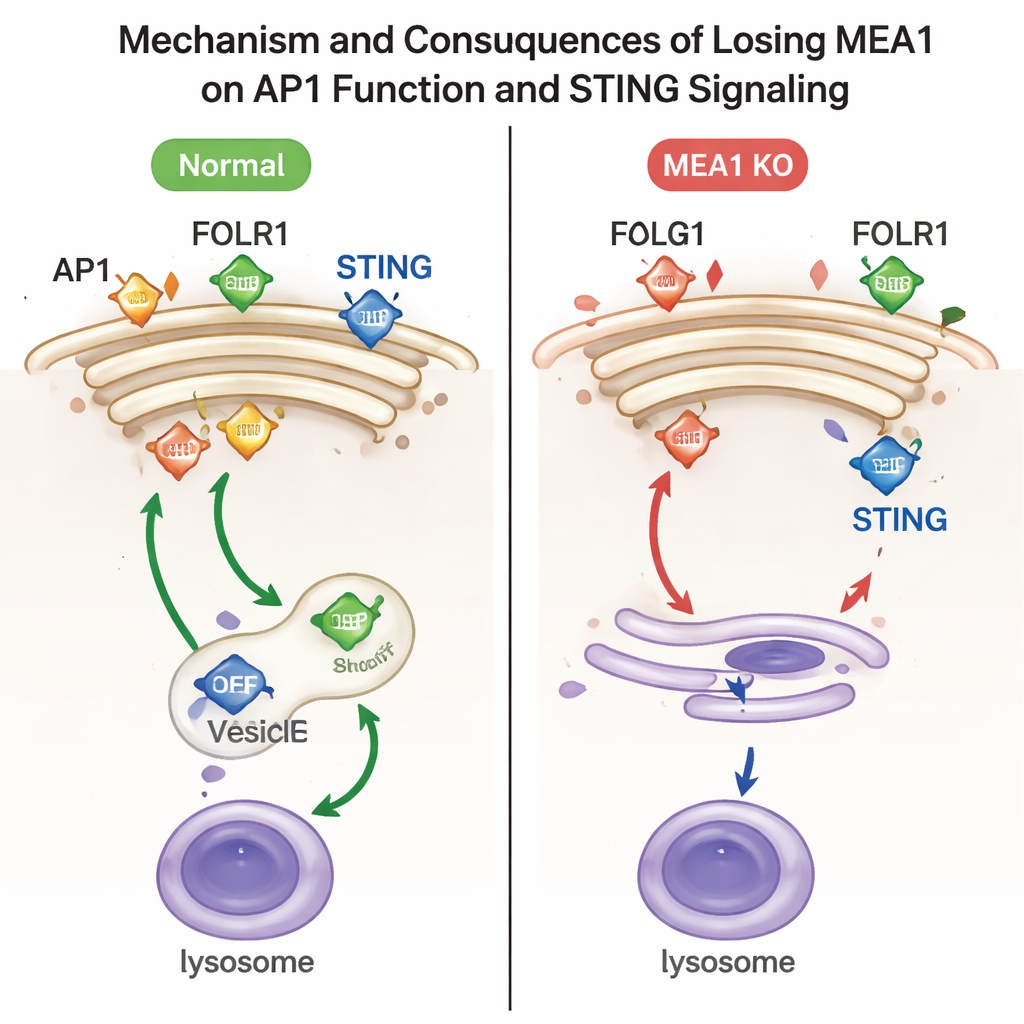
Was das für Gesundheit und Krankheit bedeutet
Für Laien ist die zentrale Erkenntnis, dass MEA1 ein entscheidender Hintergrundarbeiter ist, der beim Zusammenbau von AP1 hilft, einer Kern-Sortiermaschine in unseren Zellen. Fehlt MEA1, zerfällt AP1, Verkehrsstaus entstehen, und wichtige Regulatoren wie STING werden nicht korrekt abgeschaltet. Dieses neue Verständnis könnte langfristig helfen, bestimmte Immunstörungen oder andere Krankheiten zu erklären, die mit fehlerhaftem Proteinverkehr zusammenhängen, und es offenbart ein allgemeines Prinzip dafür, wie Zellen komplexe molekulare Maschinen sicher aus instabilen Bausteinen zusammensetzen.
Zitation: Wan, C., Wu, J., Ouyang, Y. et al. Regulation of AP1 adaptor assembly by the bi-handed chaperone MEA1. Nat Commun 17, 1876 (2026). https://doi.org/10.1038/s41467-026-68662-3
Schlüsselwörter: Proteintransport, Adapterprotein AP1, molekulare Chaperone, STING-Signalübertragung, Zellbiologie