Clear Sky Science · de
SAMSN1 bremst die von NK-Zellen vermittelte Anti-Tumor-Immunität beim hepatozellulären Karzinom
Warum unsere eigenen Killerzellen manchmal versagen
Leberkrebs gehört zu den tödlichsten Krebsarten weltweit, teilweise weil das Immunsystem des Körpers ihn oft nicht in Schach halten kann. Diese Studie stellt eine einfache, aber entscheidende Frage: Warum verlieren unsere natürlichen Killerzellen (NK-Zellen) — Immunzellen, die Krebs ohne vorherige Schulung zerstören können — in Lebertumoren ihre Schlagkraft, und lässt sich diese Schwäche umkehren?
Eine verborgene Bremse für die körpereigenen Krebsbekämpfer
Die Forschenden konzentrierten sich auf das hepatozelluläre Karzinom, die häufigste Form des primären Leberkrebses, die auf heutige Immuntherapien schlecht anspricht. Mittels Einzelzell-RNA-Sequenzierung untersuchten sie Tausende von Zellen aus Lebertumoren und dem umliegenden nicht-tumorösen Gewebe von Patientinnen und Patienten. Sie fanden heraus, dass ein Adapterprotein namens SAMSN1, das zuvor mit Immunregulation bei anderen Erkrankungen in Verbindung gebracht worden war, in NK-Zellen innerhalb der Tumoren besonders erhöht ist. Höhere SAMSN1-Spiegel korrelierten stark mit geringeren Mengen an Granzyme B — einer Schlüsselkomponente, mit der NK-Zellen Krebs abtöten — und mit schlechterem Überleben in großen öffentlichen Krebsdatensätzen. Im Gegensatz dazu zeigten andere Immunzellen im Tumor nur schwächere oder keine solche Erhöhung, was auf eine spezifische Rolle von SAMSN1 bei der Dämpfung der NK-Zell-Aktivität hinweist.
Patientenproben zeigen geschwächte NK-Feuerkraft
Um zu prüfen, wie sich dies in echten Tumoren äußert, analysierte das Team Immunzellen aus dem Kern von Lebertumoren und dem umgebenden Gewebe mittels hochdimensionaler Massencytometrie. NK-Zellen waren außerhalb des Tumors häufiger und dort stärker mit Granzyme B ausgerüstet als im Tumorinneren. Innerhalb des Tumors hatten NK-Zellen mit erhöhtem SAMSN1 deutlich weniger Granzyme B und zeigten eine stärkere Assoziation mit inhibitorischen „Checkpoint“-Markern, die Erschöpfung signalisieren. Praktisch bedeutet das: NK-Zellen in Lebertumoren sind nicht nur in effektiver Zahl reduziert, sondern auch weniger in der Lage, die molekularen Waffen abzufeuern, die nötig sind, um Krebszellen zu zerstören — genau dort, wo sie am dringendsten gebraucht werden.
Deaktivierung von SAMSN1 stellt NK-Angriff bei Mäusen wieder her
Die Forschenden wandten sich anschließend Mausmodellen zu, um zu testen, ob SAMSN1 diese Schwäche verursacht oder nur damit assoziiert ist. Mäuse, bei denen das Samsn1-Gen fehlte, entwickelten kleinere Lebertumoren, nachdem Krebszellen direkt in die Leber eingebracht wurden — ein Modell, das die menschliche Erkrankung nachahmt. Ihre NK-Zellen produzierten mehr Granzyme B und Interferon-gamma, und die Tiere überlebten länger, obwohl die Gesamtzahl der NK- und T-Zellen in den Tumoren unverändert blieb. Wichtig ist, dass, wenn die Forschenden Samsn1 nur in NK-Zellen entfernten — alle anderen Immunzellen blieben unberührt — die Vorteile im Wesentlichen gleich blieben: geringere Tumorlast und besseres Überleben. Ähnliche Effekte sah man in Modellen für Darmkrebs und Melanom, was darauf hindeutet, dass das Entfernen dieser Bremse von NK-Zellen die Anti-Tumor-Immunität über verschiedene Tumorarten hinweg stärken kann.
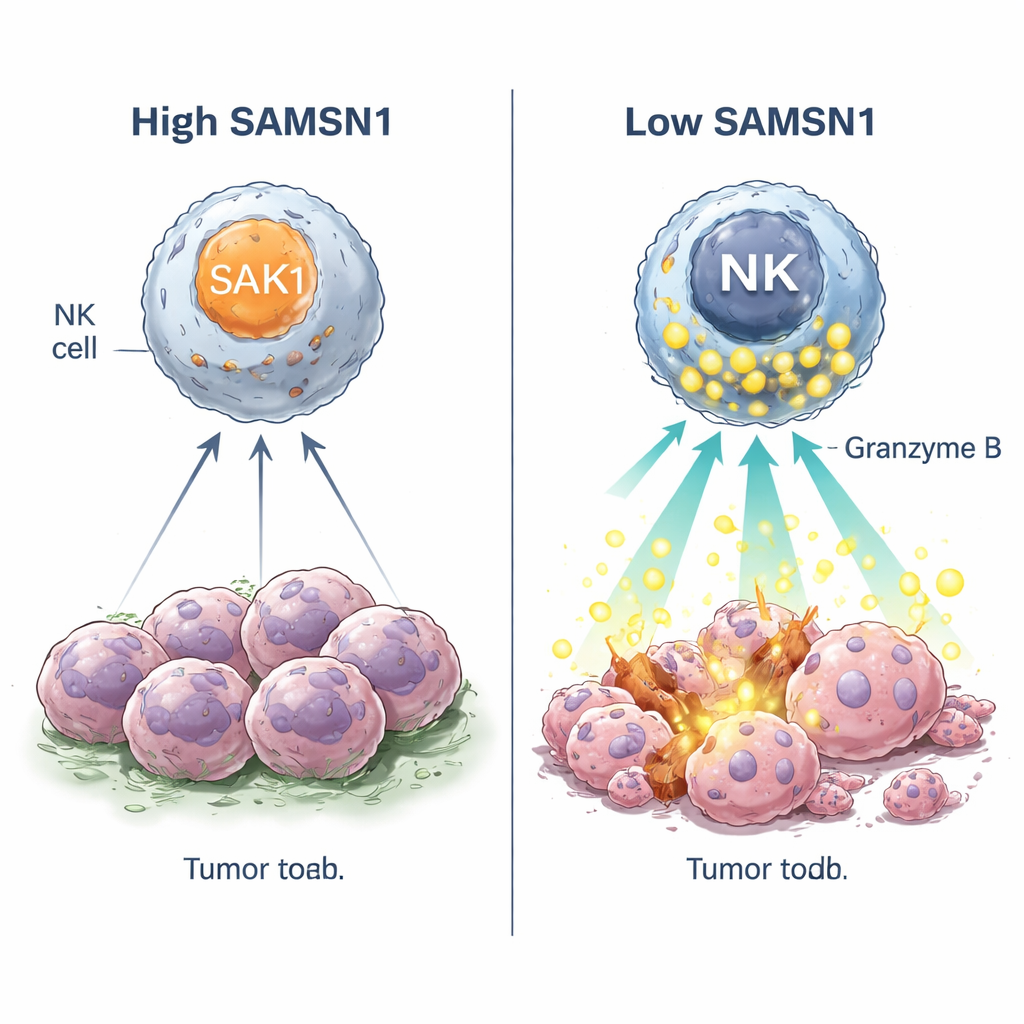
Humanen NK-Zellen zeigen dasselbe Muster
In Experimenten mit humanen Zellen nutzte das Team die CRISPR-Geneditierung, um SAMSN1 in NK-Zellen von Blutspendern auszuschalten. Diese editieren NK-Zellen zeigten mehr Aktivierungsmarker und produzierten mehr Granzyme B und Perforin, die Proteine, die Löcher in Zielzellen stanzen. In einer NK-Zell-Linie, die häufig in der Therapieforschung verwendet wird, förderte das Abschalten von SAMSN1 das Zellwachstum und die Tumor-kill-Aktivität, während das erzwungene Überexprimieren von SAMSN1 die Proliferation der NK-Zellen verlangsamte, Erschöpfungszeichen verstärkte und den zellulären Stoffwechsel in einer Weise veränderte, die zu einer müden, weniger effektiven Immunzelle passt. Wenn SAMSN1-überexprimierende NK-Zellen in immunsupprimierte Mäuse mit humanen Lebertumoren injiziert wurden, kontrollierten sie das Tumorwachstum deutlich schlechter als Kontroll-NK-Zellen.
Was das für künftige Leberkrebsbehandlungen bedeutet
Zusammen identifizieren diese Ergebnisse SAMSN1 als einen bislang wenig beachteten „Checkpoint“, der wie eine interne Bremse auf NK-Zellen wirkt, besonders in Lebertumoren. Für Laien lautet die Kernbotschaft: NK-Zellen können mächtige Krebsassassinen sein, aber beim hepatozellulären Karzinom werden viele von ihnen durch SAMSN1 in einen trägen, erschöpften Zustand versetzt. Das Entfernen oder Blockieren dieses Proteins in NK-Zellen weckt ihre Tötungskapazität wieder, verkleinert Tumore und verlängert das Überleben in Tiermodellen. Diese Arbeit legt nahe, dass Medikamente oder Zelltherapien, die SAMSN1 hemmen, eines Tages bestehende Behandlungen ergänzen könnten, sodass die angeborenen Immunzellen der Patienten bessere Chancen haben, Leberkrebs und möglicherweise andere solide Tumoren zu bekämpfen.
Zitation: Wang, R., Chen, H., Liu, H. et al. SAMSN1 restrains NK cell mediated anti-tumor immunity in hepatocellular carcinoma. Nat Commun 17, 1903 (2026). https://doi.org/10.1038/s41467-026-68661-4
Schlüsselwörter: Leberkrebs, natürliche Killerzellen, Immuntherapie, Immun-Checkpoints, SAMSN1