Clear Sky Science · de
Molekulare Erkennung von Thyreoglobulin durch Sortilin
Wie Schilddrüsenzellen entscheiden, wann sie Hormon freigeben
Schilddrüsenhormone stellen einen Teil unseres metabolischen „Thermostats“ ein und beeinflussen alles von Herzfrequenz bis Körpertemperatur. Diese Hormone werden in einem riesigen Protein namens Thyreoglobulin aufgebaut und gespeichert. Die vorliegende Studie zeigt, wie ein anderes Protein, Sortilin, den Schilddrüsenzellen hilft zu entscheiden, welche Form von Thyreoglobulin wieder in die Zelle aufgenommen werden soll, damit das Hormon ins Blut freigesetzt werden kann — eine Entscheidung, die letztlich beeinflusst, wie viel Schilddrüsenhormon dem Körper zur Verfügung steht.
Ein Speicherprotein, das auf Verarbeitung wartet
Thyreoglobulin ist ein massives, Y‑förmiges Protein, das von Schilddrüsenzellen produziert und in eine gelartige Umgebung, das Kolloid, sezerniert wird. Dort dient es sowohl als Rohmaterial als auch als Lager für Schilddrüsenhormone: bestimmte Bausteine (Aminosäuren) innerhalb des Thyreoglobulins werden mit Iod chemisch verändert und bilden so die Hormone, die noch im größeren Protein eingebettet sind. Um diese Hormone freizusetzen, muss Thyreoglobulin wieder in die Zelle aufgenommen, in Recycling‑Kompartimenten (Lysosomen) zerschnitten und die Hormonstücke ins Blut transportiert werden.
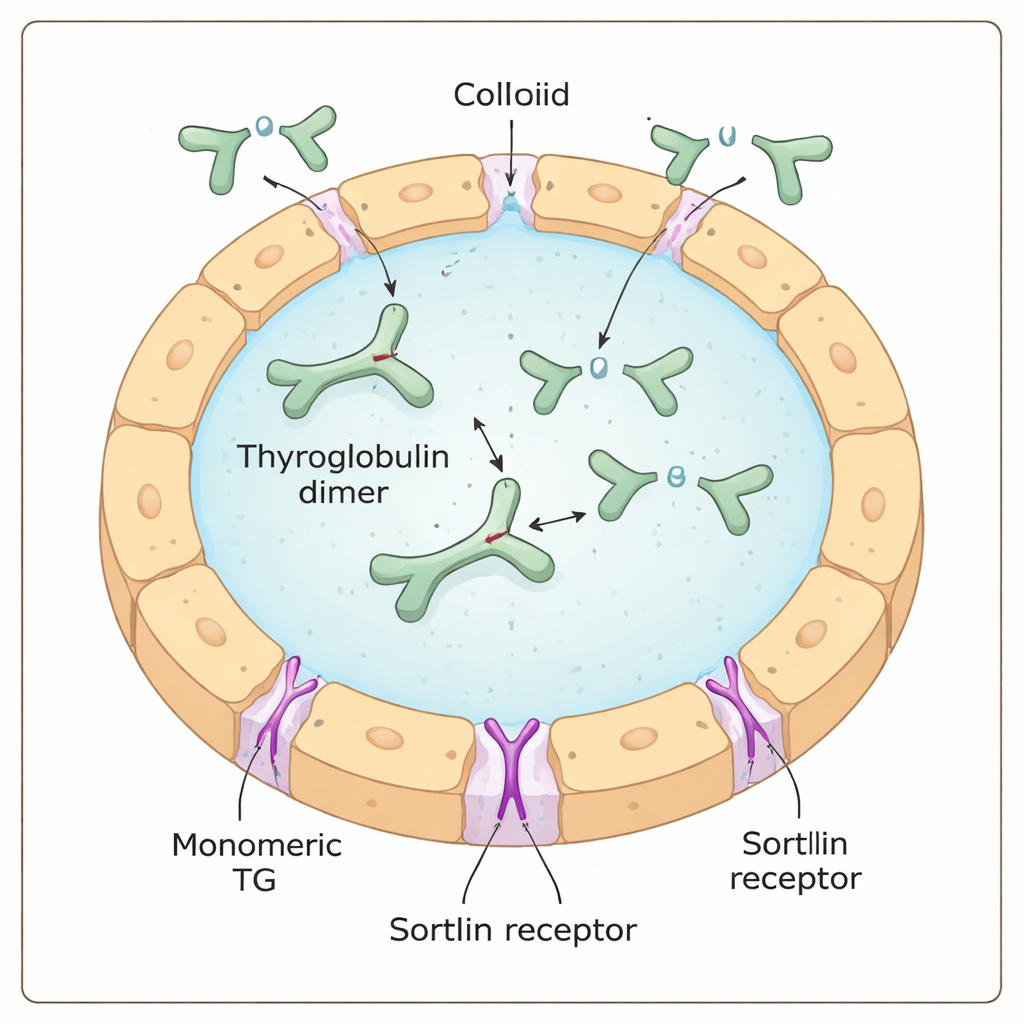
Ein zellulärer Türsteher mit versteckter Vorliebe
Der Rezeptor Sortilin wurde als einer der „Türsteher“ vorgeschlagen, die Thyreoglobulin an der Zelloberfläche binden und nach innen leiten. Frühere Arbeiten deuteten an, dass Sortilin stark iodiertes Thyreoglobulin bevorzugt, was die Vermutung nahelegte, der Rezeptor könnte den Iod‑Gehalt direkt erkennen. Mit einer Kombination aus biochemischen Tests, Einzelmolekül‑Massenspektrometrie und zellbasierten Aufnahmeversuchen fanden die Autoren stattdessen, dass Sortilin eine monomere (einzelne) Form von Thyreoglobulin deutlich gegenüber der häufigeren gepaarten, dimeren Form bevorzugt. Je mehr Monomer in einer Probe vorhanden war, desto effizienter bildeten sich Komplexe mit Sortilin und desto stärker wurde das Protein von Schilddrüsenzellen internalisiert — unabhängig davon, wie viel Iod es trug.
Der Kontaktpunkt unter dem Mikroskop
Um diese Präferenz auf atomarer Ebene zu verstehen, nutzte das Team hochauflösende Kryo‑Elektronenmikroskopie und quervernetzende Massenspektrometrie. Diese Methoden zeigten, dass Sortilin einen kurzen, flexiblen Schwanz am C‑Terminus (einem Ende) des monomeren Thyreoglobulins erkennt. Dieser Schwanz schiebt sich in eine zentrale Höhlung von Sortilin, die wie ein zehnblättriges Propellerblatt geformt ist, und dockt an zwei kleinen „Hotspots“ im Inneren an. Auffällig ist, dass im dimeren Thyreoglobulin ein Teil der Region um diesen Schwanz verborgen liegt, sodass Sortilin nicht darauf zugreifen kann — das erklärt, warum das Dimer ein schlechterer Partner ist. Die Daten deuten darauf hin, dass extrazelluläres Beschneiden oder Auflockern von Thyreoglobulin — durch natürliche Proteindegradation — dabei hilft, Dimeren in Monomere zu überführen, die Sortilin erfassen kann.
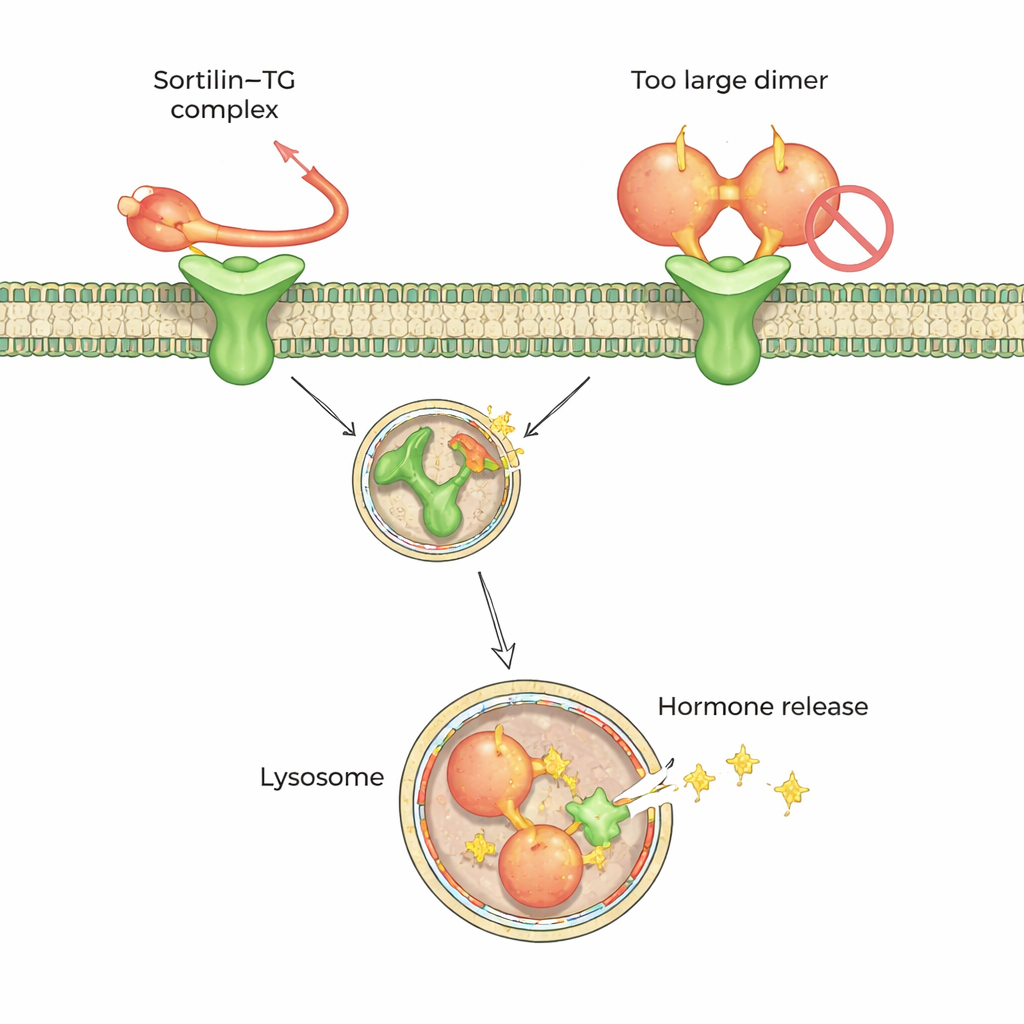
Ein gemeinsamer Andockcode für viele Frachtproteine
Sortilin ist nicht nur ein Schilddrüsenprotein; es steuert den Transport vieler verschiedener Moleküle im Körper, darunter Faktoren, die mit Herzkrankheiten und Gehirnstörungen in Verbindung stehen. Indem sie ihre strukturellen Daten mit modernen Strukturvorhersage‑Werkzeugen wie AlphaFold und AlphaPulldown kombinierten, verglichen die Forscher, wie Dutzende bekannter Sortilin‑Partner in die Propellermulde binden könnten. Sie fanden ein wiederkehrendes Muster: Viele Frachtstoffe präsentieren ein ungeordnetes Peptidsegment von etwa zwanzig Aminosäuren, das in dieselbe Tasche passt wie der Schwanz des Thyreoglobulins, manchmal in derselben Richtung wie das bekannte Gehirnpeptid Neuropeptidstalin und manchmal in entgegengesetzter Orientierung. Trotz der umgekehrten Ausrichtung teilen diese Peptide ähnliche Eigenschaften — eine saure oder negativ geladene Gruppe an einem Ende, eine sperrige aromatische Aminosäure am anderen und ein flexibler, häufig prolinreicher Abschnitt dazwischen.
Warum Iod weniger zählt als Form
Da der Schlüsselkontakt zwischen Sortilin und Thyreoglobulin dieser flexible Schwanz ist, prüften die Autoren, ob das Iodieren einer hormonausbildenden Tyrosin‑Rest im Schwanz die Bindung verändern würde. Das war nicht der Fall: Ein synthetisches Peptid, das ein vollständig ausgebildetes Schilddrüsenhormon trug, verhielt sich nahezu identisch mit der unveränderten Version. Modellierungen zeigten, dass der iodierte Ring ins Lösungsmittel herausragt, ohne neue enge Kontakte zu bilden. Zusammen mit den Aufnahmeexperimente stützt dies eine revidierte Sicht: Sortilin „zählt“ nicht die Iodatome am Thyreoglobulin. Stattdessen erkennt es, ob das Protein ausreichend gelockert oder teilweise degradiert wurde, sodass seine monomere Form und der Schwanz in der richtigen Weise zugänglich sind.
Was das für die Schilddrüsengesundheit bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft, dass die Freisetzung von Schilddrüsenhormonen weniger durch einen eingebauten Iod‑Sensor gesteuert wird als durch eine mechanische Prüfung von Proteinform und Flexibilität. Sortilin wirkt wie ein Scanner an der Zelloberfläche, der nach Thyreoglobulinmolekülen sucht, die gelockert oder zugeschnitten zu Monomeren wurden, und diese dann nach innen zieht, damit das Hormon endgültig freigesetzt und Iod recycelt werden kann. Diese Arbeit klärt einen wichtigen Schritt in der Biologie der Schilddrüsenhormone und deutet darauf hin, dass Medikamente, die Sortilin blockieren — die derzeit für andere Krankheiten untersucht werden — unbeabsichtigt die Handhabung von Schilddrüsenhormonen verändern könnten, indem sie diesen Erkennungsschritt stören.
Zitation: Boniardi, I., Tanzi, G., Di Ianni, A. et al. Molecular recognition of thyroglobulin by sortilin. Nat Commun 17, 2004 (2026). https://doi.org/10.1038/s41467-026-68658-z
Schlüsselwörter: Schilddrüsenhormon, Thyreoglobulin, Sortilin, Proteintransport, Endozytose