Clear Sky Science · de
Die Brückehelix von Cas12a ist ein allosterischer Regulator der R‑Loop‑Bildung und der RuvC‑Aktivierung
Warum das für die Genbearbeitung wichtig ist
Viele leistungsfähige Werkzeuge zur Genbearbeitung, einschließlich solcher, die in aufkommenden Therapien und schnellen Diagnosetests verwendet werden, beruhen auf CRISPR‑Proteinen, die DNA an ausgewählten Stellen zerschneiden. Treffen diese molekularen Scheren jedoch die falsche Stelle, können sie schädliche Nebenwirkungen verursachen. Diese Studie zerlegt ein winziges bewegliches Bauteil im Cas12a‑Editor, die sogenannte Brückehelix, und zeigt, wie ihre Formveränderungen als interner Sicherheitsmechanismus wirken, der die korrekte Erkennung des Ziels mit dem DNA‑Schnitt verknüpft. Das Verständnis dieses Schalters liefert eine Landkarte, um CRISPR‑Werkzeuge zu entwickeln, die sowohl präziser als auch sicherer für medizinische und biotechnologische Anwendungen sind.
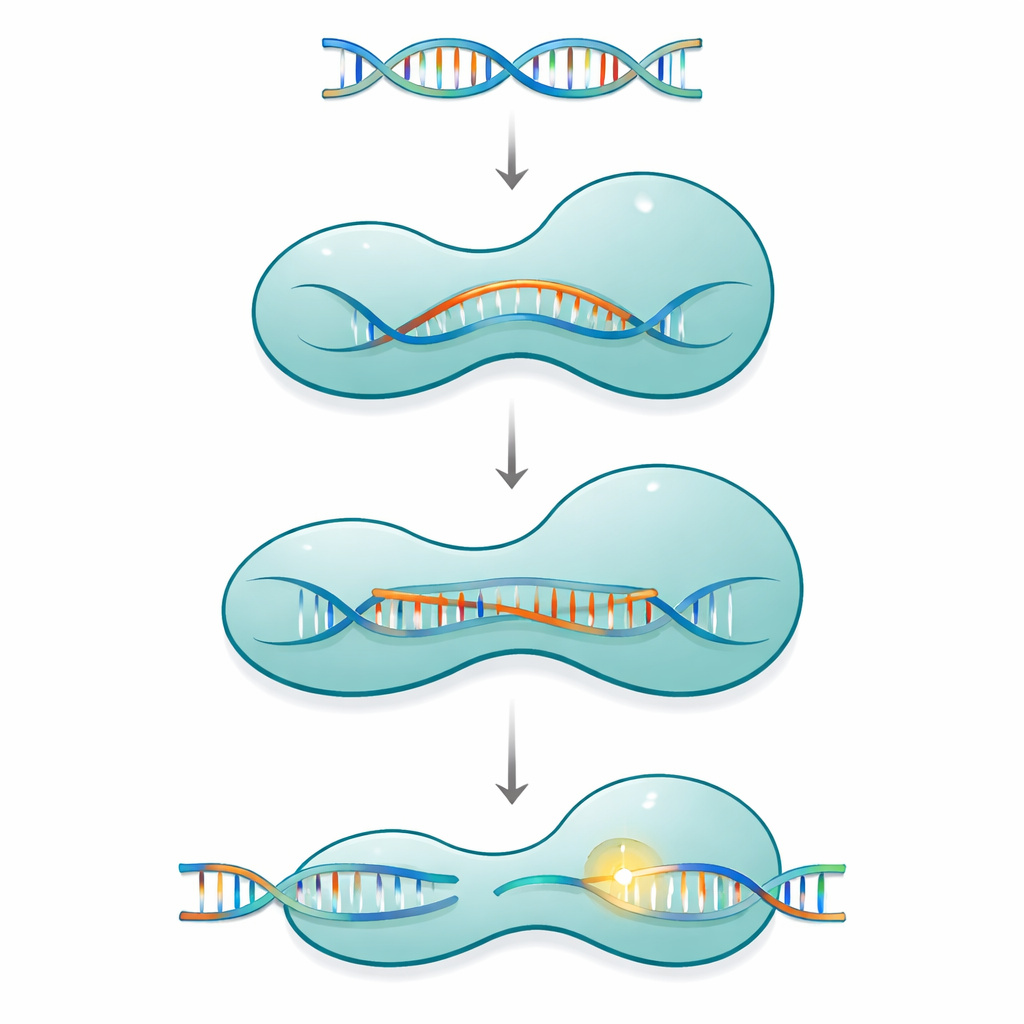
Eine molekulare Klammer mit beweglichen Teilen
Cas12a gehört zu einer Familie einkörperiger CRISPR‑Systeme, die eine kurze Guide‑RNA verwenden, um passende DNA in Viren oder im Genom einer Zelle zu finden und zu zerschneiden. Das Protein ähnelt einer zweiteiligen Klammer: einer Erkennungsseite, die die Sequenz überprüft, und einer Schnittseite, die die chemische Maschinerie enthält. Diese beiden Hälften sind durch ein schlankes, positiv geladenes Segment verbunden, die Brückehelix. Wenn Cas12a seine Guide‑RNA und anschließend sein DNA‑Ziel bindet, verhält sich das Protein nicht wie ein starres Werkzeug. Stattdessen durchläuft es eine Folge großer und kleiner Formänderungen, die sich allmählich um eine wachsende RNA–DNA‑Hybridstruktur schließen, bekannt als R‑Loop, und erst die Schneidstelle vollständig aktivieren, wenn eine ausreichend lange Strecke korrekter Basenpaarung gebildet ist.
Den eingebauten Sicherheitsmechanismus untersuchen
Die Forschenden konzentrierten sich auf ein Cas12a aus dem Bakterium Francisella novicida und eine zuvor entwickelte Variante, bei der zwei Aminosäuren der Brückehelix durch Proline ersetzt wurden — eine Änderung, die dafür bekannt ist, Helices zu versteifen oder zu unterbrechen. Diese Variante, genannt FnoCas12aKD2P, schneidet DNA selektiver, aber langsamer als das natürliche Protein. Mithilfe kryo‑Elektronenmikroskopie hielten sie fünf verschiedene strukturelle Momentaufnahmen dieser Variante fest, gebunden an ihre Guide‑RNA und ein Stück Ziel‑DNA. Diese Aufnahmen zeigen das Protein in unterschiedlichen Stadien seines Aktivierungswegs, von der frühen ersten DNA‑Erkennung bis zu späteren Zuständen, in denen ein Teil des RNA–DNA‑Hybrids gebildet ist, die volle Schneidbereitschaft jedoch noch nicht erreicht wurde.
Wie Formänderungen präzises Schneiden antreiben
Der Vergleich der Variante mit zuvor bestimmten Strukturen des normalen Cas12a offenbarte ein klares Muster. Im natürlichen Protein verwandelt sich ein Segment der Brückehelix von einer lockeren Schleife in eine längere, gerade Helix und knickt in Richtung des wachsenden RNA–DNA‑Hybrids, wobei es engen Kontakt zu diesem aufnimmt. Gleichzeitig löst sich eine benachbarte Helix in der Schnittdomäne, und eine kleine Region, die als „Deckel“ bezeichnet wird und normalerweise die aktive Stelle blockiert, verwandelt sich von einer Schleife in eine Helix und klappt auf. Zusammen öffnen diese koordinierten Bewegungen eine Tasche, die einen einzelnen DNA‑Strang einlässt, damit er geschnitten werden kann. In der Prolin‑Variante kann die Brückehelix diesen Schleifen‑zu‑Helix‑Übergang oder die richtige Krümmung nicht vollständig durchführen. Infolgedessen bleibt der RNA–DNA‑Hybrid verzerrt und weiter entfernt, der Deckel verharrt in einem geschlossenen, schleifenartigen Zustand, und der Komplex erreicht selten eine vollständig prä‑katalytische Konformation. Dieser mechanische Engpass verlangsamt das Schneiden am Ziel und erschwert es fehlangepasster DNA, die internen Prüfpunkte zu passieren.
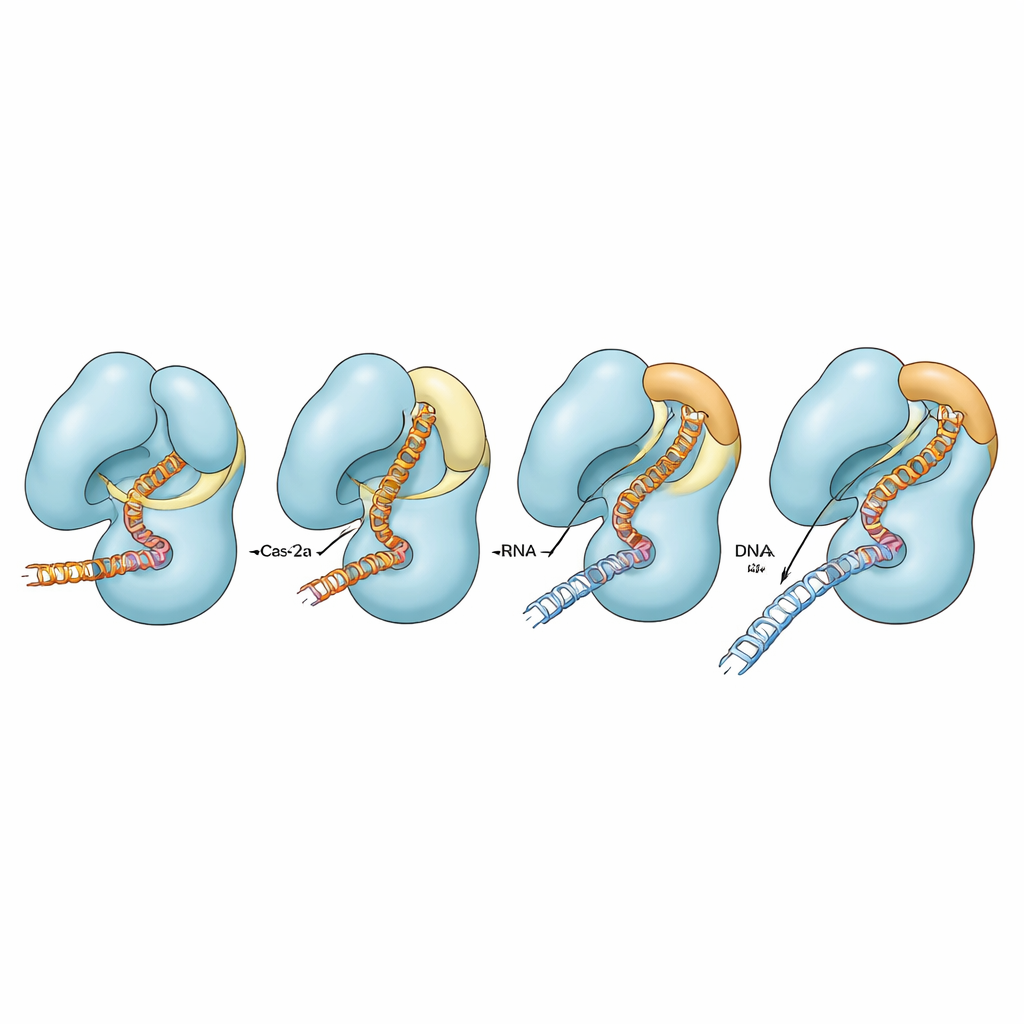
Genauigkeit feinjustieren durch Anpassung von Kontakten
Um zu prüfen, wie verschiedene Kontakte rund um den Deckel und die Brückehelix zur Aktivität beitragen, veränderten die Autor:innen bestimmte geladene Reste, die diese Bereiche verbinden. Beim normalen Cas12a hatten das Aufbrechen dieser Kontakte nur mäßige Auswirkungen auf das Schneiden perfekt übereinstimmender DNA, obwohl unter manchen Bedingungen die Effizienz des Schnitts des zweiten DNA‑Strangs bei Vorliegen von Fehlpaarungen beeinflusst wurde. In dem beeinträchtigten Brückehelix‑Hintergrund verringerten dieselben Substitutionen jedoch die Spaltung beider Stränge stark oder schafften sie nahezu vollständig ab, besonders wenn Guide und DNA nicht perfekt übereinstimmten. Computersimulationen stützten diese Befunde und zeigten, dass nur wenn die Brückehelix ihre helikale Form vollständig annehmen kann, Brücke, die angrenzende Helix, der Deckel und die Nukleinsäuren in stark koordinierter Weise bewegen. Ist die Helix beeinträchtigt, entkoppeln sich diese Bewegungen teilweise oder vollständig, und das Enzym hat Schwierigkeiten, seinen katalytischen Zyklus abzuschließen.
Ein Gestaltungsleitfaden für die nächste Generation von CRISPR‑Werkzeugen
Insgesamt offenbart die Arbeit die Brückehelix als internen Kontrollhebel, der die Länge und Qualität des RNA–DNA‑Hybrids mit dem Öffnen der Schnitttasche in Cas12a verknüpft. Indem das Protein gezwungen wird, vor dem Abschneiden der DNA eine spezifische Abfolge von Formänderungen zu durchlaufen, erzwingt dieser Mechanismus auf natürliche Weise die Diskriminierung von Fehlpaarungen. Die Ergebnisse helfen zu erklären, warum gezielte Veränderungen in diesem kleinen Bereich Cas12a‑Varianten mit reduziertem Off‑Target‑Schneiden und verminderter „kollateraler“ DNA‑Aktivität hervorbringen können — Eigenschaften, die für sicherere Genom‑Editierung und Diagnostik wünschenswert sind. Darüber hinaus unterstreicht die Studie, wie subtile Verschiebungen kurzer Helices langreichweitige Kommunikation in großen molekularen Maschinen koordinieren können, und liefert allgemeine Prinzipien für das Engineering hochpräziser Nukleinsäure‑verarbeitender Enzyme.
Zitation: Ganguly, C., Aribam, S.D., dos Santos, A.M. et al. Bridge helix of Cas12a is an allosteric regulator of R-loop formation and RuvC activation. Nat Commun 17, 2126 (2026). https://doi.org/10.1038/s41467-026-68657-0
Schlüsselwörter: CRISPR‑Cas12a, Genbearbeitungs‑Genauigkeit, Brückehelix, R‑Loop‑Bildung, allosterische Regulation