Clear Sky Science · de
RoboA verstärkt das phänotypische Schicksal planarer Stammzellen über FoxA und Anosmin1a
Wie Würmer ihre Organe nachwachsen lassen
Einige Plattwürmer können fast jeden fehlenden Körperteil nachbilden, von ihrer Fressröhre bis zum Gehirn. Diese bemerkenswerte Fähigkeit beruht auf erwachsenen Stammzellen, die je nach Bedarf in viele verschiedene Zelltypen umgewandelt werden können. Aber bei so viel Freiheit: Wie verhindern diese Zellen, dass falsches Gewebe am falschen Ort entsteht — zum Beispiel Magenschleimhautzellen im Kopf statt Neuronen? Diese Studie nutzt die planare Flachwurmart, um zu ergründen, wie ein kleiner Satz von Signalen hochflexible Stammzellen während der Regeneration auf dem richtigen Weg hält.
Der regenerierende Wurm und sein verborgenes Potenzial
Die Planarie Schmidtea mediterranea ist ein bevorzugtes Modell zur Untersuchung der Regeneration, weil eine große Population von Stammzellen im gesamten Körper verteilt ist. Ein wichtiges Organ ist der Pharynx, eine muskuläre Fressröhre, die in der Körpermitte liegt und beim Fressen mit der Außenwelt verbunden wird. Frühere Arbeiten zeigten, dass ein Gen namens foxA entscheidend für den Wiederaufbau dieses Pharynx nach Verletzung ist und dass normalerweise nur bestimmte Stammzellen in der Nähe des Pharynx foxA aktivieren. Die neue Studie stellt eine scheinbar einfache Frage: Was verhindert, dass Stammzellen in anderen Regionen — insbesondere im Kopf und Gehirn — ebenfalls eine Pharynx-Identität wählen?
Wenn die Führung fehlt
Die Forscher konzentrierten sich auf ein Rezeptorprotein namens RoboA, das in niedrigen Mengen in vielen Zelltypen, einschließlich Stammzellen, vorkommt. Wenn sie die RoboA-Aktivität mittels RNA-Interferenz verringerten, wuchsen die Tiere nach Schnitten häufig zusätzliche, fehlplatzierte Pharynxstrukturen. Genauere Untersuchungen zeigten etwas Subtileres: Selbst in unverletzten Würmern führte die Reduktion von RoboA zum Auftreten pharynxähnlicher Neuronen und Muskeln im Gehirnbereich. Diese „ektopen Pharynxneuronen“ verhielten sich in ihrer Genexpression wie normale Pharynxzellen, befanden sich aber am falschen Ort. Wichtig ist, dass der Gesamtbauplan und die Gehirnarchitektur weitgehend intakt blieben, was darauf hindeutet, dass RoboA nicht den gesamten Körper umgestaltet, sondern vielmehr fein abstimmt, was benachbarte Stammzellen werden.
Ein Dreiparteien-Schalter für das Zellschicksal
Um zu verstehen, wie RoboA wirkt, suchte das Team nach Partnern außerhalb der Zelle. Obwohl Robo-Proteine am besten dafür bekannt sind, an ein Ligandenmolekül namens Slit zu binden, reproduzierte die Reduktion von Slit nicht das Auftreten fehlplatzierter Pharynxzellen. Ein großer RNAi-Screen sekretierter und membranständiger Proteine identifizierte stattdessen Anosmin1a (Anos1a), ein sekretiertes Protein, das mit einem menschlichen Faktor verwandt ist, der bei der Kallmann-Syndrom-Pathologie eine Rolle spielt. Die Verringerung von Anos1a führte zu ähnlichen zusätzlichen Pharynxneuronen, und kombinierte RoboA–Anos1a-Knockdowns verhielten sich, als würden sie im selben Signalweg arbeiten. Zeitgleich zeigte die molekulare Profilierung, dass der Transkriptionsfaktor FoxA im Zentrum der Entscheidungsfindung sitzt: Ist RoboA vorhanden, hält es FoxA in Kopfstammzellen ausgeschaltet; wird die RoboA-Signalgebung entfernt, schaltet sich FoxA ein und dieselben Stammzellen können selbst im Gehirn eine Pharynx-Neuronen-Identität annehmen.
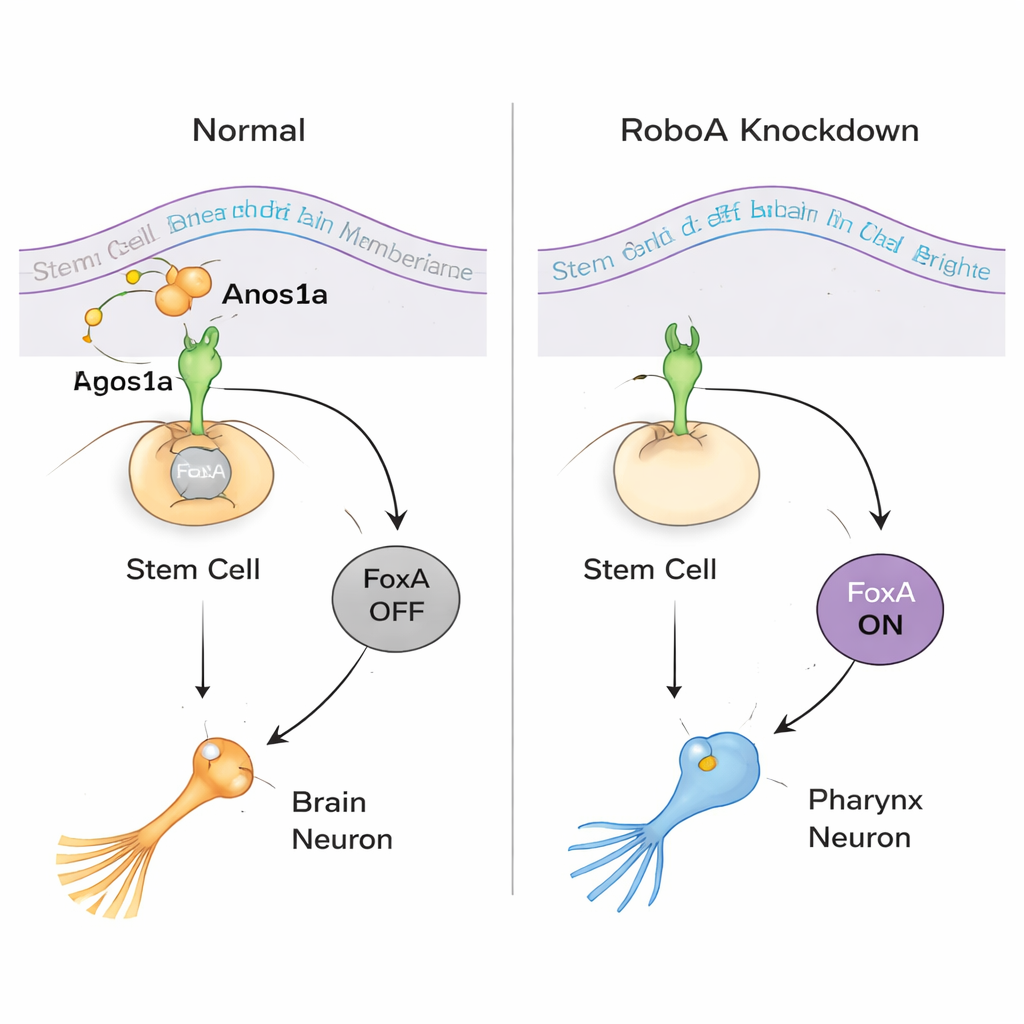
Aufdeckung einer zweiseitigen Wahl in Stammzellen
Das Team fragte dann, ob diese Flexibilität in beide Richtungen funktioniert. In normalen Tieren verlassen sich Stammzellen um den Pharynx herum auf FoxA, um Pharynxneuronen und epithelialen Zellen zu werden, während Pharynxmuskeln einem anderen Entwicklungsweg folgen. Wenn FoxA über längere Zeit abgeschaltet wurde, verloren Würmer ihre Pharynxe vollständig und entwickelten abnorme Auswüchse in der Körpermitte. Einzelzell-RNA-Sequenzierung und Markeranalysen zeigten, dass diese Auswüchse viele Zelltypen enthielten, die normalerweise auf den Kopf beschränkt sind, einschließlich Augen- und gehirnspezifischer Neuronen. Mit anderen Worten: Fehlt FoxA dort, wo der Pharynx entstehen sollte, tendieren lokale Stammzellen standardmäßig zu einem gehirnähnlichen Schicksal. Dieser Befund zeigt, dass dieselben Stammzellen je nach empfangenem Signal entweder in Richtung „Pharynx“ oder „Gehirn“ gedrängt werden können.
Feinabstimmung der Regeneration, nicht das Umzeichnen der Karte
In der Zusammenschau schlagen die Autoren vor, dass die Regeneration bei Planarien auf zwei Ebenen gesteuert wird. Breite „Positionskontroll“-Signale, wie Wnt und andere Musterungsmoleküle, legen die grobe Karte von Kopf, Rumpf und Schwanz fest. Darauf aufbauend wirken lokale „Schicksal-verstärkende“ Gene wie RoboA und Anos1a als Sicherheitsbarrieren, die unpassende Optionen blockieren. Im Kopf hält die RoboA–Anos1a-Signalgebung FoxA ausgeschaltet, sodass Stammzellen Gehirnneuronentypen statt Pharynxzellen produzieren; in Pharynxnähe darf sich FoxA einschalten und pharynxspezifische Schicksale antreiben. Diese geschichtete Kontrolle erlaubt es planaren Stammzellen, außerordentlich plastisch zu bleiben und gleichzeitig Organe am richtigen Ort nachzubilden — ein Leitbild dafür, wie robuste Regeneration mit strikter anatomischer Ordnung koexistieren kann.
Zitation: Wang, KT., Tsai, FY., Chen, YC. et al. RoboA reinforces planarian stem cell fate through FoxA and Anosmin1a. Nat Commun 17, 1971 (2026). https://doi.org/10.1038/s41467-026-68656-1
Schlüsselwörter: Regeneration von Planarien, Stammzellplastizität, Organmusterbildung, RoboA-Signalgebung, Transkriptionsfaktor FoxA