Clear Sky Science · de
Stenotrophomonas fördert das Fortschreiten gastrointestinaler Tumoren durch Abbau von STING in Tumorzellen und abgeschwächte Immunantwort
Verborgene Keime in Tumoren
Die meisten Menschen wissen, dass die Mikroben in unserem Darm Verdauung und sogar Stimmung beeinflussen können, doch nur wenige ahnen, dass lebende Bakterien tatsächlich in Krebszellen selbst einziehen können. Diese Studie zeigt, wie ein häufiges Umweltbakterium, Stenotrophomonas, in gastrointestinalen Tumoren verweilt und deren Wachstum fördert, während es gleichzeitig die Immunabwehr des Körpers abschwächt und moderne Krebsimmuntherapien weniger wirksam macht.
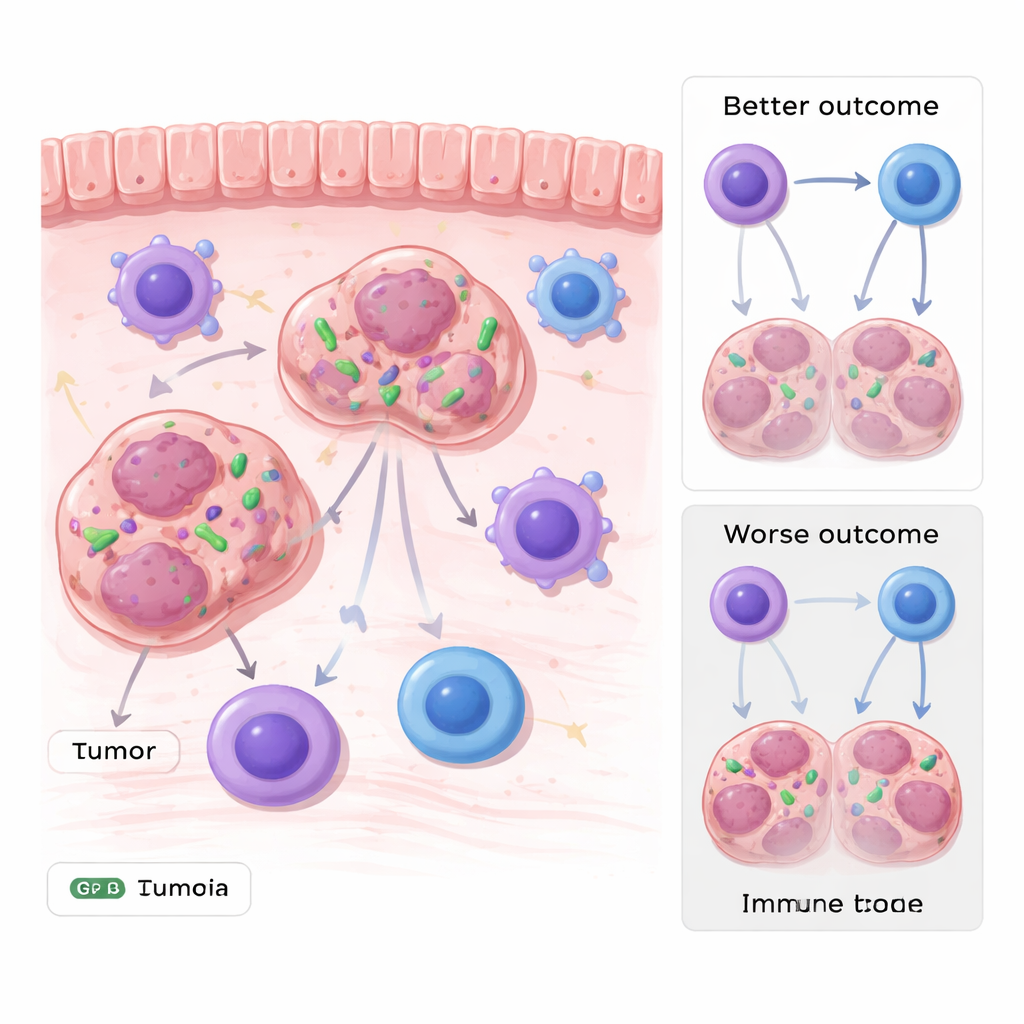
Bakterien leben in Krebszellen
Gastrointestinale Tumoren, etwa Magen- und Kolorektalkarzinome, wachsen in ständigem Kontakt mit den vielfältigen bakteriellen Gemeinschaften des Verdauungstrakts. Durch Auswertung mehrerer genetischer Datensätze von Patientinnen und Patienten und anschließende Validierung in Tumorproben fanden die Forschenden, dass DNA von Stenotrophomonas in mehreren Arten gastrointestinaler Tumoren ungewöhnlich häufig vorkam. Wichtig war, dass es sich nicht nur um Oberflächenkontamination handelte: Bildgebende Verfahren, darunter fluoreszierende Sonden und Elektronenmikroskopie, zeigten ganze Bakterien im Zytoplasma von Tumorzellen. Patientinnen und Patienten, deren Tumoren höhere Mengen dieses Bakteriums enthielten, hatten tendenziell eine schlechtere Prognose, was das Mikrobenvorkommen mit ungünstigem Verlauf verknüpft.
Wie ein Mikroorganismus das immunologische Gleichgewicht kippt
Als Nächstes untersuchten die Forschenden, ob diese verborgenen Bakterien nur mit aggressiven Tumoren zusammenfallen oder aktiv zur Krankheitsentwicklung beitragen. In Mausmodellen infizierten sie Tumorzellen mit fluoreszent markierten Stenotrophomonas, bevor sie diese in Tiere einpflanzten. Tumoren mit dem Bakterium wuchsen schneller und größer als bakterienfreie Tumoren, über mehrere Zelltypen hinweg. Bei Untersuchung der umgebenden Immunlandschaft stellten sie fest, dass die Gesamtzahl der Immunzellen, einschließlich T‑Zellen und Makrophagen, ähnlich war. Der entscheidende Unterschied lag in einer spezialisierten Untergruppe von Makrophagen, die das Molekül MHC‑II tragen und damit Tumorfragmente an zytotoxische T‑Zellen präsentieren. In Tumoren mit Stenotrophomonas waren diese MHC‑II‑positiven Makrophagen deutlich reduziert, und die T‑Zellen zeigten eine schwächere Tumorzell‑Abtötungsaktivität.
Unterbrechung eines zellulären Alarmsystems
Zur Aufklärung des Mechanismus konzentrierten sich die Forschenden auf einen wichtigen innerzellulären Alarmweg namens STING, der normalerweise fremde DNA erkennt und die Freisetzung antiviraler „Gefahr“-Signale, die Typ‑I‑Interferone, auslöst. In Laborversuchen produzierten Tumorzellen, die mit Stenotrophomonas infiziert waren, deutlich weniger Interferon‑beta, und Gene, die normalerweise durch diesen Weg aktiviert werden, waren unterdrückt. Die Studie zeigte, dass das Bakterium Stress im Proteinfaltungsbetrieb der Zelle, dem endoplasmatischen Retikulum, verursacht und anschließend einen Qualitätskontrollweg namens ER‑assoziierter Abbau (ERAD) kapert. Über ein Helferprotein namens SEL1L markiert dieser Weg das STING‑Protein zur Zerstörung im Proteasom der Zelle. Mit reduziertem STING‑Spiegel sendet die Tumorzelle einen schwächeren Alarm, was zu geringerer Interferonfreisetzung und nachgelagert zu einer abgeschwächten Aktivierung der MHC‑II‑positiven Makrophagen führt.
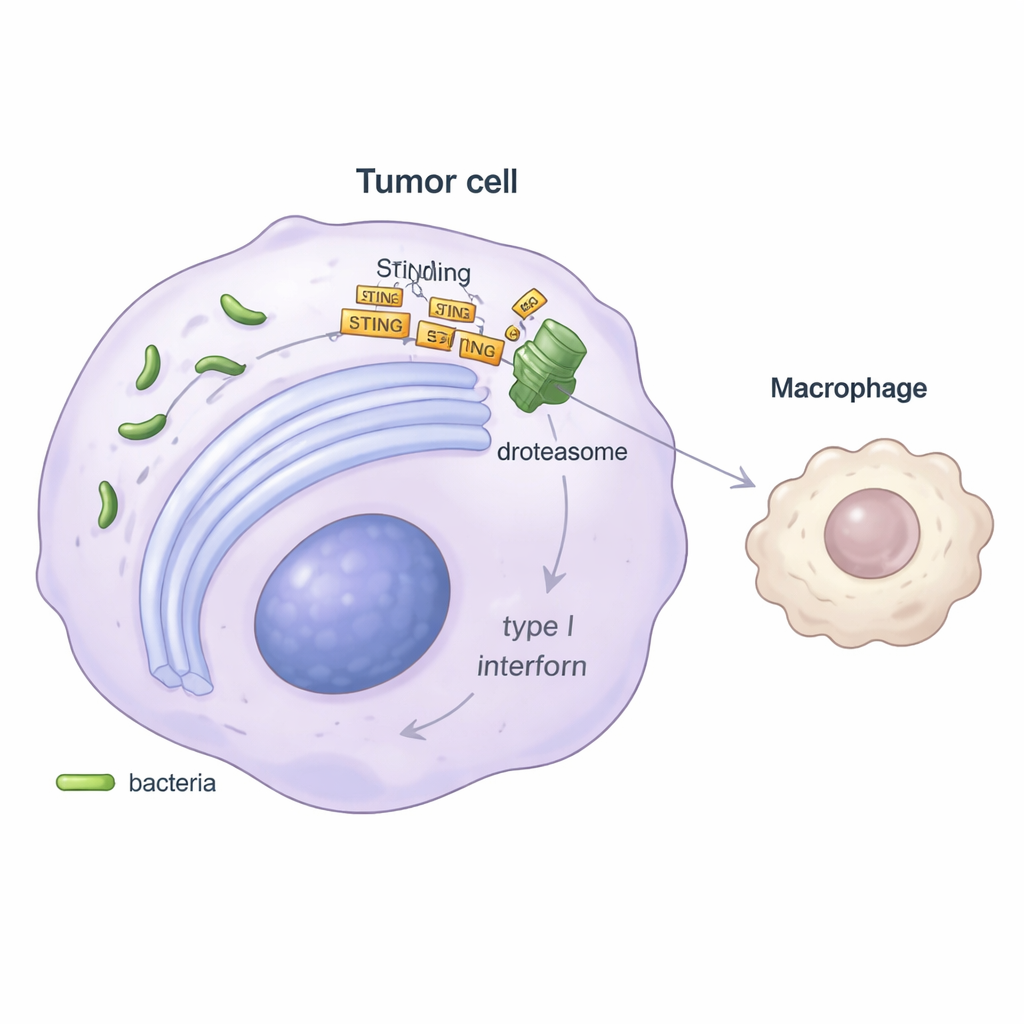
Unterminierung der Immuntherapie — und ein möglicher Ausweg
Da moderne Immuntherapien wie Anti‑PD‑1‑Medikamente auf eine kräftige T‑Zell‑Antwort angewiesen sind, prüfte das Team, wie intrazelluläres Stenotrophomonas die Behandlung beeinflusst. In Mäusen sprachen Tumoren mit dem Bakterium schlechter auf Anti‑PD‑1 an als bakterienfreie Tumoren, selbst in Kombination mit Chemotherapie. Die T‑Zellen in diesen Tumoren zeigten verringerte Aktivitäts‑ und Teilungsmarker, was mit schwacher immunologischer Stimulation übereinstimmt. Auffällig war, dass die Behandlung der Tiere mit dem Antibiotikum Levofloxacin, das Stenotrophomonas effektiv abtötet, das Tumorwachstum verlangsamte und die Ansprechrate auf Anti‑PD‑1 verbesserte. Die Wiederherstellung der Interferon‑Signalgebung mit einem klinisch verwendeten Interferonpräparat konnte ebenfalls die Population hilfreicher MHC‑II‑positiver Makrophagen retten und in einigen Fällen die T‑Zell‑Killing‑Funktion reaktivieren, was die zentrale Rolle dieses Signalwegs unterstreicht.
Was das für Patientinnen und Patienten bedeutet
Für Laien lautet die Kernbotschaft: Manche gastrointestinalen Krebserkrankungen können ein eigenes internes Mikrobiom „mitbringen“, das ihnen hilft, dem Immunsystem zu entkommen. Stenotrophomonas schwächt durch den Abbau des STING‑Alarmsystems in Tumorzellen die Immun‑Signale, die normalerweise Makrophagen und zytotoxische T‑Zellen mobilisieren würden. Das beschleunigt nicht nur das Tumorwachstum, sondern könnte auch erklären, warum bestimmte Patientinnen und Patienten keinen Nutzen aus starken Immuntherapien ziehen. Obwohl weitere Forschung nötig ist, bevor dies die klinische Praxis verändert, legen die Ergebnisse nahe, dass das Testen von Tumoren auf solche Bakterien — und deren gezielte Behandlung mit passenden Antibiotika oder Medikamenten, die STING stabilisieren — eines Tages die Ergebnisse für Menschen mit Magen‑ und Darmkrebs verbessern könnte.
Zitation: Feng, H., Chen, K., Xi, Z. et al. Stenotrophomonas promotes gastrointestinal tumor progression via STING degradation in tumour cells and mitigated immune response. Nat Commun 17, 2042 (2026). https://doi.org/10.1038/s41467-026-68649-0
Schlüsselwörter: Tumormikrobiom, gastrointestinale Krebsarten, Stenotrophomonas, STING-Signalweg, Krebs-Immuntherapie