Clear Sky Science · de
NR6A1 ist unerlässlich für die Spezifikation, Bildung und das Überleben von Neuralleistenzellen
Wie frühe Zellentscheidungen Gesicht und Körper formen
Bevor wir geboren werden, wandert eine besondere Zellgruppe, die Neuralleistenzellen genannt wird, durch den Embryo und hilft beim Aufbau von Gesicht, Herz, Nerven und mehr. Gehen diese Zellen fehl, können schwere Fehlbildungen entstehen. Die vorliegende Studie enthüllt einen bisher unterschätzten molekularen Schalter — ein Protein namens NR6A1 — das mitentscheidet, wann und wo sich Neuralleistenzellen bei Säugetierembryonen bilden und was passiert, wenn dieser Schalter ausfällt.
Die wandernden Baumeister des Embryos
Neuralleistenzellen entstehen sehr früh in der Entwicklung entlang der Grenze zwischen dem sich bildenden Gehirn und Rückenmark. Nachdem sie sich von diesem Gewebe gelöst haben, migrieren sie weite Strecken und schaffen zahlreiche Strukturen, von Gesichtsknochen und Knorpel bis zu Teilen des peripheren Nervensystems und Pigmentzellen in der Haut. Weil sie zu so vielen Organen beitragen, können selbst kleine Störungen in ihrer Bildung weitreichende Erkrankungen verursachen, die als Neurocristopathien bekannt sind, etwa kraniofaziale Syndrome wie Treacher-Collins. Zu verstehen, wie diese Zellen zunächst entstehen, ist daher zentral für die Erklärung sowohl normaler Entwicklung als auch angeborener Fehlbildungen.
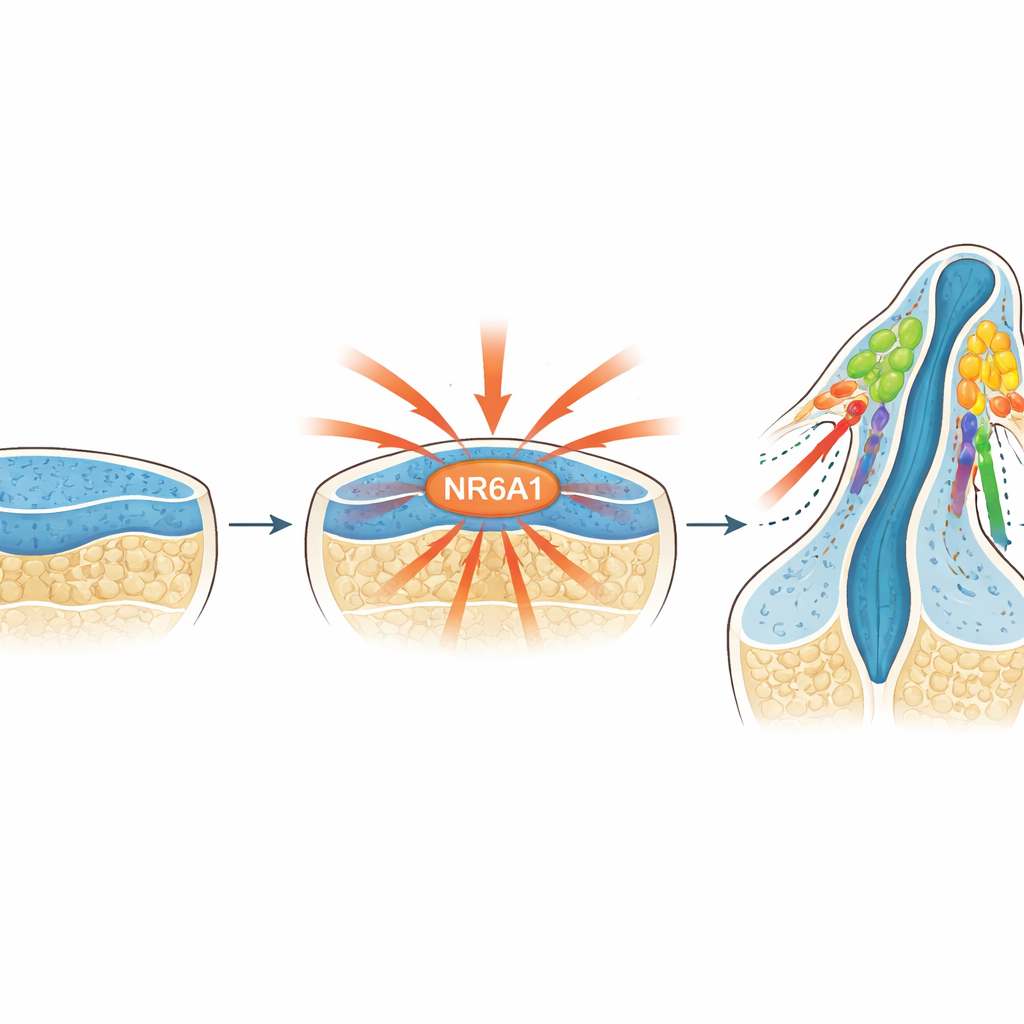
Ein neu erkannter Master-Schalter
Die Forschenden konzentrierten sich auf NR6A1, ein Mitglied der nukleären Rezeptorfamilie von Proteinen, die die Genaktivität steuern. Frühere Arbeiten deuteten bereits an, dass NR6A1 an Kopf- und Gesichtsanomalien beteiligt sein könnte, doch seine Rolle in Neuralleistenzellen war unbekannt. Durch das Verfolgen von NR6A1 in Maus-Embryonen kurz nach der Implantation entdeckte das Team, dass seine Präsenz eng mit dem Ort und der Zeit übereinstimmt, an denen Neuralleistenzellen normalerweise entstehen: Es tritt im frühen Neuralgewebe auf, konzentriert sich entlang der dorsalen (rückwärtigen) Seite des sich entwickelnden Gehirns und Rückenmarks und ist auch in Zellen zu sehen, sobald diese das Gewebe verlassen, um zu migrieren.
Was passiert, wenn der Schalter fehlt
Mäuse, die vollständig ohne NR6A1 sind, sterben früh in der Entwicklung, sodass das Team Embryonen kurz vor diesem Zeitpunkt untersuchte. Sie beobachteten einen starken Mangel an Neuralleistenzellen, besonders hinter dem ersten Bogen, aus dem Teile von Kiefer und Hals entstehen — dort fehlten die migrierenden Neuralleistenzellen nahezu vollständig. Wichtige Genprogramme, die normalerweise die Neuralleistenidentität markieren und das Ablösen sowie die Bewegung der Zellen ermöglichen, waren deutlich reduziert. Gleichzeitig blieben Gene, die Zellen in einem stammzellähnlichen, hochproliferativen Zustand halten, weiterhin aktiv, und viele der wenigen entstandenen neuralleistenähnlichen Zellen starben bald darauf. Diese Befunde zeigen, dass ohne NR6A1 Neuralstammzellen nicht richtig in migratorische Neuralleistenzellen übergehen und nicht überleben können.
Die Pluripotenz ausschalten und Bewegung einschalten
Um zu verstehen, wie NR6A1 diese Kontrolle ausübt, kombinierten die Autorinnen und Autoren mehrere leistungsfähige molekulare Techniken, darunter Einzelzell-RNA-Sequenzierung, Kartierung der Chromatinzugänglichkeit und gezielte DNA–Protein-Bindungsassays sowohl in Maus- als auch in aus humanen Stammzellen abgeleiteten Neuralleistenzellen. Sie fanden heraus, dass NR6A1 physisch an spezifische DNA-Motive in der Nähe von Genen bindet, die zwei gegensätzliche Programme steuern: eines, das die Pluripotenz aufrechterhält (die Fähigkeit, viele Zelltypen zu werden), und ein anderes, das die Neuralleistenidentität sowie Zellbewegung antreibt. Wenn NR6A1 vorhanden ist, wird das Chromatin um Stammzellgene wie Oct4 und Nanog weniger zugänglich und diese Gene werden herunterreguliert, während Regionen in der Nähe von Neuralleisten- und epithelial-mesenchymalen Transitionsgenen offener und aktiver werden. Eine Überexpression von Oct4 während des kritischen Zeitfensters der Neuralleistenbildung ahmte den Verlust von NR6A1 nach und zeigte weiter, dass die Pluripotenz ausgeschaltet werden muss, damit Neuralleistenzellen entstehen können.
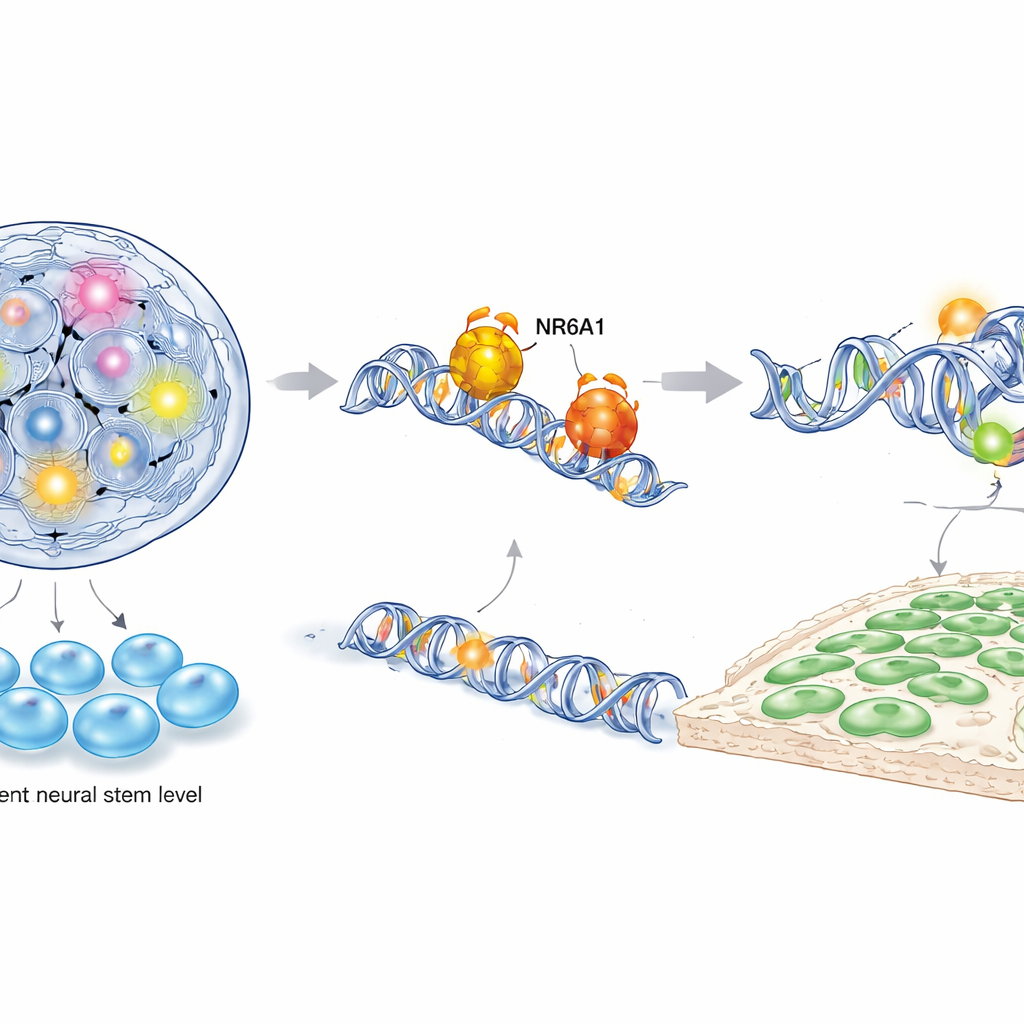
Den Zeitplan der frühen Entwicklung neu schreiben
Die Studie stellt auch den Zeitplan in Frage, wann Neuralleistenzellen bei Säugetieren zu spezifizieren beginnen. Mithilfe eines induzierbaren genetischen Systems, um NR6A1 zu verschiedenen Zeiten zu entfernen, zeigte das Team, dass dessen Deletion bis zur Mitte der Gastrulation — einer früheren Phase als traditionell angenommen — ausreichte, um die Aktivierung des Neuralleistengenprogramms zu blockieren. Im Gegensatz dazu führte eine spätere Deletion von NR6A1, etwa mit einer häufig verwendeten neuralleisten-spezifischen Treiberlinie, zu keinen offensichtlichen Defekten. Das bedeutet, dass entscheidende Weichenstellungen zur Neuralleistenbestimmung getroffen werden, bevor diese Standardwerkzeuge überhaupt aktiv werden, was erklärt, warum einige frühere Mausstudien frühe Anforderungen möglicherweise übersehen haben.
Warum das für Fehlbildungen und Krankheiten wichtig ist
Insgesamt zeigt die Arbeit NR6A1 als zentralen Koordinator, der Neuralstammzellen dabei hilft, zu Neuralleistenzellen „heranzuwachsen“, indem er gleichzeitig Pluripotenzprogramme ausschaltet und Programme für Migration und Überleben einschaltet. Diese doppelte Wirkung beginnt offenbar während der Mitte der Gastrulation, früher als zuvor bei Säugetieren angenommen, und bringt die Entwicklung der Maus näher an die anderer Wirbeltiere heran. Indem die Studie klärt, wann und wie dieser Schalter wirkt, liefert sie einen Rahmen, um frühere genetische Experimente neu zu interpretieren, bessere Werkzeuge für die Erforschung der Neuralleistenbiologie zu identifizieren und letztlich Neurocristopathien, die durch Fehlentscheidungen in dieser frühen Entwicklungsphase entstehen, besser zu verstehen und möglicherweise zu verhindern.
Zitation: Moore Zajic, E.L., Muñoz, W.A., Dennis, J.F. et al. NR6A1 is essential for neural crest cell specification, formation and survival. Nat Commun 17, 2140 (2026). https://doi.org/10.1038/s41467-026-68647-2
Schlüsselwörter: Neuralleistenzellen, NR6A1, embryonale Entwicklung, Pluripotenz-Schalter, Neurocristopathie