Clear Sky Science · de
Entwicklung des MmeFz2-ωRNA-Systems für effiziente Genomeditierung durch ein integriertes rechnerisch-experimentelles Framework
Kleinere Genscheren für große medizinische Probleme
Die Genbearbeitung hat bereits die Forschung an Krankheiten verändert, doch ihre Umsetzung in sichere, praktikable Therapien bleibt eine große Herausforderung. Ein wesentliches Hindernis sind die heute leistungsfähigsten DNA-„Scheren“, wie CRISPR-Cas9: sie sind physisch groß und schwer in die winzigen Transportvehikel zu verpacken, die bei Patientinnen und Patienten eingesetzt werden. Diese Studie stellt ein neues, kompaktes Geneditierwerkzeug vor, das aus einer wenig bekannten Enzymfamilie namens Fanzor2 aufgebaut ist, und zeigt, wie künstliche Intelligenz es schnell in einen vielversprechenden Kandidaten für künftige Gentherapien umgestalten kann.
Eine neue Klasse kompakter Geneditoren
Die meisten aktuellen Genomeditoren, etwa Cas9 und Cas12a, sind sperrige Proteine aus mehr als tausend Bausteinen. Diese Größe erschwert ihre Verpackung in adenoassoziierte Viren (AAVs), das führende Transportsystem für Gentherapien. Im Gegensatz dazu sind Fanzor2-Proteine deutlich kleiner und kommen natürlicherweise in Eukaryoten vor — dem Zweig des Lebens, zu dem auch Tiere und Menschen gehören. Die Autorinnen und Autoren konzentrierten sich auf ein Familienmitglied, MmeFz2, das eine kurze RNA namens ωRNA nutzt, um bestimmte DNA-Sequenzen zu finden und zu schneiden. Auf dem Papier schien MmeFz2 ideal für Therapien: kompakt und programmierbar. In der Praxis jedoch war seine Aktivität in menschlichen Zellen gering und lag bei weniger als einem Prozent der Zielstellen. Das Team machte sich daran, dieses schlecht funktionierende Enzym in ein brauchbares Werkzeug zu verwandeln.
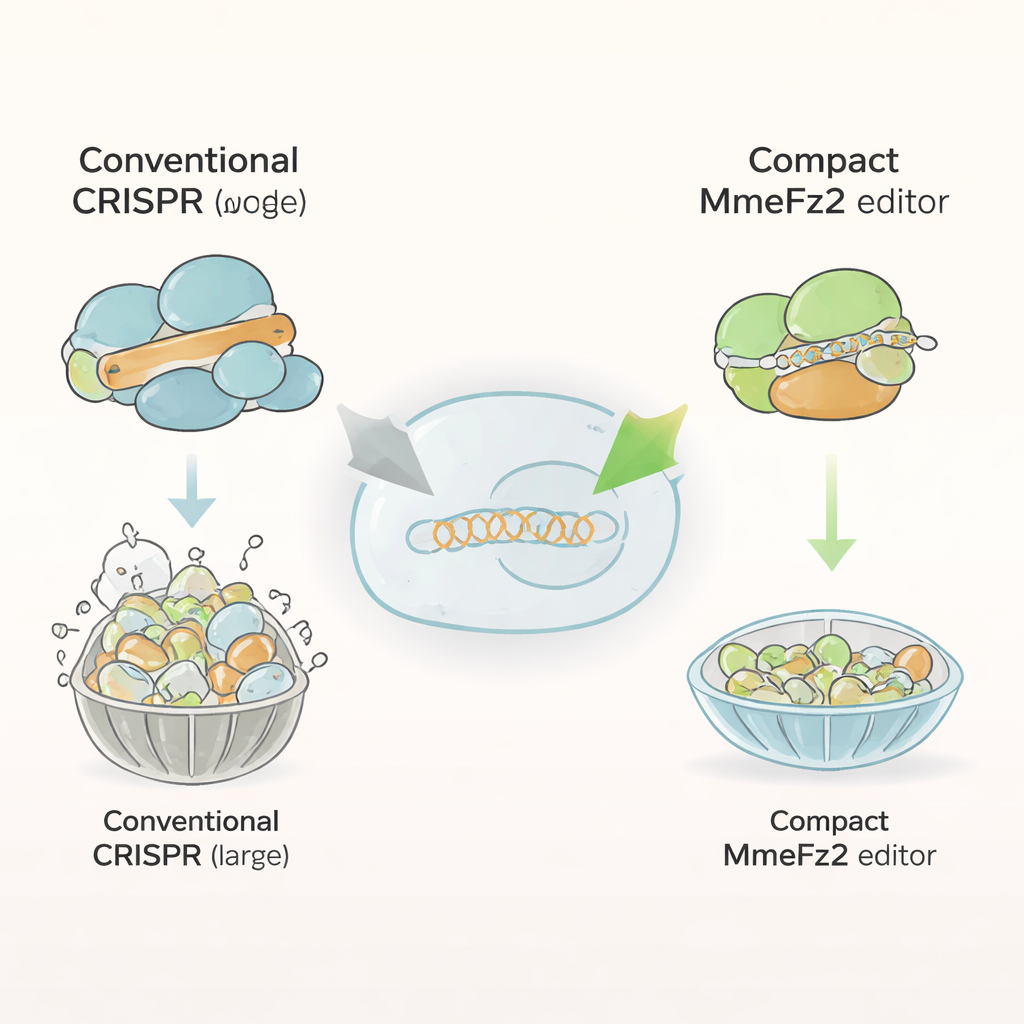
Mit KI die Leit-RNA neu gestalten
Das erste Ziel war die ωRNA, die das MmeFz2 anleitet, wo geschnitten werden soll. Mithilfe von AlphaFold3, einem hochmodernen Programm zur Vorhersage 3D-Strukturen von Protein–RNA–DNA-Komplexen, modellierten die Forschenden MmeFz2 gebunden an seine ωRNA und eine DNA-Zielsequenz. Diese virtuelle Struktur zeigte, dass Teile der ωRNA schlaff, schlecht gepaart und kaum mit dem Protein in Kontakt waren. Anhand dieser Informationen ersetzte das Team systematisch instabile Verbindungen in der RNA und entfernte Ketten von Uridin-Basen, die die Transkription stören können. Anschließend testeten sie dutzende Varianten in menschlichen Zellen. Durch Kombination der besten Änderungen und das Kürzen einer unnötigen Stammregion entstand eine verkleinerte ωRNA, die 30 % kürzer war und dennoch eine fast 20-fache Steigerung der Editierleistung über viele DNA-Stellen brachte.
Feinabstimmung des Proteins mit maschinellem Lernen
Als Nächstes verfeinerte das Team das Protein selbst. Wieder nutzten sie AlphaFold3, um kartografisch darzustellen, wo MmeFz2 RNA und DNA berührt, und entwarfen mehr als hundert Einzel-Aminosäure-Änderungen mit dem Ziel, diese Kontakte zu stärken oder die Flexibilität zu verbessern. Nach dem Screening dieser Varianten in Zellen fütterten sie die Leistungsdaten in EVOLVEpro ein, ein System für maschinelles Lernen, das auf Protein-Sprachmodellen basiert und aus Millionen natürlicher Sequenzen trainiert wurde. Dieses Werkzeug lernte, welche Merkmale tendenziell die Aktivität erhöhen, und schlug neue Mutationskombinationen vor, die voraussichtlich noch besser funktionieren. Durch einige Runden dieser rechnerisch-experimentellen Schleife gelangten die Wissenschaftlerinnen und Wissenschaftler zu zwei optimierten Enzymvarianten, die, gepaart mit der verbesserten ωRNA, die Editieraktivität gegenüber dem Ausgangssystem mehr als 60-fach steigerten.
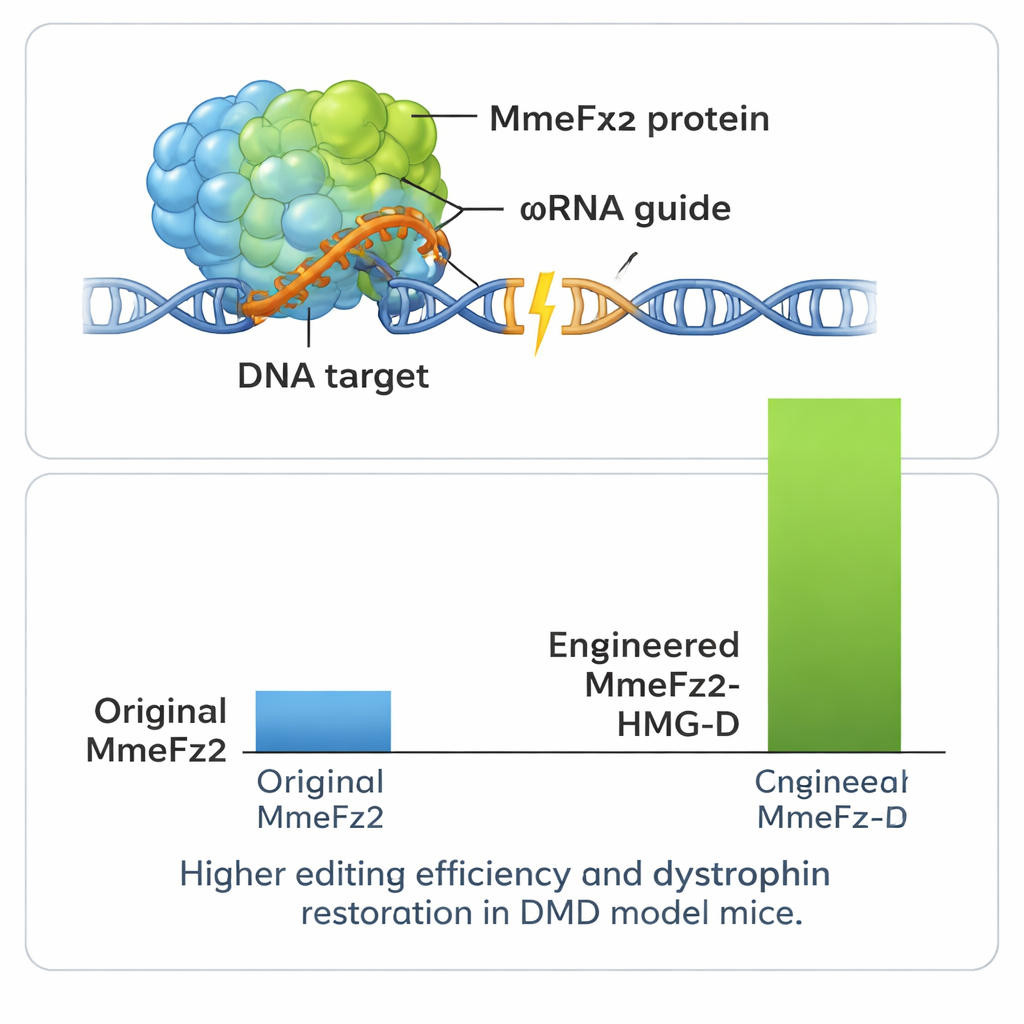
Mehr Leistung und Tests in einem Krankheitsmodell
Um noch mehr Leistung aus dem System herauszuholen, fügten die Autorinnen und Autoren MmeFz2 kleine DNA-Bindedomänen hinzu, die Proteinen helfen, sich an genetisches Material zu heften. Eine davon, HMG-D genannt, erwies sich als besonders effektiv, wenn sie an das Ende des modifizierten Enzyms angefügt wurde und an einigen Stellen Editierwerte über 80 % erzeugte. Wichtig war, dass Tests an vorhergesagten Off-Target-Stellen im Genom zeigten, dass diese zusätzliche Kraft nicht mit einem großen Verlust an Präzision einherging. Da der gesamte Geneditor — Protein und Leit-RNA — so kompakt ist, passt er bequem in einen einzelnen AAV-Vektor, was bei den meisten CRISPR-Systemen nicht möglich ist. Das Team nutzte diesen Vorteil in einem Mausmodell der Duchenne-Muskeldystrophie, einer tödlichen Muskelschwunderkrankung, die durch Fehler im Dystrophin-Gen verursacht wird. Eine einmalige Injektion des AAV-vermittelten Editors in die Beinmuskulatur führte zu nachweisbaren Korrekturen in der Gen-RNA und stellte in einem beträchtlichen Anteil der Muskelfasern Dystrophin-Protein wieder her.
Was das für künftige Gentherapien bedeutet
Für Nicht-Fachleute lautet die Kernbotschaft: Die Autorinnen und Autoren haben ein schwaches, kaum bekanntes Genschneideenzym in einen kompakten, leistungsfähigen Editor verwandelt, der in einem einzigen viralen Paket ausgeliefert werden kann und in einem realistischen Tiermodell eine schwere Erbkrankheit repariert. Ebenso wichtig ist, wie sie das erreichten: Durch enge Verknüpfung von KI-basierter Strukturvorhersage und maschinellem Lernen mit gezielten Labortests verbesserten sie sowohl das Protein als auch seine Leit-RNA deutlich effizienter als mit traditionellen Trial-and-Error-Methoden. Diese integrierte Strategie könnte die Entwicklung zahlreicher nächster Generationen von Geneditoren beschleunigen und präzisere sowie sicherere Gentherapien für Patientinnen und Patienten mit Muskeldystrophie und anderen erblichen Erkrankungen näherbringen.
Zitation: Li, S., Xu, K., Li, G. et al. Engineering the MmeFz2-ωRNA system for efficient genome editing through an integrated computational-experimental framework. Nat Commun 17, 1867 (2026). https://doi.org/10.1038/s41467-026-68644-5
Schlüsselwörter: Genbearbeitung, CRISPR-Alternativen, Duchenne-Muskeldystrophie, virale Gentherapie, Künstliche Intelligenz in der Biologie