Clear Sky Science · de
Getarnte Nanoroboter zielen auf und regulieren den subzellulären Organelle‑Dialog von Makrophagen, um die neuronale Regeneration zu fördern
Warum winzige „getarnte“ Helfer bei Rückenmarksverletzungen wichtig sind
Eine Rückenmarksverletzung führt häufig zu lebenslanger Lähmung, weil geschädigtes Nervengewebe extrem schwer zu reparieren ist. Ein zentraler Grund ist, dass die Verletzungsstelle zu einer feindlichen Zone wird, gefüllt mit Entzündung und zellulärem Stress, die die Heilung blockieren. Diese Studie beschreibt eine neue Art getarnter Nanoroboter, die durch den Blutkreislauf reisen, die Abwehr des Körpers umgehen und Immunzellen an der Verletzungsstelle so umprogrammieren, dass sie vom Angriffs- in den Reparaturmodus wechseln und so das Nachwachsen von Nerven bei Tieren mit Rückenmarksverletzungen unterstützen.
Das Problem: eine Entzündung, die nicht abschaltet
Nach einer Rückenmarksverletzung entsteht die erste Schadenswelle durch das physische Trauma selbst. Eine zweite, langsamere Welle wird jedoch durch Entzündungen, toxische Moleküle wie reaktive Sauerstoffspezies und weitreichenden Zelltod angetrieben. Immunzellen, bekannt als Makrophagen, strömen herbei, um Trümmer zu beseitigen. Zu Beginn nehmen sie einen aggressiven „M1“-Zustand an, der Pathogene und beschädigte Zellen abtötet, aber auch starke entzündliche Signale freisetzt. Damit echte Heilung beginnen kann, müssen dieselben Zellen später in einen beruhigenden „M2“-Zustand wechseln, der Gewebereparatur, Gefäßbildung und Nervenregeneration unterstützt. Leider kann der intensive Stress im verletzten Gewebe Makrophagen im schädlichen M1‑Zustand festhalten und einen Kreislauf chronischer Entzündung erzeugen, der eine funktionelle Erholung verhindert.
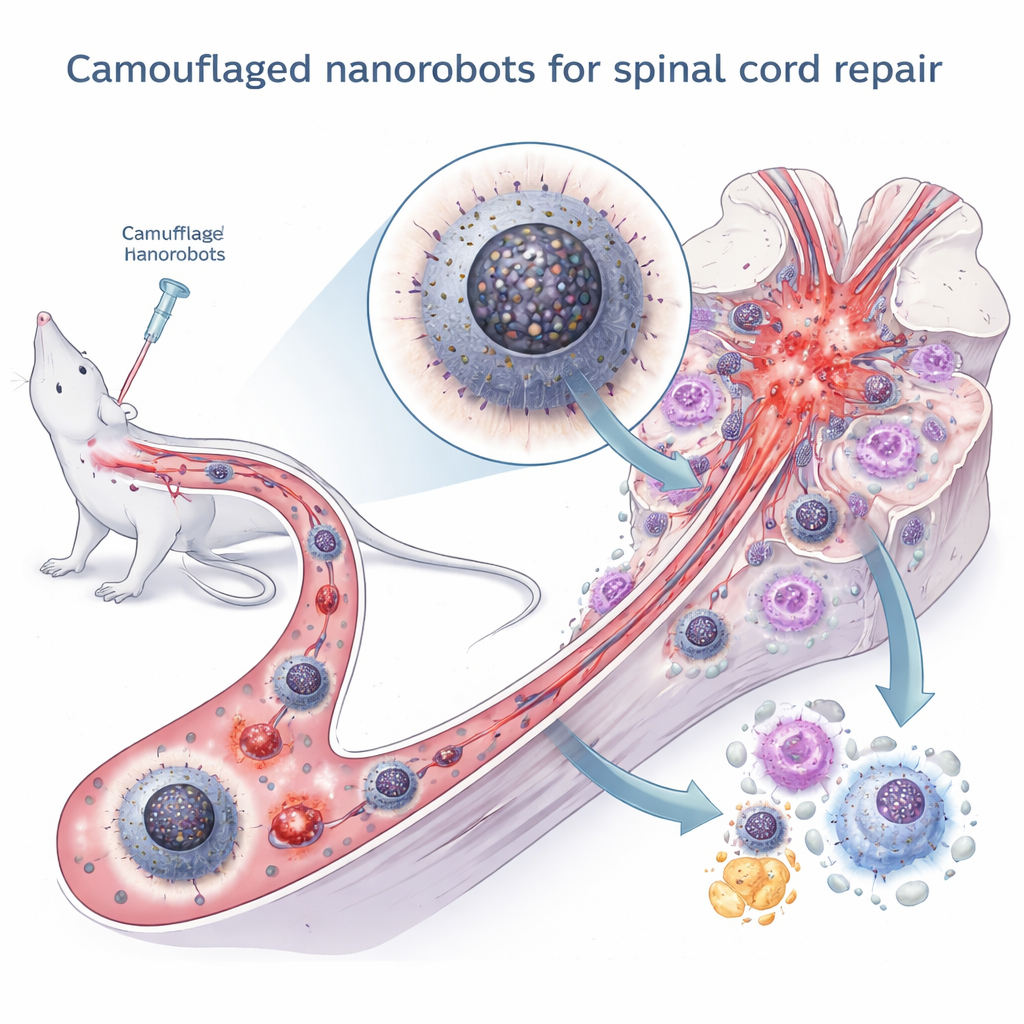
Verborgene Kommunikation zwischen Zellteilen
Die Autoren konzentrierten sich auf ein subtileres, aber entscheidendes internes „Gespräch“ in Makrophagen: die Kommunikation zwischen zwei Schlüsselkompartimenten, dem endoplasmatischen Retikulum (das beim Falten von Proteinen hilft und Calcium speichert) und den Mitochondrien (den Kraftwerken der Zelle). Unter normalen Bedingungen teilen diese Strukturen geringe Mengen an Calciumionen über spezialisierte Kontaktstellen, was hilft, die Energieproduktion an den Bedarf der Zelle anzupassen. Nach einer Verletzung verursachen jedoch überschüssige reaktive Sauerstoffspezies Proteinfehlfaltung und Stress im endoplasmatischen Retikulum. Dieser Stress treibt wiederum übermäßigen Calciumtransfer in die Mitochondrien, was zu einem Energiesturz, verstärkter Bildung toxischer Moleküle und dem Auslaufen mitochondrialer DNA in das Zellplasma führt. Diese entwichene DNA löst einen starken Alarmweg namens cGAS–STING–NFκB aus, der Makrophagen weiter in den entzündlichen M1‑Zustand drängt.
Entwurf eines getarnten Nanoroboters
Um diesen Teufelskreis zu durchbrechen, baute das Team einen mehrschichtigen Nanoroboter namens BP@D/N. Im Kern befinden sich Black‑Phosphorus‑Quantenpunkte, winzige Partikel mit starker antioxidativer und antiinflammatorischer Aktivität, aber schlechter Stabilität im Körper. Diese Punkte sind in eine hohle Hülle aus Polydopamin gepackt, einem biokompatiblen Material, das sie vor zu frühem Abbau schützt und selbst antioxidative Eigenschaften beiträgt. Schließlich ist das gesamte Partikel mit einer Membran bedeckt, die von aktivierten Neutrophilen gewonnen wurde — einer Art weißer Blutkörperchen, die natürlicherweise zu Entzündungsherden gezogen werden. Diese „Tarnung“ ermöglicht es dem Nanoroboter, der Immunabwehr zu entgehen, Entzündungssignalen zum verletzten Rückenmark zu folgen und an Makrophagen zu haften, um eine effiziente Aufnahme zu gewährleisten.
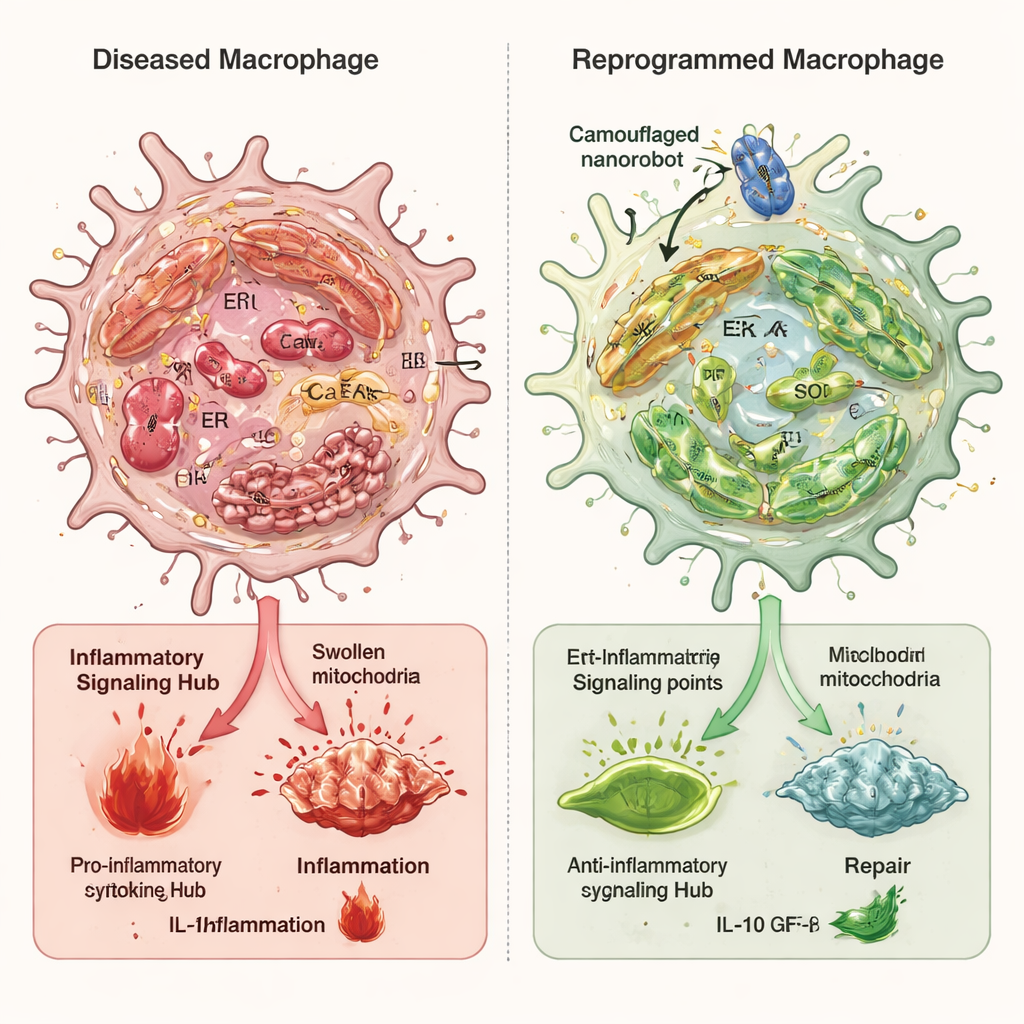
Umprogrammierung gestresster Immunzellen
In Zellstudien zeigten Makrophagen, die entzündlichen Auslösern ausgesetzt waren, hohe Werte an endoplasmatischem Retikulum‑Stress, geschwollene und beschädigte Mitochondrien, Calciumüberladung und starke Aktivierung des cGAS–STING–NFκB‑Alarmwegs. Nach Behandlung mit den getarnten Nanorobotern sank der oxidative Stress insgesamt deutlich, die internen Membrankontakte zwischen endoplasmatischem Retikulum und Mitochondrien wurden weniger übervernetzt, und mitochondrialer Calciumspiegel kehrte weitgehend zur Normalität zurück. Dadurch wurde das Austreten mitochondrialer DNA ins Zellplasma verhindert und die entzündliche Signalcascade heruntergeregelt. Ein wichtiger Akteur in diesem Prozess war ein Enzym namens Ero1α, das das oxidative Milieu und die Calciumfreisetzung aus dem endoplasmatischen Retikulum mitsteuert. Die Nanoroboter reduzierten die Ero1α‑Aktivität; als die Forschenden Ero1α künstlich erhöhten, hob das weitgehend die Vorteile der Nanoroboter auf und bestätigte so seine zentrale Rolle.
Von der Entzündungsberuhigung zur Nervenregeneration
Diese internen Veränderungen veranlassten die Makrophagen, vom zerstörerischen M1‑Zustand in den heilenden M2‑Zustand zu wechseln. In Zellkulturen sezernierten die in Richtung M2 verschobenen Zellen weniger entzündliche Moleküle wie TNF‑α und IL‑6 und mehr Wachstumsfaktoren, die Nervenzellen und Stützgewebe zum Wachsen und zur Achsenausdehnung anregen. In Rattenmodellen mit Rückenmarksverletzung führte wiederholte Injektion der Nanoroboter zu weniger schädlichen Immunreaktionen an der Läsion, weniger Narbenbildung, geringerer Kavitätenbildung und mehr regenerierenden Nervenfasern. Tiere, die die getarnten Nanoroboter erhielten, zeigten eine bessere Funktion der Hinterbeine, stärkere Muskelantworten und eine verbesserte Blasenstruktur im Vergleich zu unbehandelten oder weniger zielgerichteten Nanopartikel‑Behandlungen.
Was das für zukünftige Patientinnen und Patienten bedeuten könnte
Diese Arbeit zeigt, dass eine präzise Steuerung des internen Stresses und der Kommunikation zwischen Zellkompartimenten Immunzellen von schädlich zu hilfreich für verletzte Nerven umschalten kann. Durch das Verpacken starker, aber fragiler antioxidativer Partikel in einen getarnten, zielgerichteten Nanoroboter stellten die Forschenden ein gesünderes Gleichgewicht zwischen Entzündung und Reparatur im verletzten Rückenmark von Ratten wieder her. Obwohl noch viel Arbeit nötig ist, bevor dieser Ansatz beim Menschen getestet werden kann, bietet er einen vielversprechenden Entwurf: Statt Entzündung breit zu unterdrücken, könnten künftige Therapien gezielt zelluläre Mechanismen in Makrophagen steuern, um ein günstigeres Umfeld für die neuronale Regeneration nach Rückenmarksverletzung zu schaffen.
Zitation: Guo, Q., Wang, W., Jiang, X. et al. Camouflaged nanorobots target and regulate macrophage subcellular organelle crosstalk patterns to promote neural regeneration. Nat Commun 17, 1952 (2026). https://doi.org/10.1038/s41467-026-68636-5
Schlüsselwörter: Rückenmarksverletzung, Nanoroboter, Makrophagen, neuronale Regeneration, Nanotherapie