Clear Sky Science · de
Metabolische Charakterisierung von Tumor‑Immun‑Interaktionen durch multiplexe Immunfluoreszenz zeigt räumliche Mechanismen der Immuntherapieantwort beim nicht‑kleinzelligen Lungenkarzinom (NSCLC)
Warum diese Forschung wichtig ist
Die Immuntherapie hat die Behandlung für manche Menschen mit fortgeschrittenem Lungenkrebs revolutioniert, dennoch schreitet bei den meisten Patientinnen und Patienten der Tumor trotz dieser wirkungsvollen Medikamente weiter voran. Diese Studie stellt eine einfache, aber entscheidende Frage: Können wir das Tumorgewebe selbst — also die Lage verschiedener Zellen und ihren Energiestoffwechsel — genauer betrachten, um vorherzusagen, wer tatsächlich von einer Immuntherapie profitiert? Indem winzige Biopsieproben in detaillierte Zellkarten verwandelt werden, zielen die Forschenden darauf ab, die Versorgung von Lungenkrebspatienten in Richtung echter Präzisionsmedizin zu verschieben.
In Lungen Tumoren hineinschauen wie auf eine Stadtkarte
Das Team untersuchte Gewebe von 55 Personen mit fortgeschrittenem nicht‑kleinzelligem Lungenkarzinom (NSCLC), die mit Checkpoint‑Inhibitoren behandelt wurden, einer wichtigen Klasse von Immuntherapeutika. Vor der Behandlung wurden die Tumorproben mit einem 44‑Marker‑Panel mittels multiplexer Immunfluoreszenz angefärbt, sodass viele Proteine gleichzeitig sichtbar wurden. Ein Deep‑Learning‑System identifizierte anschließend Schlüsselfzelltypen — etwa Tumorzellen, T‑Zellen, B‑Zellen, Makrophagen und Fibroblasten — und klassifizierte deren Funktionszustand (z. B. aktiviert, teilend oder erschöpft) sowie ihr metabolisches Profil, also wie sie Energie erzeugen und nutzen. Anstatt nur Zellen zu zählen, kartierten die Forschenden auch die räumliche Beziehung der Zellen zueinander und schufen innerhalb jeder Biopsie nachbarschaftsähnliche Regionen.
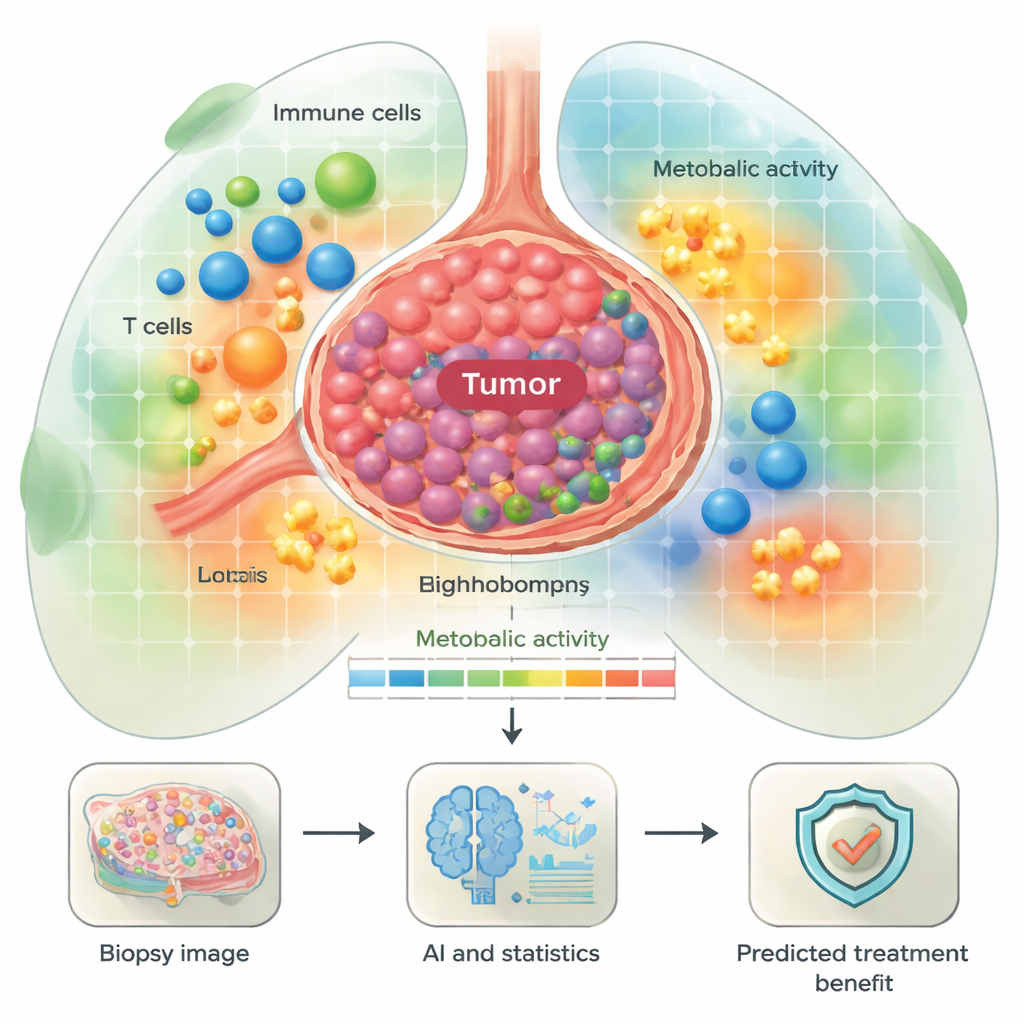
Energiehungrige Tumoren und ihr immunologisches Umfeld
Ein Schwerpunkt war der Stoffwechsel — die Art und Weise, wie Zellen Treibstoff erzeugen, um zu wachsen oder Krankheit zu bekämpfen. Die Forschenden definierten „metabolische Nachbarschaften“ mit unterschiedlichen Leveln und Typen von Energieverbrauch, von niedriger Aktivität bis zu hochaktiven Zonen reich an oxidativer Phosphorylierung und Glykolyse. Sie fanden, dass sowohl Tumorzellen als auch bestimmte Immunzellen wie Makrophagen häufig starke energieproduzierende Wege zeigten. Einige dieser Muster korrelierten mit dem klinischen Verlauf. So gehörten Tumoren mit hoher Aktivität in Wegen zur Aminosäureverwertung und dem TCA‑Zyklus eher zu Patientinnen und Patienten, die früh nach der Immuntherapie rezidivierten. Dagegen waren bestimmte Plasmazellen (antikorpenbildende B‑Zellen) mit aktiven Energiestoffwechselwegen innerhalb des Tumors häufiger bei Patientinnen und Patienten mit besserem Verlauf, was darauf hindeutet, dass nicht alle energieintensiven Zellen schädlich sind — manche könnten eine effektive antitumorale Immunantwort unterstützen.
Gute und schlechte Immunakteure in der Tumorlandschaft
Über die bloße Häufigkeit hinaus spielten Typ und Verhalten der Immunzellen eine Rolle. Makrophagen, die das zytotoxische Molekül Granzyme B trugen, waren stark mit schlechterem progressionsfreiem Überleben assoziiert, insbesondere wenn sie in metabolisch inaktiven oder schwach aktiven Nachbarschaften vorkamen. Diese Regionen könnten nährstoffarme oder ruhende Bereiche darstellen, in denen die Immunabwehr abgeschwächt ist. Demgegenüber schienen bestimmte Anordnungen von regulatorischen T‑Zellen (Tregs) und Fibroblasten an der Grenze zwischen Tumor und umgebendem Gewebe mit besseren Ergebnissen verbunden zu sein — möglicherweise weil unterdrückende Zellen am Rand gehalten werden, statt tief in den Tumor einzudringen. Verhältnisse verschiedener Immunzellen, wie Granulozyten zu CD8‑T‑Zellen, korrelierten ebenfalls mit dem Therapieansprechen und unterstreichen, dass Gleichgewicht und Positionierung des Immunsystems wichtiger sind als bloße Zellzahlen.
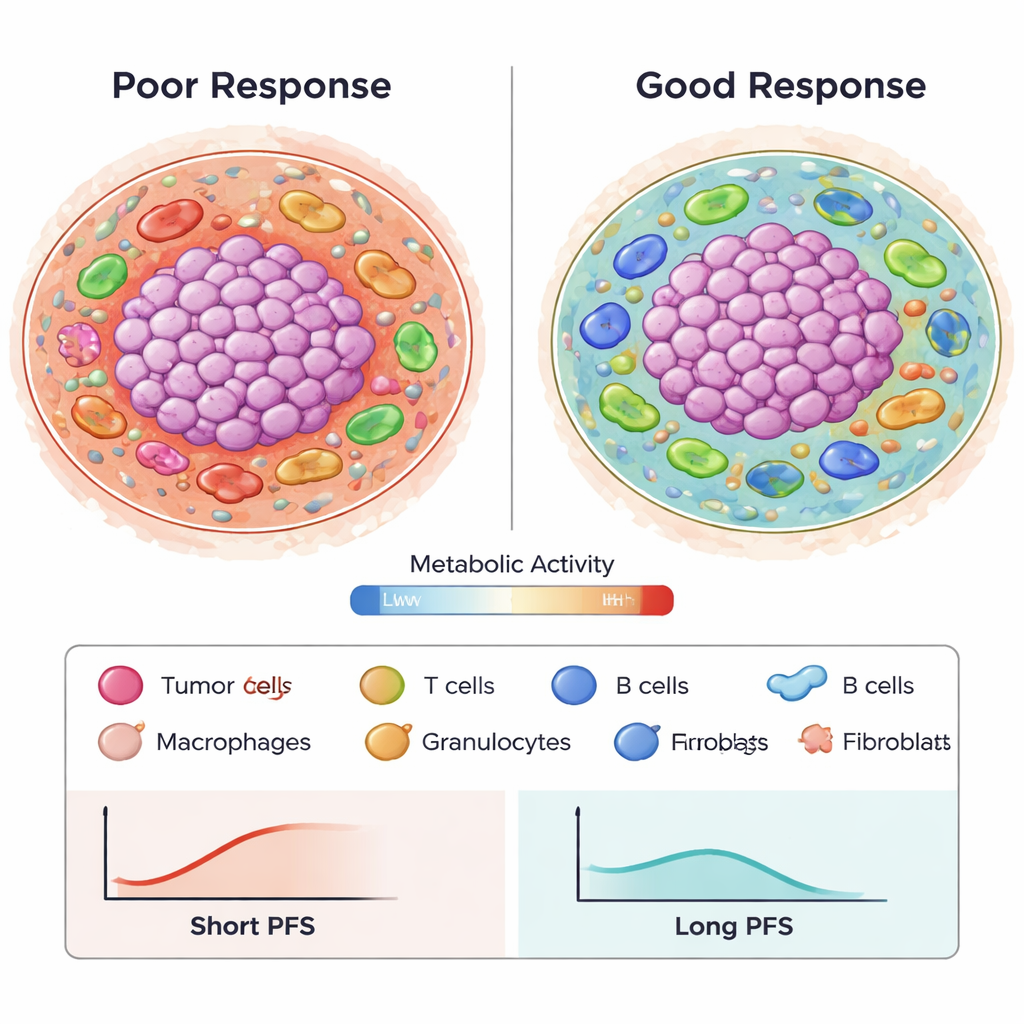
Von komplexen Bildern zu vorhersagbaren Mustern
Um über eine Million konstruierter räumlicher Merkmale zu verstehen — die Zelltypen, Abstände und metabolischen Zustände beschreiben — nutzten die Autorinnen und Autoren eine fortschrittliche Merkmal‑Selektionsmethode (Stabl) und Überlebensmodelle. Sie identifizierten 87 Schlüsselfeatures, viele davon spiegelten wider, wie metabolisch aktive Tumorzellen mit Makrophagen und T‑Zellen interagieren oder wie bestimmte Immunzelltypen in der Nähe von Blutgefäßen und Fibroblasten klustern. Mithilfe dieser Merkmale in Cox‑Regressionsmodellen bauten sie einen Prädiktor, der das progressionsfreie Überleben über 24 Monate mit einer Genauigkeit (AUC) von etwa 0,8 schätzte und damit klassische Einzelmarker wie PD‑L1‑Färbung oder Tumormutationslast in früheren Studien übertraf. Wichtig ist, dass mehrere Merkmale in zwei unabhängigen Patientenkohorten reproduzierbar waren, was darauf hindeutet, dass die Muster nicht nur zufälliges Rauschen sind.
Was das für Patientinnen und Patienten bedeutet
Für Laien lautet die Kernbotschaft: Wo Zellen in einem LungenTumor liegen und wie sie sich energetisch versorgen, kann erklären helfen, warum einige Patienten gut auf Immuntherapie ansprechen und andere nicht. Diese Studie zeigt, dass reiche räumliche und metabolische Informationen aus einer Routinetbiopsie, kombiniert mit künstlicher Intelligenz und statistischer Modellierung, Signaturen aufdecken können, die einen wahrscheinlichen Nutzen oder eine Resistenz vorhersagen. Obwohl die Ergebnisse in größeren Gruppen und an Ganzgewebeschnitten noch validiert werden müssen, skizziert die Arbeit einen Weg zu künftigen Tests, die Ärztinnen und Ärzten vor Therapiebeginn sagen könnten, welche Patientinnen und Patienten mit hoher Wahrscheinlichkeit eine dauerhafte Kontrolle durch Immuntherapie erreichen und welche alternative oder kombinierte Strategien benötigen.
Zitation: Monkman, J., Kilgallon, A., Lawler, C. et al. Metabolic characterization of tumor-immune interactions by multiplexed immunofluorescence reveals spatial mechanisms of immunotherapy response in non-small cell lung carcinoma (NSCLC). Nat Commun 17, 837 (2026). https://doi.org/10.1038/s41467-026-68633-8
Schlüsselwörter: Resistenz gegen Immuntherapie, nicht‑kleinzelliges Lungenkarzinom, Tumormikroumgebung, räumliche Biologie, Krebsstoffwechsel