Clear Sky Science · de
Hydrogel mit Zell-Zell-Haftsignalen fördert die neuronale Regeneration
Dem verletzten Gehirn beim Selbstheilen helfen
Traumatische Hirnverletzungen können langfristige Probleme mit Bewegung, Gedächtnis und Denken hinterlassen, weil beschädigte Nervenzellen im Gehirn selten wieder vollständig nachwachsen oder sich richtig wieder verbinden. Ärzte können Blutgerinnsel entfernen oder den Schädel stabilisieren, doch sie haben nur wenige Werkzeuge, um die feine Verschaltung des Gehirns wieder aufzubauen. Diese Studie beschreibt ein weiches, wasserreiches Material – ein Hydrogel –, das so konstruiert ist, dass es nachahmt, wie sich Gehirnzellen natürlicherweise aneinander anheften. Indem es diese winzigen „Händeschütteln“ zwischen Zellen nachbildet, hilft das Material beschädigten Nervenfasern beim Nachwachsen, beim Wiederaufbau von Verbindungen und bei der Wiederherstellung von Funktionen in verletzten Rattengehirnen.
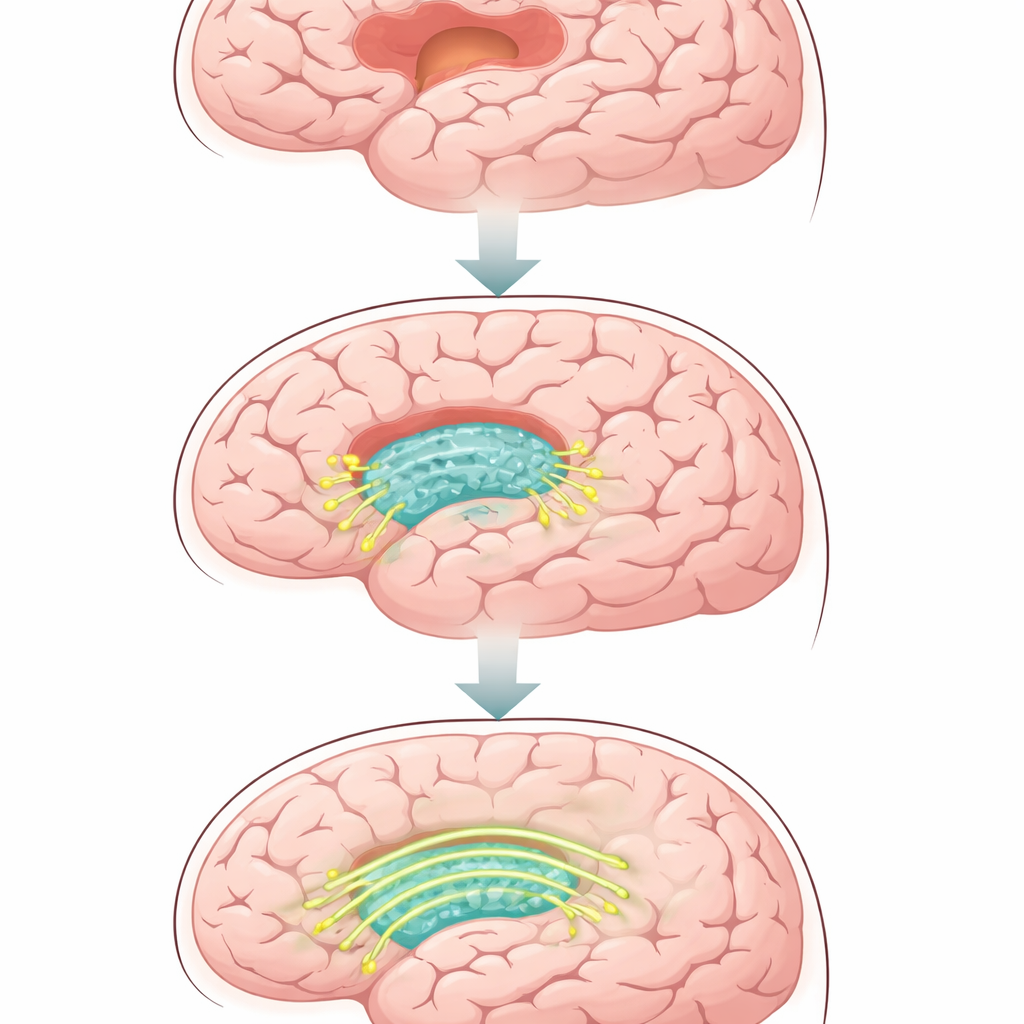
Ein weiches Gerüst für beschädigtes Hirngewebe
Die Forscher begannen mit einem seidenbasierten Hydrogel, das sich ähnlich wie Hirngewebe anfühlt – sehr weich und flexibel, mit vielen winzigen Poren, in denen Zellen sich bewegen und ihre Fortsätze ausstrecken können. Anschließend überzogen sie dieses Gel mit einer dünnen, flüssigen Schicht aus Fettsubstanzen, die sich wie eine Zellmembran verhält. Diese Schicht kann spezielle Proteine halten und ihnen gleichzeitig erlauben, seitlich zu diffundieren, so wie es auf echten Zellen geschieht. Das Ergebnis ist ein dreidimensionales, injizierbares Material, das unregelmäßige Hirnwunden ausfüllen und bewegliche Signale an nahegelegene Nervenzellen abgeben kann, statt nur passiv eine Füllung zu sein.
Sich die zelluläre Handshake-Mechanik der Natur zunutze machen
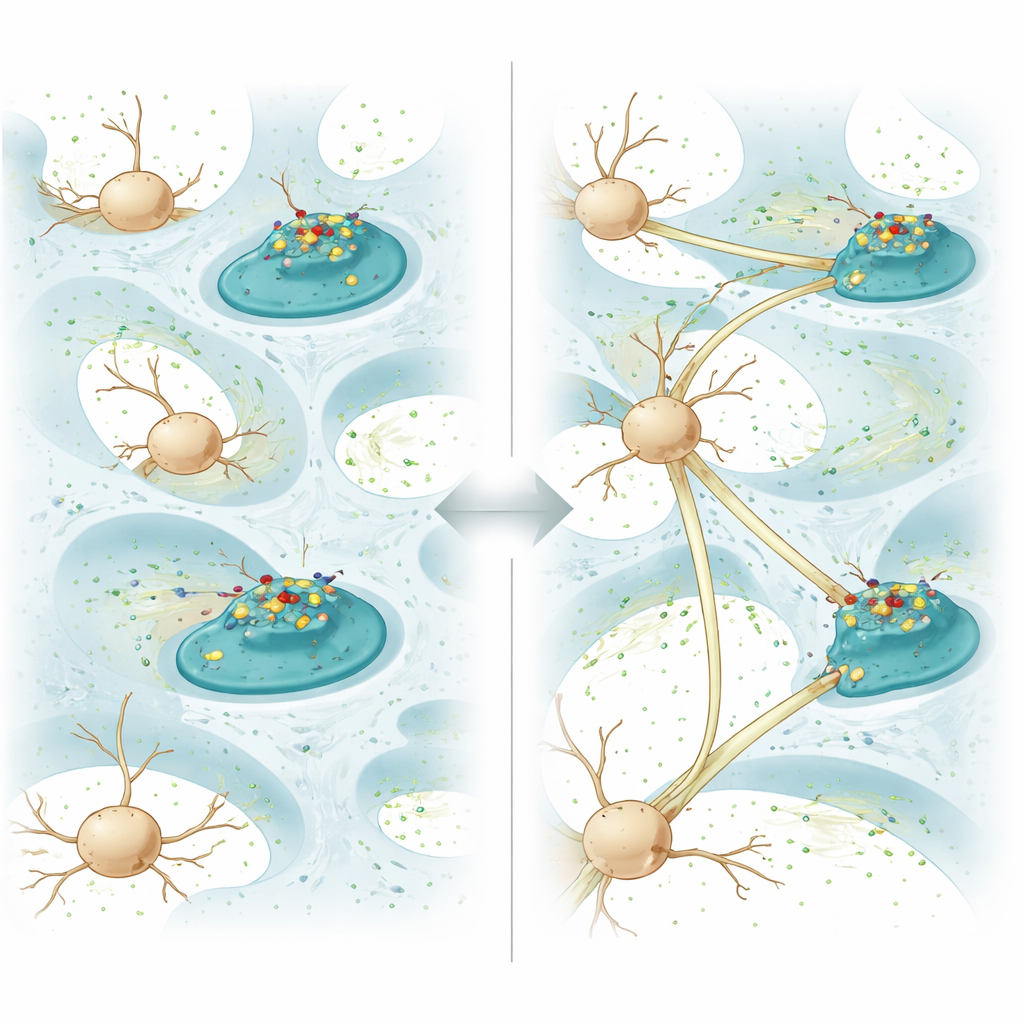
Um das Hydrogel zu einem aktiven Partner der Heilung zu machen, befestigte das Team ein Protein namens N‑Cadherin an der fetthaltigen Beschichtung. Im Gehirn sitzt N‑Cadherin auf der Oberfläche von Neuronen und hilft benachbarten Zellen, sich zu erkennen und aneinander zu haften, stabile Kontakte zu bilden und schließlich Synapsen, an denen Signale von Zelle zu Zelle übertragen werden. In diesem Gel ist N‑Cadherin nicht fixiert; es kann frei über die Beschichtung diffundieren. Wenn Neuronen gegen das Gel wachsen, reichert sich das Protein an den Stellen an, an denen ihre Membranen das Material berühren, verändert die kleinen Ausstülpungen der Zellen und löst die Bildung von Zell‑zu‑Zell‑Verbindungen aus. In Zellkulturen streckten Neuronen auf diesem „diffusiven N‑Cadherin“-Gel längere Fortsätze aus, bildeten mehr Verbindungen und zeigten stärkere elektrische Kommunikation als auf ähnlichen Gelen, bei denen das Protein fixiert und unbeweglich war.
Die Reparaturprogramme des Gehirns aktivieren
Über den bloßen Kontakt hinaus veranlasst das Hydrogel Neuronen auch dazu, interne Reparaturwege einzuschalten. Gen‑ und Proteinanalysen zeigten, dass Zellen auf dem diffusiven N‑Cadherin‑Gel Signale reduzierten, die den programmierten Zelltod antreiben, und Wege verstärkten, die Wachstum und Überleben fördern. Besonders stieg das Niveau eines Proteins namens Thrombospondin‑1 an, das von Stütz‑/Gliazellen im Gehirn freigesetzt wird und sowohl die Synapsenbildung begünstigen als auch wachstumsfördernde Signalwege aktivieren kann. Zwei dieser Wege, oft als TGF‑β/Smad‑ und AKT/mTOR‑Signalwege bezeichnet, wurden stark aktiviert, was zu gesünderen Mitochondrien, mehr Energieproduktion und verbessertem Nachwachsen durchtrennter Nervenfasern in einem mikrofluidischen Modell führte, das abgeschnittene Axone nachahmt.
Vom Petrischälchen ins lebende Gehirn
Um zu prüfen, ob diese Effekte im lebenden Gehirn relevant sind, injizierte das Team das Hydrogel in Ratten mit einer kontrollierten Form traumatischer Hirnverletzung. Über mehrere Wochen schnitten die mit dem diffusiven N‑Cadherin‑Gel behandelten Tiere bei Bewegungstests und in einem Wasserlabyrinth‑Test, der Lernen und Gedächtnis misst, besser ab als Tiere, die plaines Gel, nur Lipid‑Gel oder nur Kochsalzlösung erhielten. Hirnscans und Gewebeschnitte zeigten kleinere Hohlräume an der Verletzungsstelle sowie mehr neu gebildete Nervenfasern und Synapsen im reparierten Bereich. Gleichzeitig zeigten die behandelten Gehirne weniger überaktive Immunzellen und weniger dichte Narbenbildung, wodurch ein einladenderes Umfeld für das Nachwachsen entstand. Marker für Zelltod waren reduziert, während Proteine, die mit gesunder neuronaler Kommunikation verknüpft sind, erhöht waren.
Warum das für künftige Hirnreparaturen wichtig ist
Vereinfacht gesagt zeigt diese Arbeit, dass das Bereitstellen der richtigen „sozialen Signale“ für verletztes Hirngewebe einen großen Unterschied für dessen Heilung machen kann. Statt Gewebe nur mechanisch zu stützen, rekonstruiert das Hydrogel die beweglichen Kontaktsignale, die echte Gehirnzellen verwenden, um einander zu finden und festzuhalten. Bei Ratten füllte diese Strategie nicht nur Löcher im Gehirn, sondern half auch, funktionsfähige neuronale Schaltkreise wieder aufzubauen und verbesserte das Verhalten nach der Verletzung. Obwohl vor einer Anwendung beim Menschen noch viele Tests nötig sind, könnte der Ansatz – frei bewegliche Zelladhäsionsproteine in weiche, injizierbare Gele einzubetten – über N‑Cadherin und über das Gehirn hinaus erweitert werden und eine allgemeine Rezeptur für Materialien bieten, die die Geweberegeneration aktiv steuern.
Zitation: Tang, X., Zhang, S., Liu, M. et al. Hydrogel with cell-cell adhesion cues enhances neural regeneration. Nat Commun 17, 2178 (2026). https://doi.org/10.1038/s41467-026-68632-9
Schlüsselwörter: neuronale Regeneration, traumatische Hirnverletzung, Hydrogel-Gerüst, Zelladhäsion, N-Cadherin