Clear Sky Science · de
Modulation der Nudt21-Spiegel zeigt dosisabhängige Rollen der alternativen Polyadenylierung bei der Geweberegeneration
Wie Zellen unser Gewebe jung halten
Unser Körper repariert sich ständig selbst. In Haut, Darm, Knochenmark und Muskeln ruhende Stammzellen ersetzen im Verborgenen abgenutzte Zellen, damit Gewebe gesund bleiben. Diese Arbeit untersucht eine unsichtbare Kontrollebene in diesen Stammzellen — wie sie ihre RNA-Botschaften abschließen — und zeigt, dass kleine Veränderungen in diesem Prozess darüber entscheiden können, ob Gewebe sich problemlos regenerieren, ins Stocken geraten oder versagen. 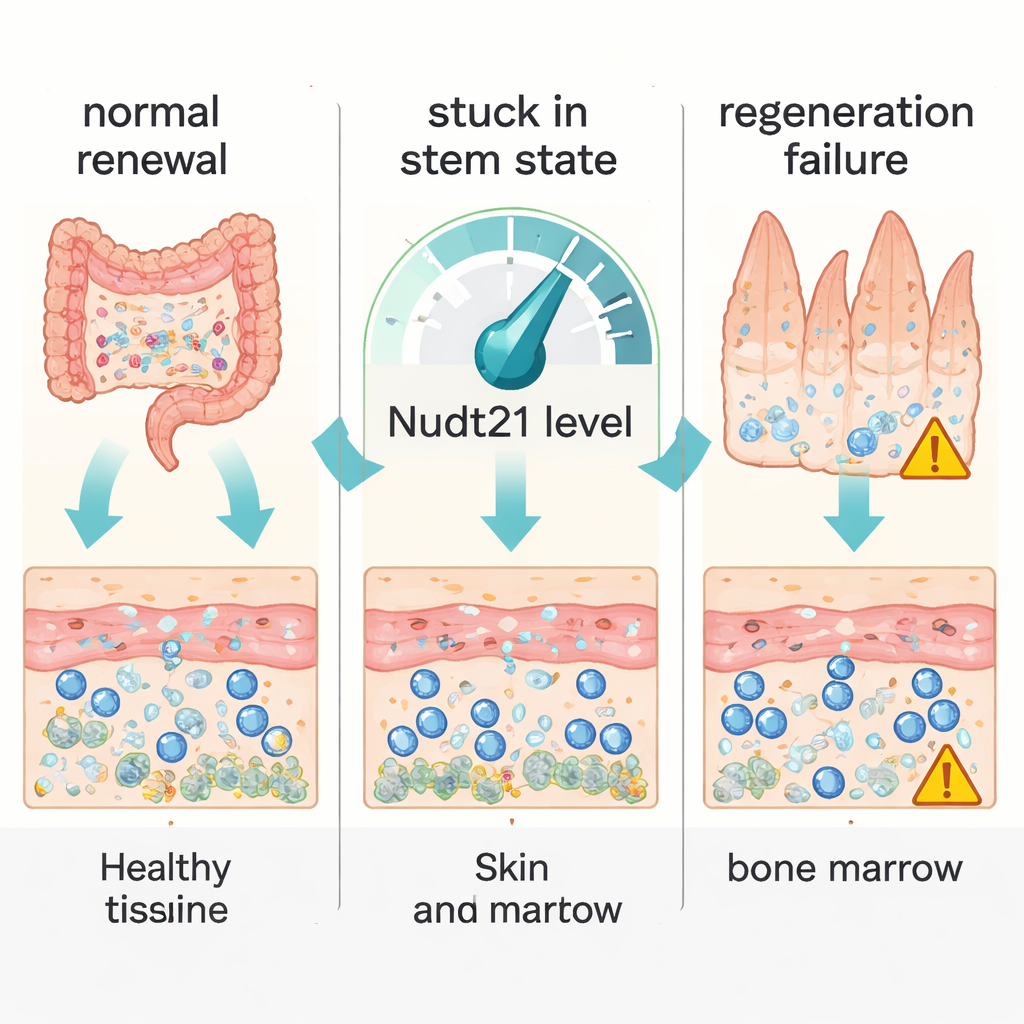
Den Schwanz genetischer Botschaften abschneiden
Jedes Gen, das in einer Zelle aktiviert wird, wird zuerst in eine RNA-Botschaft kopiert. Bevor diese Botschaft zur Proteinproduktion genutzt werden kann, erhält sie an ihrem Ende eine chemische „Schwanz“-Anhängung, ein Vorgang, der als Polyadenylierung bezeichnet wird. Viele Gene haben mehr als eine mögliche Schnittstelle, sodass dieselbe Botschaft mit einer längeren oder kürzeren Schwanzregion enden kann. Diese Schwanzregionen, bekannt als 3'UTRs, codieren nicht für Protein, fungieren aber als Andockstellen für andere Regulatoren, einschließlich microRNAs, die die Menge des produzierten Proteins feinjustieren. Das Protein Nudt21 hilft der Zelle bei der Wahl der Schnittstelle und bestimmt damit, wie lang diese RNA-Schwänze werden.
Ein einzelner Regelknopf mit zwei sehr unterschiedlichen Effekten
Die Forschenden konstruierten Mäuse, bei denen Nudt21 in erwachsenen Geweben heruntergedreht oder vollständig ausgeschaltet werden konnte. Wurde Nudt21 im gesamten Körper vollständig entfernt, erkrankten die Tiere rasch und starben, jedoch nicht, weil „statische“ Organe wie Herz oder Niere versagten. Stattdessen verloren Gewebe mit hoher Erneuerungsrate — etwa die Auskleidung von Darm und Speiseröhre, das blutbildende System im Knochenmark und Muskelstammzellen (sogenannte Satellitenzellen) — ihre Fähigkeit zur Erneuerung. Stamm- und Vorläuferzellen in diesen Geweben blieben im Zellzyklus stehen und versäumten, ihre DNA zu replizieren und sich zu teilen. Im Gegensatz dazu konnten sich bei einer nur teilweisen Reduktion der Nudt21-Spiegel die Stammzellen zwar weiterhin vermehren, reiften aber nicht mehr korrekt zu spezialisierten Zellen heran. Das zeigt, dass Selbst-Erneuerung und Differenzierung unterschiedlich empfindlich auf die Dosis desselben Regulationsfaktors reagieren.
Verkürzte Botschaften, die die Bremsen der Differenzierung umgehen
Um die intrazellulären Veränderungen zu analysieren, kartierte das Team die Schnittstellen der RNA-Botschaften und untersuchte Verschiebungen der Proteinmengen. Bei moderater Reduktion von Nudt21 wechselten etwa tausend RNA-Botschaften von längeren zu kürzeren Schwanzregionen. Da viele der verlorenen Abschnitte Bindungsstellen für microRNAs enthielten, wurden diese verkürzten Botschaften schwerer zu unterdrücken. Wichtige Regulatoren von Zellidentität und Entwicklung, darunter Enzyme, die die DNA-Verpackung umgestalten, und Transportproteine, wurden im Überschuss produziert. Diese Überproduktion störte empfindliche „konkurrenzielle RNA“-Netzwerke, in denen viele Botschaften dieselben microRNA-Regulatoren teilen. Als Folge blieben Stammzellen in einem unreifen Zustand: Sie behielten Stammzellmarker, schalteten aber die für die vollständige Differenzierung nötigen Gene nicht ein, selbst wenn sie starke pro-differenzierende Signale erhielten.
Wenn die Maschinerie der Zelle auseinanderfällt
Der vollständige Verlust von Nudt21 hatte eine schwerere und unerwartete Konsequenz. Zusätzlich zur Differenzierungsblockade erhielten viele Botschaften, die Bestandteile essentieller Mehrprotein-Maschinen kodieren, verkürzte Schwänze. Diese Botschaften produzierten im Gegensatz dazu tendenziell weniger Protein, nicht mehr. Das eindrücklichste Beispiel war der nukleäre Porenkomplex, das große Tor, das die Kernhülle durchspannt und den Export von RNAs aus dem Zellkern ermöglicht. Fast die Hälfte der Bausteine dieses Porenkomplexes zeigte veränderte Schwanzlängen und ging in ihrer Menge zurück, wodurch Poren von der Kernoberfläche verschwanden, RNA sich im Zellkern ansammelte und Anzeichen von DNA-Schäden auftraten. Durch selektives Entfernen nur der langschwänzigen Region eines einzelnen Porenbestandteils, Nup160, konnten die Forschenden vieles des vollständigen Nudt21-Verlusts nachahmen: Kernporen wurden instabil, genetisches Material brach während der Zellteilung, und Stammzellen stellten die Erneuerung ein. Ähnliche Störungen wurden in anderen kritischen Komplexen beobachtet, die an Proteinsynthese und RNA-Prozessierung beteiligt sind, was darauf hindeutet, dass die richtige Wahl der Schwanzlänge hilft, die Zusammensetzung dieser großen Maschinerien zu koordinieren. 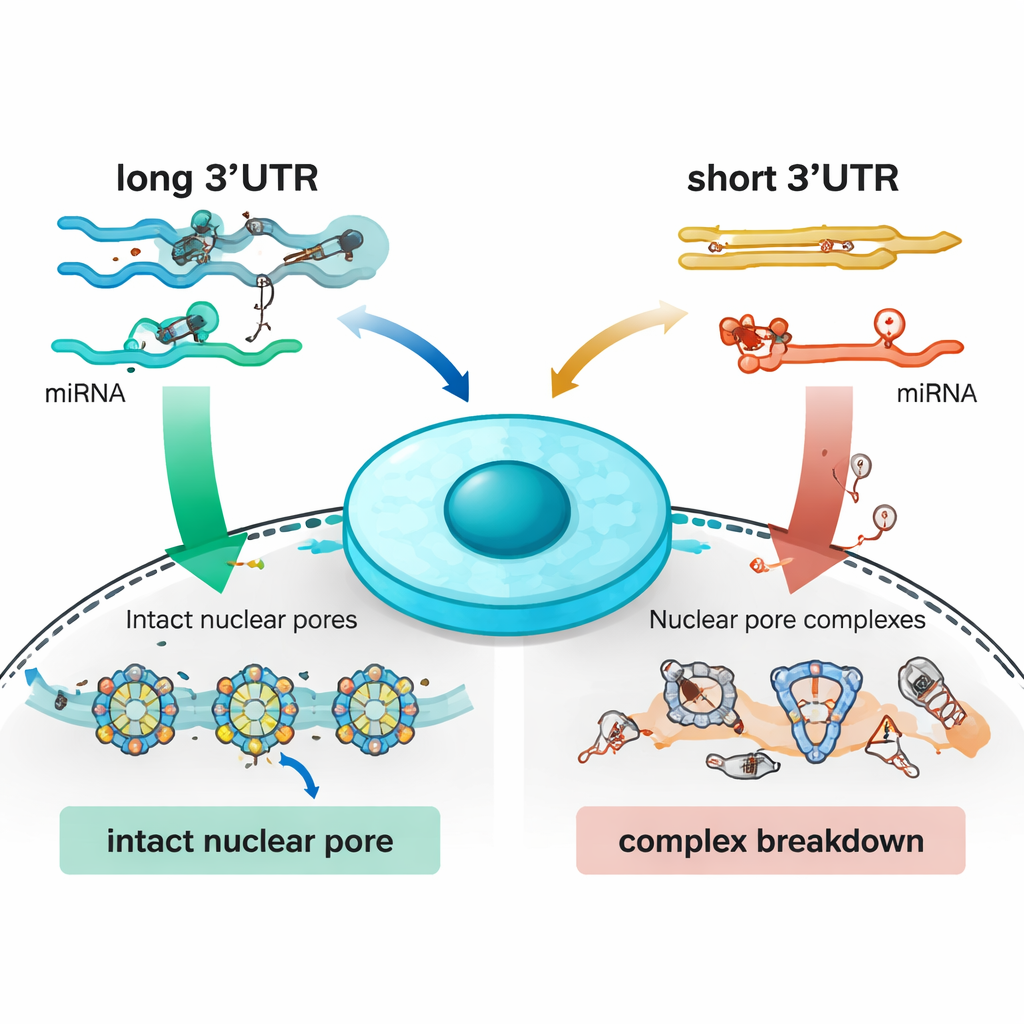
Warum das für Gesundheit, Altern und Krebs wichtig ist
Für Nicht-Spezialisten lautet die Kernbotschaft: Die von Stammzellen getriebene Reparatur hängt nicht nur davon ab, welche Gene ein- oder ausgeschaltet sind, sondern auch davon, wie genau ihre RNA-Botschaften abgeschlossen werden. Nudt21 wirkt wie ein dosis-sensitiver Hauptregler dieses Abschluss-Schritts. Eine leichte Herunterregulierung erlaubt den Stammzellen, sich weiter zu teilen, hält sie jedoch in einem unreifen, schwer differenzierbaren Zustand — eine Situation, die bestimmten aggressiven Krebsarten ähneln könnte. Eine zu starke Reduktion führt dazu, dass zentrale zelluläre Maschinerien, wie Nukleoporine, auseinanderfallen, was zu DNA-Schäden und Verlust der regenerativen Fähigkeit führt. Das Verständnis und die Kontrolle dieses RNA-Schwanz-Schneide-Mechanismus könnte neue Wege eröffnen, Geweberegeneration zu fördern, die Genomstabilität im Alter zu schützen oder Krebszellen gezielt in einen tödlichen Ausfallzustand zu treiben.
Zitation: Tsopoulidis, N., Yagi, M., Brumbaugh, J. et al. Modulation of Nudt21 levels reveals dose-dependent roles of alternative polyadenylation in tissue regeneration. Nat Commun 17, 2005 (2026). https://doi.org/10.1038/s41467-026-68630-x
Schlüsselwörter: Stammzellen, Geweberegeneration, RNA-Prozessierung, nukleärer Porenkomplex, alternative Polyadenylierung