Clear Sky Science · de
G9a-vermittelte H3K9me2 steuert die Regeneration des intestinalen Epithels durch epigenetische Stilllegung zellzyklusbezogener Gene
Warum die Selbstreparatur des Darms wichtig ist
Jeden Tag ist die Schleimhaut Ihres Darms harten Bedingungen ausgesetzt: Magensäure, Nahrungsbestandteile und Billionen von Mikroben. Dennoch überlebt dieses Gewebe nicht nur, es erneuert sich ständig. Wenn dieses Reparatursystem versagt – nach Strahlentherapie, bei entzündlichen Darmerkrankungen oder bei schweren Infektionen – können Schmerzen, Blutungen und lebensbedrohliche Komplikationen auftreten. Diese Studie enthüllt einen verborgenen „Schalter“ in Darmzellen, der ihnen hilft zu entscheiden, wann sie aus der Ruhephase heraustreten und mit dem Wiederaufbau beginnen sollen, und liefert Hinweise auf neue Behandlungsansätze, die die natürliche Reparaturkraft des Darms stärken könnten.
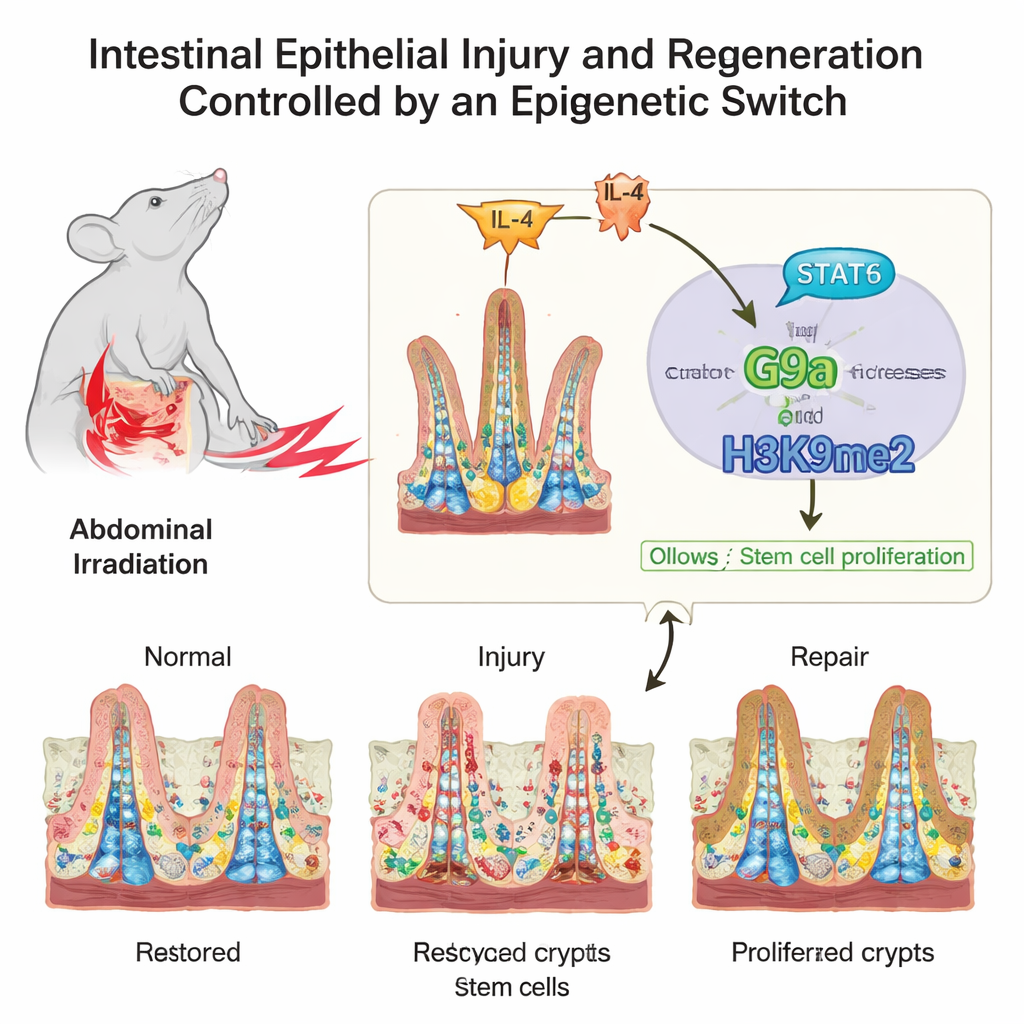
Eine fragile Architektur unter ständigem Stress
Die innere Oberfläche des Darms ähnelt unter dem Mikroskop einem flauschigen Teppich: fingerartige Zotten, die Nährstoffe aufnehmen, und Gruben, sogenannte Krypten, in denen die Stammzellen leben. Diese Stammzellen und ihre schnell teilenden Töchter müssen ein Gleichgewicht zwischen kontinuierlicher Erneuerung und Notfallreparatur halten. Die Autoren konzentrierten sich darauf, wie chemische Markierungen an den DNA verpackenden Proteinen, den Histonen, dieses Gleichgewicht beeinflussen. Diese Markierungen verändern nicht die Gene selbst, sondern funktionieren eher wie Dimmer-Schalter, die Gencluster hoch- oder runterregeln, wenn der Darm vom Normalzustand in die Verletzung und zurück zur Gesundheit übergeht.
Eine epigenetische Markierung, die Schaden und Heilung verfolgt
An Mäusen, die Strahlung ausgesetzt wurden – eine häufige Ursache für Darmverletzungen bei Krebsbehandlungen – untersuchten die Forscher zahlreiche Histonmarken in den stamzellreichen Krypten. Eine Marke, bekannt als H3K9me2, stieg deutlich an, als der Darm vom Verletzungszustand in die Reparaturphase überging. Ihr schreibendes Enzym, das Protein G9a, zeigte dasselbe Muster. Das Team untersuchte dann humane Proben von Patienten nach Beckenstrahlentherapie sowie von Personen mit Morbus Crohn. In beiden Fällen gingen höhere H3K9me2- und G9a-Level in Darmzellen mit besseren Zeichen der Gewebereparatur einher, was darauf hindeutet, dass dieses System bei Mäusen und Menschen konserviert ist.
Wenn der Reparaturschalter beschädigt ist
Um zu prüfen, ob diese Markierung nur ein Begleitphänomen ist oder tatsächlich die Heilung antreibt, entfernten die Wissenschaftler G9a spezifisch aus der Darmschleimhaut von Mäusen oder blockierten seine Aktivität mit einem Wirkstoff. In beiden Fällen fielen die H3K9me2-Werte. Nach Strahlen- oder chemischer Verletzung verloren diese Mäuse mehr Gewicht, hatten kürzere und stärker geschädigte Därme und zeigten weniger regenerierende Krypten und Stammzellen als normale Tiere. Selbst ohne gezielte Verletzung wirkte die Darmschleimhaut G9a-defizienter Mäuse unterentwickelt: Die Krypten waren flacher, die Zotten kürzer und die Anzahl der Stammzellen sowie ihrer spezialisierten Nachkommen verringerte sich. Winzige „Mini-Därme“, aus diesen Zellen im Labor gezüchtet, wuchsen ebenfalls schlecht, was unterstreicht, dass dieses molekulare System zentral für die tägliche Erneuerung des Darms ist.
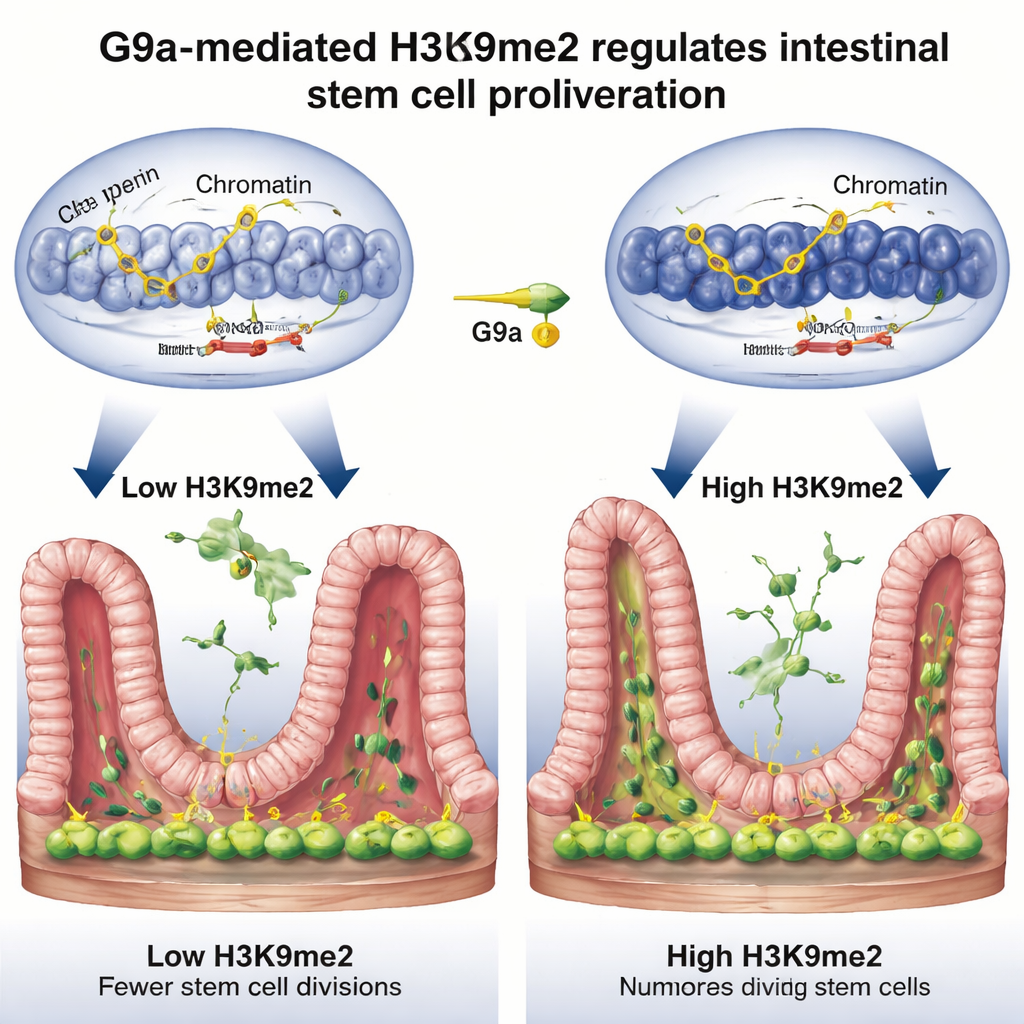
Die Bremsen der Zellteilung lösen
Bei genauerer Untersuchung fragten die Forscher, welche Gene dieser Reparaturschalter kontrolliert. Durch die Kombination dreier leistungsfähiger genomweiter Methoden fanden sie heraus, dass H3K9me2, aufgebracht von G9a, dazu neigt, sich auf DNA-Abschnitte zu legen, die normalerweise als Bremsen des Zellzyklus wirken – Gene wie Rb1cc1, Rb1, Cdkn1a und Pten, die die Zellteilung verlangsamen oder stoppen. Fehlt G9a, verschwindet die chemische Markierung aus diesen Regionen, die umgebende DNA öffnet sich und diese Bremsgene werden stärker aktiviert, was zu einer trägeren Proliferation der Stammzellen führt. Während der normalen Reparatur nach Verletzung steigen die H3K9me2-Level an diesen Genen, ihre Aktivität sinkt und die Stammzellen können freier teilen und das Epithel wiederaufbauen. Im Wesentlichen dämpfen G9a und H3K9me2 vorübergehend die „Stopp“-Signale, damit das Gewebe nachwachsen kann.
Eine Signalkette von Immunhinweisen zur Reparatur
Der Darm handelt nicht isoliert; er hört kontinuierlich auf Signale des Immunsystems. Die Forscher verfolgten ein solches Signal stromaufwärts von G9a. Nach einer Verletzung stiegen die Werte des Immunboten IL‑4 an, was die Aktivierung eines Proteins namens STAT6 in den Darmzellen auslöste. Aktiviertes STAT6 bindete direkt an die Kontrollregion des G9a-Gens und steigerte dessen Produktion. So entstand eine Befehlskette: IL‑4 aktiviert STAT6, STAT6 erhöht G9a, und G9a fügt H3K9me2 hinzu, um Zellzyklus-Bremsgene stummzuschalten, wodurch sich Stammzellen ausdehnen und die beschädigte Schleimhaut wiederherstellen können.
Was das für künftige Therapien bedeutet
Für Nichtfachleute zeigen diese Befunde, dass die Darmreparatur nicht nur von Genen geleitet wird, sondern von reversiblen chemischen Markierungen, die fein abstimmen, wann diese Gene genutzt werden. Der IL‑4–STAT6–G9a–H3K9me2‑Weg wirkt wie ein internes Bedienfeld, das die Bremsen der Stammzellteilung nur so lange löst, bis geheilt ist, und dann zurückgesetzt werden kann. Künftig könnten Therapien, die diesen Weg sanft verstärken – etwa Wirkstoffe oder gentherapeutische Ansätze, die G9a zur richtigen Zeit am richtigen Ort erhöhen – Patienten helfen, sich nach Strahlenschäden, Schüben entzündlicher Darmerkrankungen oder anderen Schädigungen der Darmschleimhaut schneller zu erholen, bei gleichzeitiger Minimierung des Risikos unkontrollierten Zellwachstums.
Zitation: Chen, J., Shi, X., Zhou, X. et al. G9a-mediated H3K9me2 orchestrates intestinal epithelial regeneration through epigenetic silencing of cell cycle-related genes. Nat Commun 17, 1874 (2026). https://doi.org/10.1038/s41467-026-68626-7
Schlüsselwörter: Darmregeneration, Epigenetik, Stammzellen, Histonmethylierung, entzündliche Darmerkrankung