Clear Sky Science · de
WDR5 formt NANOG-Kondensate um, um Transkriptionsprogramme zu steuern und die Stammzellidentität zu erhalten
Warum das für Stammzellen und Krebs wichtig ist
Stammzellen besitzen die bemerkenswerte Fähigkeit, sich in viele verschiedene Zelltypen zu verwandeln – eine Eigenschaft, die die frühe Entwicklung, die Gewebereparatur und leider auch manche Krebsarten antreibt. Diese Studie zeigt, wie zwei Schlüsselproteine, NANOG und WDR5, zusammenarbeiten, um Stammzellen in diesem flexiblen Zustand zu halten. Indem sie belegt, dass WDR5 die physikalische Organisation von NANOG auf der DNA umgestalten kann, verbindet die Arbeit die Physik von Proteintröpfchen im Zellkern mit der Genregulation in gesunden Stammzellen und bei Leukämien.
Proteine, die über das Schicksal einer Zelle entscheiden
Embryonale Stammzellen bleiben pluripotent – also nahezu jede Zellart bilden können – dank Master-Regulatoren wie NANOG, OCT4 und SOX2. Diese Proteine schalten ganze Gennetzwerke an und aus. NANOG ist dabei besonders zentral: Es bindet nicht nur DNA, sondern rekrutiert auch große Enzymkomplexe, die aktivierende chemische Markierungen an Histonen anbringen, den Proteinen, die DNA verpacken. WDR5 ist ein weiterer entscheidender Akteur. Es unterstützt Histon-modifizierende Maschinen dabei, Markierungen zu setzen, die aktive Gene kennzeichnen. Obwohl sowohl NANOG als auch WDR5 dafür bekannt sind, die Stammzellidentität zu stützen, war unklar, wie sie auf molekularer Ebene miteinander kommunizieren und ob das ihre Fähigkeit beeinflusst, winzige Tröpfchen – oder „Kondensate“ – im Zellkern zu bilden.
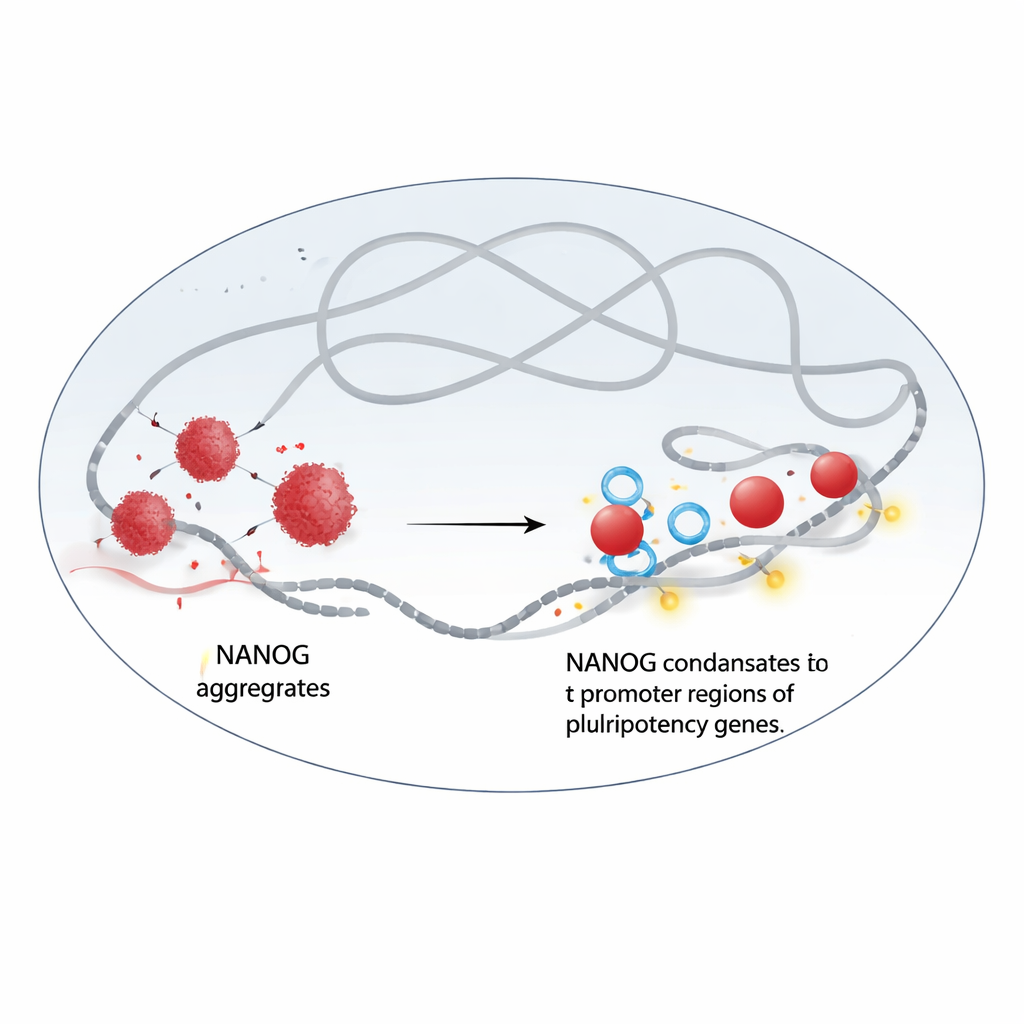
Von Klumpen zu flüssigen Tröpfchen
Die Autoren fanden heraus, dass NANOG und WDR5 direkt miteinander interagieren. Wenn NANOG alleine gereinigt wird, neigt es dazu, in unregelmäßige, festartige Aggregate zu verklumpen. Mithilfe von Elektronenmikroskopie und Fluoreszenzexperimenten zeigte das Team, dass die Zugabe von WDR5 diese Klumpen in runde, flüssigkeitsähnliche Tröpfchen umorganisiert, die sich als dynamische Kondensate verhalten. In lebenden Zellen sammeln sich NANOG und WDR5 in hellen nukleären Punkten, die sich schnell auflösen, wenn eine Chemikalie verwendet wird, die für die Störung von flüssig–flüssiger Phasentrennung bekannt ist. Wenn dies geschieht, verlieren beide Proteine weitgehend ihren Halt am Chromatin, dem DNA–Protein-Komplex, der unsere genetische Information speichert, und ihre Anwesenheit an wichtigen Pluripotenzgenen nimmt stark ab.
Ein spezieller molekularer Handschlag
Um die Partnerschaft auf atomarer Ebene zu verstehen, lösten die Forscher die Kristallstruktur der DNA-bindenden Region von NANOG in Komplex mit WDR5. Im Gegensatz zu vielen anderen WDR5-Partnern, die kurze flexible Schleifen verwenden, bindet NANOG WDR5 über eine ausgedehnte Oberfläche, die sowohl einen ungeordneten Arm als auch benachbarte Helices umfasst. Eine einzelne Arginin-Aminosäure in NANOG an Position 153 steckt tief in einen zentralen Kanal von WDR5 und bildet einen Schlüsselteil der „Schloss-und-Schlüssel“-Interaktion. Der Austausch dieser Aminosäure gegen Alanin (die R153A-Mutation) hebt die Bindung weitgehend auf. Wichtig ist, dass das mutierte NANOG weiterhin DNA binden kann, aber WDR5 seine Aggregate nicht mehr effizient in flüssige Tröpfchen umwandeln kann, was darauf hinweist, dass dieser spezifische Kontakt essenziell für die Bildung funktioneller Kondensate ist.
Stammzellen jung halten – und was passiert, wenn das fehlschlägt
Als die Autoren Maus-embryonale Stammzellen so konstruierten, dass sie nur das NANOG-R153A-Mutant exprimierten, waren die Folgen dramatisch. Die mutanten Zellen verloren die dichten, kuppelförmigen Kolonien, die für pluripotente Zellen typisch sind, und flachten ab – ein optisches Zeichen von Differenzierung. Sie bildeten weniger alkalisch‑phosphatasepositive Kolonien, ein weiteres Kennzeichen der Stammzellhaftigkeit, und reduzierten die Expression vieler zentraler Pluripotenzgene wie Nanog selbst, Sox2, Esrrb und Klf4. Gleichzeitig wurden Gene, die mit bestimmten Zelllinien assoziiert sind, darunter Knochen- und Entwicklungsregulatoren, aktiviert. Genomweite Profilierungen zeigten, dass NANOG und WDR5 nicht länger gemeinsam Tausende von Promotoren belegten, und zwei wichtige aktivierende Histonmarken, H3K4me3 und H4K16ac, gingen speziell an diesen gemeinsamen Stellen verloren. Früh in der Differenzierung fielen diese chemischen Markierungen und neu synthetisierte RNA-Transkripte ab, noch bevor die Gesamt-mRNA-Spiegel sanken, was auf ein primäres Versagen in der Aufrechterhaltung aktiven Chromatins hindeutet.
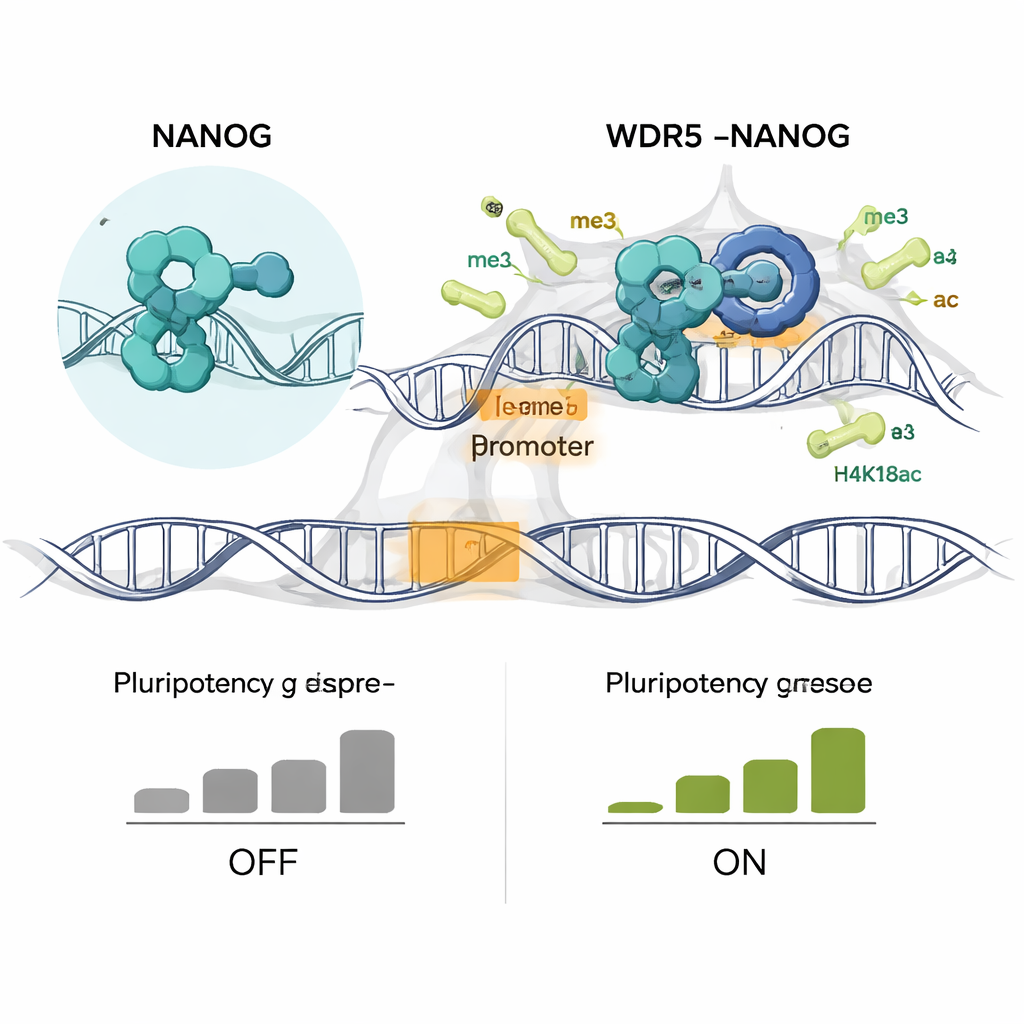
Ein grundlegender Mechanismus als Strategie gegen Krebs
Da ähnliche Genprogramme einige Krebsstammzellen antreiben, testete das Team, ob die Störung der NANOG–WDR5-Achse Leukämie-Stammzellen in einem Mausmodell der akuten myeloischen Leukämie eindämmen könnte. Ein kleines Molekül, C16, das dieselbe WDR5-Tasche bindet, die auch NANOG nutzt, schwächte selektiv die WDR5–NANOG-Interaktion. In Leukämiezellen reduzierte C16 die Koloniebildung stark, erschöpfte die stammszellähnliche Population und trieb die Zellen in reifere myeloische Schicksale, während normale Blutstammzellen deutlich stärker geschont wurden als durch ein bestehendes Leukämie-Medikament, das einen anderen WDR5-Partner angreift. RNA-Sequenzierungen zeigten, dass C16 Genprogramme für Stammhaftigkeit und Selbsterneuerung herunterfuhr und Differenzierungswege förderte. In Mäusen verringerte die Behandlung mit C16 die Leukämie-Stamm- und Vorläuferpopulationen, was das therapeutische Potenzial eines Angriffs auf diese Proteinpartnerschaft unterstreicht.
Großes Bild: Wie Tröpfchen über Zellidentität mitentscheiden
Diese Arbeit zeigt, dass WDR5 mehr tut, als nur am Chromatin zu sitzen und Enzyme zu rekrutieren: Es kann NANOG physikalisch von inerten Aggregaten in flexible flüssige Kondensate umformen, die auf Promotoren von Pluripotenzgenen sitzen und aktivierende Histonmarken anziehen. Wenn diese Umgestaltung blockiert wird – sei es durch eine präzise Mutation in NANOG oder durch ein kleines Molekül, das ihren Kontakt stört – verlieren Stammzellen ihre Identität und Krebsstammzellen ihre Fähigkeit zur Selbsterneuerung. Für Leser ohne Fachwissen lautet die Kernbotschaft, dass schon kleine Veränderungen darin, wie Proteine als Tröpfchen auf DNA zusammenkommen, enorme Folgen haben können: ob eine Zelle jung und flexibel bleibt, in ein bestimmtes Schicksal reift oder Krankheit antreibt.
Zitation: Wang, D., Shi, X., Xie, J. et al. WDR5 remodels NANOG condensates to drive transcriptional programs and sustain stem cell identity. Nat Commun 17, 1907 (2026). https://doi.org/10.1038/s41467-026-68623-w
Schlüsselwörter: Stammzellpluripotenz, NANOG, WDR5, Phasentrennung, Leukämie-Stammzellen