Clear Sky Science · de
Duale Quorum-Sensing-Signal-Synthasen DspII und DspI koordinieren den Virulenz‑Schalter in Pseudomonas aeruginosa
Wie ein Krankenhauskeim seine Angriffsstrategie ändert
Pseudomonas aeruginosa ist ein berüchtigter Krankenhauskeim, der hartnäckige Lungen‑ und Wundinfektionen verursachen kann, besonders bei geschwächten Patientinnen und Patienten. Er überlebt, indem er zwischen zwei Lebensweisen wechselt: einer geschützten, langsam wachsenden Gemeinschaft namens Biofilm und einer schnellen, aggressiven Form, die Gewebe angreift. Diese Studie zeigt, wie das Bakterium selbst entscheidet, wann es aus einem lang bestehenden Biofilm ausbricht und einen plötzlichen akuten Angriff startet, und legt damit potenzielle neue Schwachstellen für künftige Behandlungen offen.
Ein mikrobielles Leben zwischen Verstecken und Angreifen
Viele bakterielle Infektionen verlaufen in Phasen. In frühen Stadien breiten sich frei schwimmende Zellen im Körper aus und setzen mächtige Waffen frei, die Wirtsgewebe schädigen. Später sesshaft werden sie oft in Biofilmen—dicken, schleimigen Schichten an Oberflächen wie Kathetern, Lungengewebe oder Wunden. In diesen Gemeinschaften sind die Zellen von einer schützenden Matrix umgeben, die sie gegenüber Antibiotika und Immunabwehr schwer angreifbar macht. Biofilme sind jedoch kein Endpunkt: Zellen können den Biofilm verlassen, Motilität zurückgewinnen und neue Runden akuter Infektion an anderen Stellen auslösen. Bislang war unklar, wie Pseudomonas aeruginosa diesen Wechsel von chronischem Verbleib zurück zu aggressiver Krankheit aktiv koordiniert.
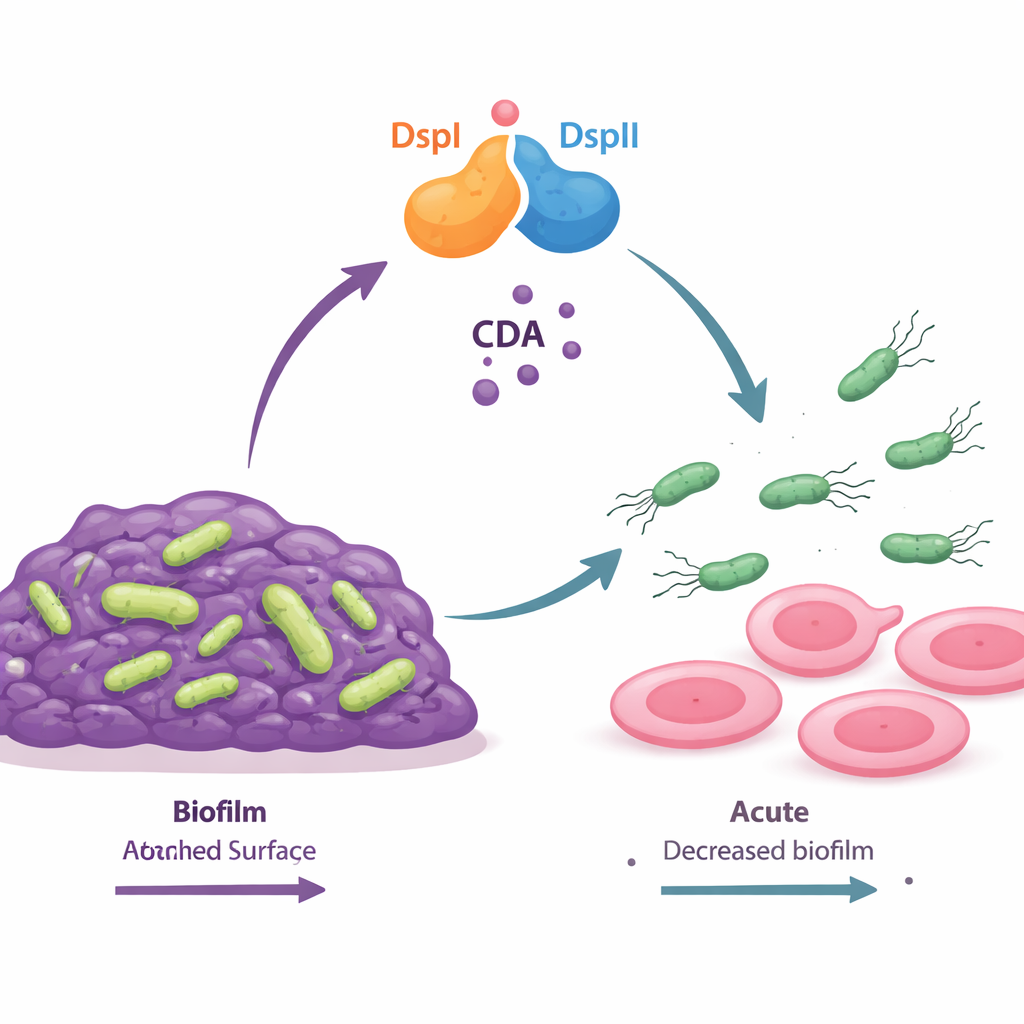
Ein Zwei‑Protein‑Schalter, der ein chemisches "Los"‑Signal erzeugt
Die Autorinnen und Autoren entdeckten, dass zwei bakterielle Proteine, DspI und DspII genannt, zusammen als eine Art molekularer Schalter funktionieren. Beide sind Enzyme desselben allgemeinen Typs und liegen nebeneinander im bakteriellen Genom, wobei sie mit zunehmender Populationsdichte gemeinsam hochreguliert werden. Wenn sie ein Paar bilden, stellen sie ein kleines Fettsäure‑Signal her, die cis‑2‑Decensäure (CDA), die zu einer größeren Gruppe von Kommunikationsmolekülen gehört, den DSF‑Signalen. Mutanten, denen entweder DspI oder DspII fehlt, konnten kein CDA mehr produzieren, bildeten ungewöhnlich dicke Biofilme und verloren die Fähigkeit, über Oberflächen zu „swarmen“. Nur wenn beide Proteine gemeinsam wiederhergestellt wurden, erholten die Zellen die normale Signalproduktion, den Biofilmabbau und die Motilität—ein Befund, der zeigt, dass die beiden Enzyme als voneinander abhängiges Team funktionieren.
Vom chemischen Signal zu Bewegung und Flucht
CDA wirkt nicht isoliert; es greift in die interne Signalübermittlung des Bakteriums ein. Das Team zeigte, dass CDA die Konzentration eines anderen Botenmoleküls, cyclic di‑GMP, senkt, indem es die Aktivität eines spezifischen Enzyms namens RbdA erhöht, das diesen Boten abbaut. Hohe cyclic di‑GMP‑Werte fördern üblicherweise den Biofilmaufbau, indem sie die Produktion der zuckrigen Matrix stimulieren und die Flagellen—die winzigen Propeller fürs Schwimmen—unterdrücken. In Anwesenheit von CDA sinken die cyclic di‑GMP‑Spiegel, ein Regulator namens FleQ schaltet um, die klebrige Zuckersynthese nimmt ab, und Flagellen werden ausgestreckt und gestärkt. Dadurch lockern sich die Biofilme und die Zellen gewinnen die Fähigkeit zurück, sich wegzubewegen und neue Lebensräume zu besiedeln.
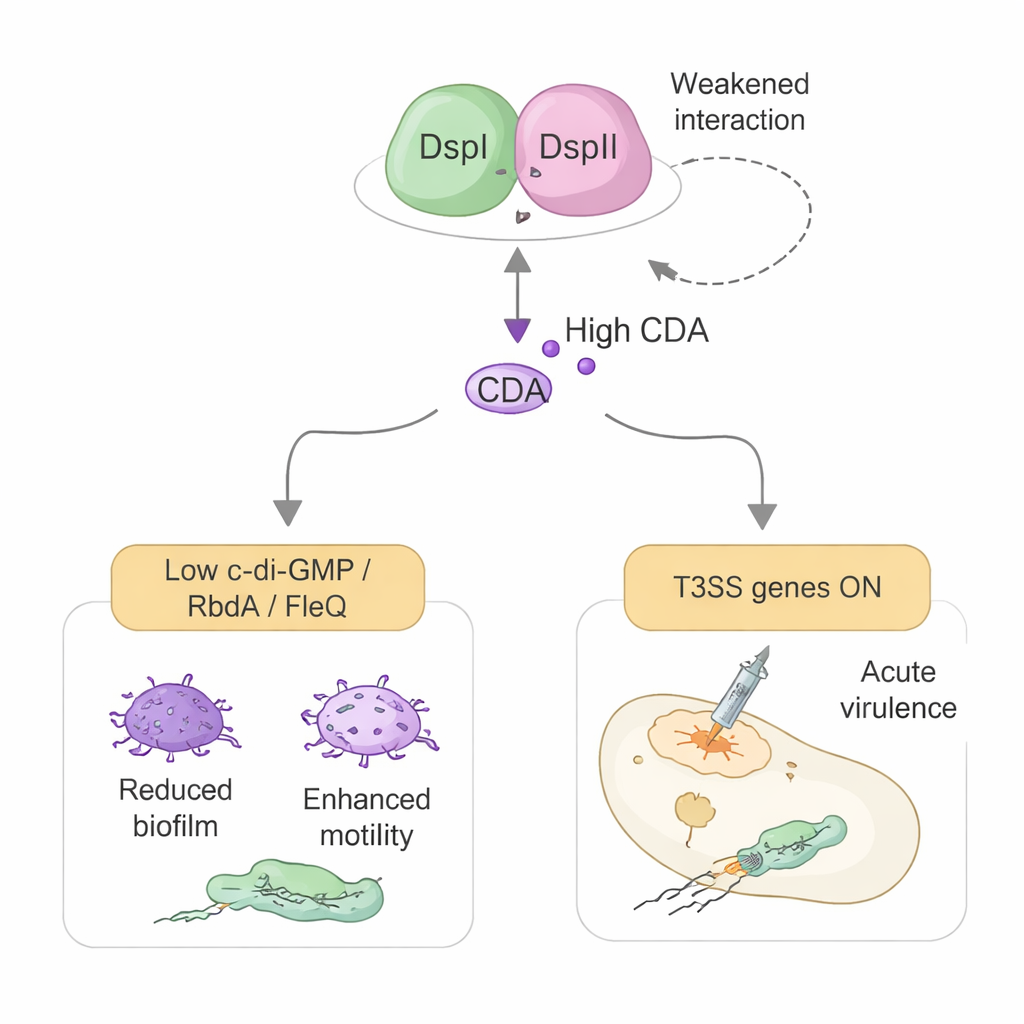
Umschaltung des bakteriellen Waffensystems
Die Studie offenbart außerdem eine zweite, unerwartete Rolle von DspI und DspII, die über die Chemie hinausgeht. Dasselbe Proteinpaar hilft, das Typ‑III‑Sekretionssystem (T3SS) des Bakteriums einzuschalten—eine spritzenartige Apparatur, mit der Toxine direkt in Wirtszellen injiziert werden. Dieser Effekt läuft nicht über CDA, sondern über direkte Kontrolle genetischer Schalter. DspI und DspII dämpfen die Produktion von zwei kleinen regulatorischen RNAs, RsmY und RsmZ, die normalerweise die T3SS‑Proteinsynthese abschalten. Sie tun dies, indem sie an die DNA‑Kontrollregion einer dieser RNAs binden und physisch mit einem Master‑Regulatorprotein namens GacA interagieren. Wenn RsmY und RsmZ unterdrückt sind, wird ein nachgeschalteter Aktivator namens RsmA freigesetzt, und die Gene für das T3SS sowie sein Hauptregulator ExsA werden aktiviert—was die Zytotoxizität in Zellkultur erhöht und die Mortalität in einem Insekteninfektionsmodell steigert.
Ein selbstabstimmendes System mit Angriffspunkten für Medikamente
Klugerweise wird die Stärke der DspI–DspII‑Partnerschaft und ihre Kontrolle über die Virulenz selbst durch CDA‑Spiegel reguliert. Bei niedrigen Konzentrationen—wie sie in Zellen zu erwarten sind, die gerade einen Biofilm verlassen—verstärkt CDA die Wechselwirkung der beiden Proteine und fördert sowohl die weitere Signalproduktion als auch die Aktivierung des T3SS. Bei hohen Konzentrationen, wie sie in dichten Biofilmen vorkommen, schwächt CDA ihre Interaktion und verringert deren DNA‑Bindung, wodurch weitere Signalbildung und die kostspielige Produktion von Waffen in sesshaften Zellen begrenzt werden. Diese doppelte Rolle macht den DspI–DspII‑Komplex zu einem zentralen Knotenpunkt, der Populationsgröße, Biofilmflucht und akute Virulenz verknüpft. Da eine Störung des Komplexes sowohl die Signalproduktion als auch die Aktivierung des Toxin‑Systems blockieren kann, bietet er ein attraktives Ziel für künftige Medikamente, die Pseudomonas in einem weniger schädlichen, chronischen Zustand halten und gefährliche Aufflackern verhindern könnten.
Zitation: Huang, J., Zhou, T., Zhou, X. et al. Dual-functional quorum sensing signal synthases DspII and DspI coordinate virulence switch in Pseudomonas aeruginosa. Nat Commun 17, 1926 (2026). https://doi.org/10.1038/s41467-026-68622-x
Schlüsselwörter: Pseudomonas aeruginosa, Biofilm‑Dispersion, Quorum Sensing, Virulenz‑Schalter, cis‑2‑Decensäure