Clear Sky Science · de
Dynamische Signatur des Aktivitäts‑Stabilitäts‑Kompromisses in der Evolution von Lactamasen
Warum das für Antibiotikaresistenz wichtig ist
Antibiotikaresistenz wirkt oft wie eine Blackbox: Bakterien verändern sich „irgendwie“ und Medikamente verlieren ihre Wirkung. Diese Studie öffnet diese Box für eines der weltweit am besten untersuchten Resistenzenzyme, die TEM‑1 β‑Lactamase, das Bakterien dabei hilft, penicillinähnliche Antibiotika zu zerstören. Indem die Autoren beobachten, wie sich Form und Bewegungen dieses Enzyms verändern, während es sich an neuere Wirkstoffe anpasst, zeigen sie, warum Mutationen, die die Aktivität steigern, oft die Stabilität schwächen — und wie die Evolution beides geschickt ausbalanciert.
Vom Penicillin‑Fighter zum breiteren Wirkstoff‑Zerstörer
TEM‑1 ist ursprünglich darauf spezialisiert, ältere Penicillinantibiotika zu spalten, ist aber schlecht darin, neuere, sperrigere Wirkstoffe wie Cefotaxim zu verarbeiten. In vielen klinischen Stämmen tritt eine einzelne Schlüsselmutation namens G238S nahe der aktiven Stelle des Enzyms auf, der Tasche, in der Antibiotika geschnitten werden. Diese Mutation verbessert dramatisch die Fähigkeit des Enzyms, Cefotaxim zu zerstören, ohne seine ursprüngliche Penicillin‑Aktivität stark zu beeinträchtigen. Die Autoren zeigen, dass G238S die Tasche nicht einfach nur weitet; sie reorganisiert die Bewegungen mehrerer umliegender Schleifen und Helices und erzeugt so eine neue funktionelle Konformation, die sperrige Wirkstoffe besser aufnimmt.
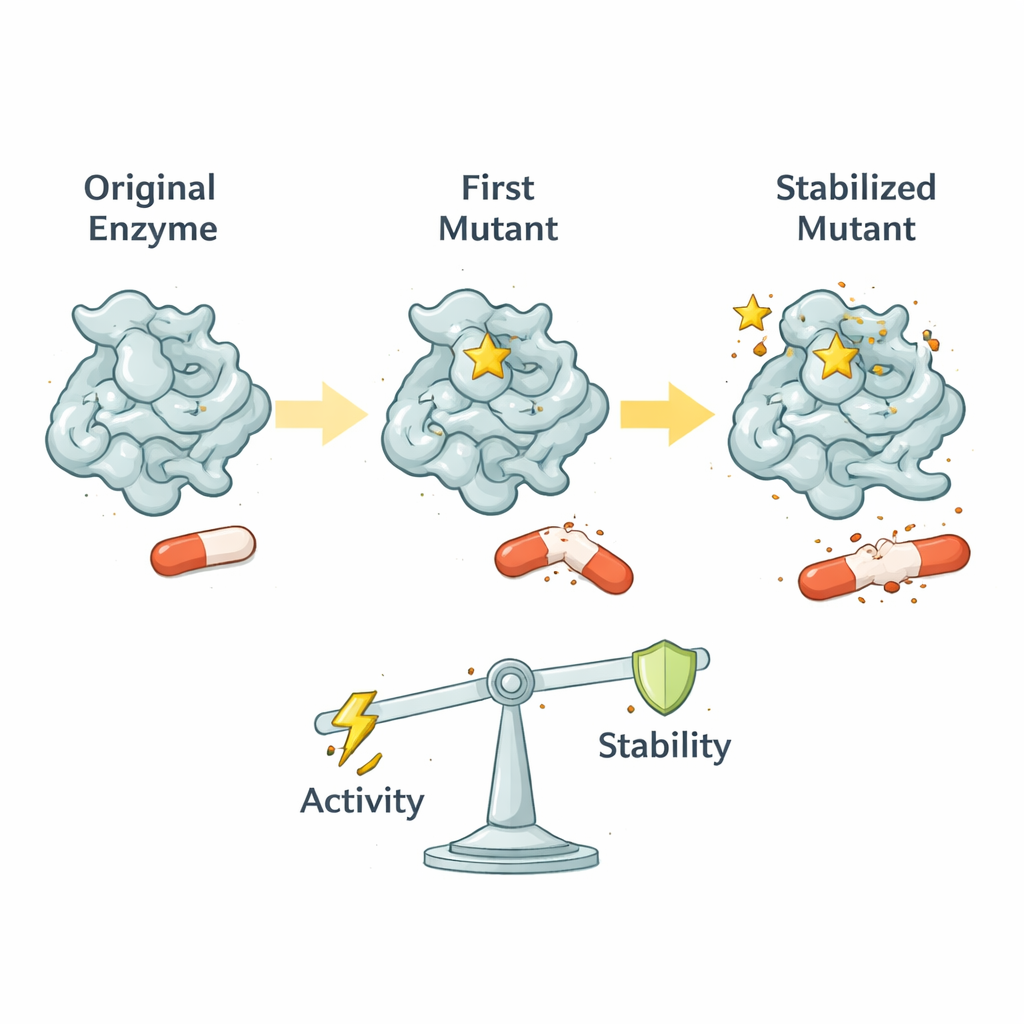
Proteinbewegung als evolutionärer Einstellknopf
Mit fortgeschrittenen Kernspinresonanz‑(NMR‑)Techniken maßen die Forschenden, wie sich verschiedene Teile von TEM‑1 über Zeitenstufen von Billionsteln bis Tausendsteln einer Sekunde bewegen. Das Wildtyp‑TEM‑1 ist ziemlich starr, was ihm hilft, seine ursprünglichen Substrate effizient zu verarbeiten. G238S lässt den Großteil dieser schnellen Steifigkeit erhalten, führt aber langsamer abgestimmte Bewegungen in vielen Wänden des aktiven Zentrums ein. Diese Bewegungen sind schnell genug, um mit der Chemie des Enzyms mitzuhalten, aber nicht so heftig, dass kritische katalytische Reste gestört werden. Das Ergebnis ist ein „optimiertes Fenster“ an Flexibilität: gerade genug Bewegung, um die Tasche für Cefotaxim zu öffnen, während die Kernchemie korrekt ausgerichtet bleibt.
Zwischen zwei Formen balancieren statt eine zu wählen
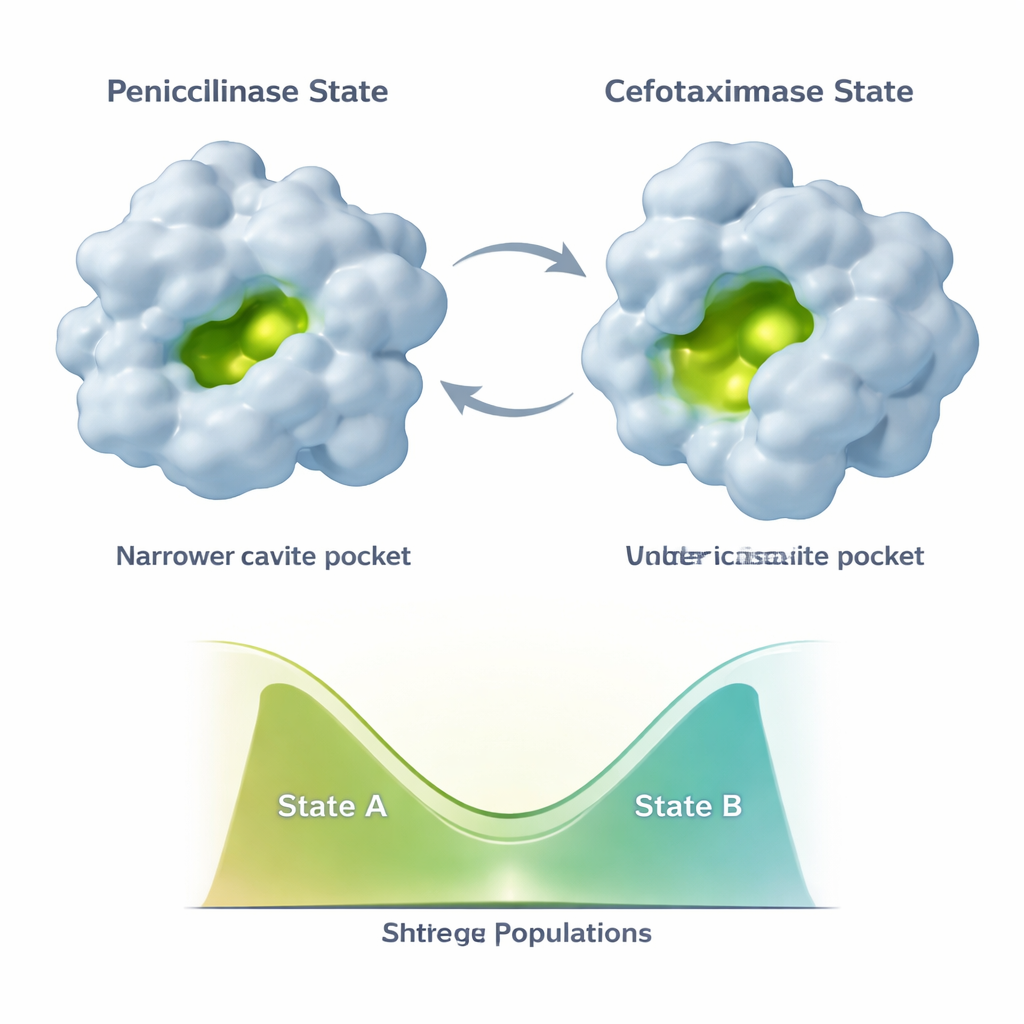
Die Evolution friert TEM‑1 nicht in eine einzige neue Form ein. Stattdessen probiert das Enzym mindestens zwei Hauptkonformationen aus: einen „Penicillinase“-Zustand, der der ursprünglichen Struktur ähnelt, und einen offeneren „Cefotaximase“-Zustand, der besser für neuere Wirkstoffe geeignet ist. Zusätzliche Mutationen, die später auftreten — etwa E104K und A42G — wirken subtil. Anstatt die neue, cefotaximase‑freundliche Form einfach stabiler zu machen, verschieben sie das Verhältnis der beiden Zustände. NMR‑Daten zeigen, dass verschiedene Teile des aktiven Zentrums und des tragenden Gerüsts ihre Populationsverhältnisse entlang dieses Zwei‑Zustands‑Kontinuums unabhängig voneinander verändern können. Das erzeugt eine kombinatorische Vielfalt an Enzymvarianten, jede mit einer unterschiedlichen Mischung aus penicillin‑ähnlichen und cefotaxim‑ähnlichen Konformationen und damit unterschiedlichen katalytischen Profilen.
Versteckte Schwachstellen und fernwirkende Reparaturen
Mutationen, die die Aktivität verbessern, tragen oft einen versteckten Preis: sie machen das Protein weniger stabil. Anstatt nur das vollständige Entfalten zu betrachten, kartierte das Team die lokale Stabilität auf Ebene kurzer Segmente mit Wasserstoff‑Deuterium‑Austausch gekoppelt an Massenspektrometrie. G238S destabilisierte nicht nur benachbarte Schleifen, sondern auch entfernte Helices und Beta‑Strang‑Regionen, die ein strukturelles Rückgrat bilden. Einige dieser Regionen überlappen mit einer „kryptischen“ allosterischen Tasche — einer selten geöffneten Öffnung im Proteinkern, die kleine Moleküle binden und die Aktivität dämpfen kann. G238S macht diese Tasche leichter zugänglich und baut damit gewissermaßen eine milde selbst‑inhibitorische Eigenschaft in das Enzym ein. Spätere Mutationen, besonders A42G, verstärken dieses geschwächte Rückgratnetzwerk, verbessern die lokale Stabilität um drei wechselwirkende Helices, ohne die vorteilhaften Dynamiken des aktiven Zentrums zu beseitigen. Anders gesagt, die Evolution flickt entfernte strukturelle Schwachstellen statt die ursprüngliche Innovation rückgängig zu machen.
Was die Studie über die Strategie der Evolution offenbart
Für einen Laien ist die zentrale Botschaft: Proteine wie TEM‑1 entwickeln Resistenz nicht durch einen einfachen An‑/Aus‑Schalter. Jede Mutation formt leicht, wie das Enzym atmet, sich biegt und seine Zeit zwischen verschiedenen Arbeitsposen aufteilt. G238S öffnet die Tür für eine neue Aufgabe — das Spalten neuerer Antibiotika — erzeugt aber zugleich lokale Schwachstellen und einen teilweise selbst‑inhibitorischen Zustand. Sekundärmutationen wirken wie behutsame Verstärkungen, stabilisieren das Gerüst und feinjustieren das Gleichgewicht zwischen alten und neuen Konformationen, sodass das Enzym sowohl aktiv als auch dauerhaft bleibt. Diese dynamische Sicht der Evolution, in der Bewegungen und lokale Schwächen ebenso wichtig sind wie die statische Struktur, kann die Entwicklung künftiger Antibiotika und enzymzielgerichteter Wirkstoffe leiten, die für Bakterien schwerer zu umgehen sind.
Zitation: Arcia, E., Keramisanou, D., Jacobs, L.M.C. et al. Dynamic signature of activity-stability tradeoff in lactamase evolution. Nat Commun 17, 1884 (2026). https://doi.org/10.1038/s41467-026-68620-z
Schlüsselwörter: Antibiotikaresistenz, Beta‑Lactamase, Proteinevolution, Enzymdynamik, Proteinmabilität