Clear Sky Science · de
Ein räumlich aufgelöstes Atlas von Magenkrebs charakterisiert eine lymphozyten-aggregierte Region
Warum die Nachbarschaft um einen Tumor wichtig ist
Krebs ist nicht einfach ein Haufen fehlgeleiteter Zellen; er lebt in einer belebten Nachbarschaft aus Immun- und Strukturzellen, die den Tumor entweder bekämpfen oder sein Wachstum ungehindert zulassen können. Diese Studie kartiert diese Nachbarschaft bei Magenkrebs mit beispielloser Detailtreue und zeigt, wie winzige Immun-Hotspots und -Coldspots innerhalb desselben Tumors beeinflussen können, ob ein Patient auf moderne Immuntherapien anspricht.
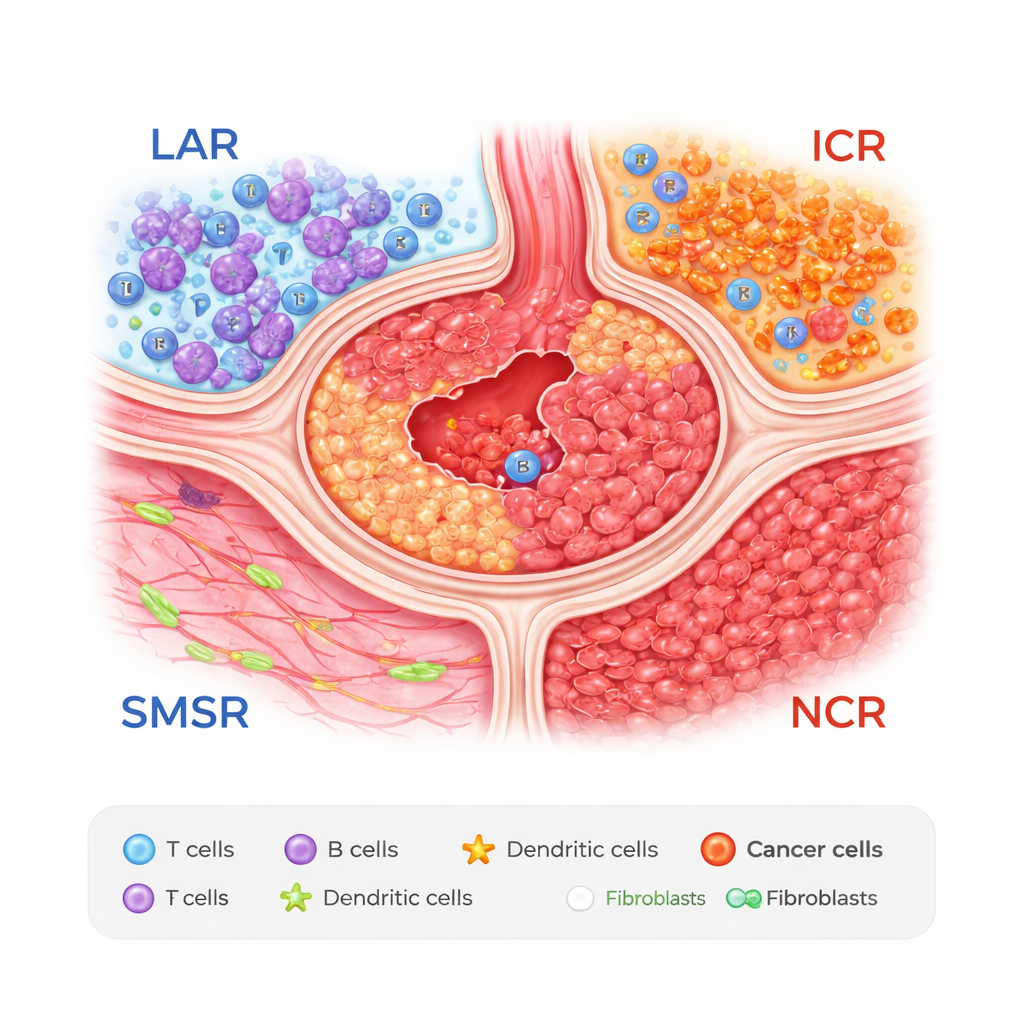
Vier Zonen innerhalb eines Magen-Tumors
Die Forschenden kombinierten zwei leistungsstarke Methoden: Einzelzell-RNA-Sequenzierung, die Genaktivität in einzelnen Zellen erfasst, und räumliche Transkriptomik, die dokumentiert, wo diese Zellen in Gewebeschnitten liegen. Anhand von Proben aus 27 Patientinnen und Patienten entdeckten sie, dass sich Magenkarzinome in vier wiederkehrende Zonen einteilen lassen. Eine davon ist eine lymphozyten-aggregierte Region (LAR), reich an Clustern von T- und B-Zellen, die Miniatur-Lymphknoten ähneln. Eine andere ist eine glatte Muskel- und Stromaregion (SMSR), dominiert von Muskel- und Bindegewebe. Die verbleibenden beiden Zonen sind krebsreiche Bereiche: eine immunogene Krebsregion (ICR), in der Tumorzellen mit einigen schützenden Magenzelltypen durchmischt sind, und eine negativ-immunogene Krebsregion (NCR), vollgepackt mit malignen Zellen und vergleichsweise wenigen Abwehrzellen.
Immun-Hotspots stehen mit besseren Ergebnissen in Verbindung
Das Team fand, dass die LAR-Zone für Gene angereichert ist, die normalerweise in Lymphknoten vorkommen, wo Immunzellen ausgebildet und aktiviert werden. Dazu gehören Signale, die Lymphozyten anziehen und sie in Strukturen organisieren, die als tertiäre lymphoide Strukturen bezeichnet werden. In großen öffentlichen Krebs-Datensätzen zeigten Tumoren mit höherer Expression von LAR-assoziierten Genen tendenziell ein besseres Überleben der Patienten und eine etwas höhere Wahrscheinlichkeit, auf Immun-Checkpoint-Therapien zu reagieren, die die Bremsen der T‑Zellen lösen. Im Gegensatz dazu waren Gensignaturen aus muskelreichen oder stark krebsbetonten Regionen meist mit schlechteren Ergebnissen über mehrere Krebsarten hinweg assoziiert.
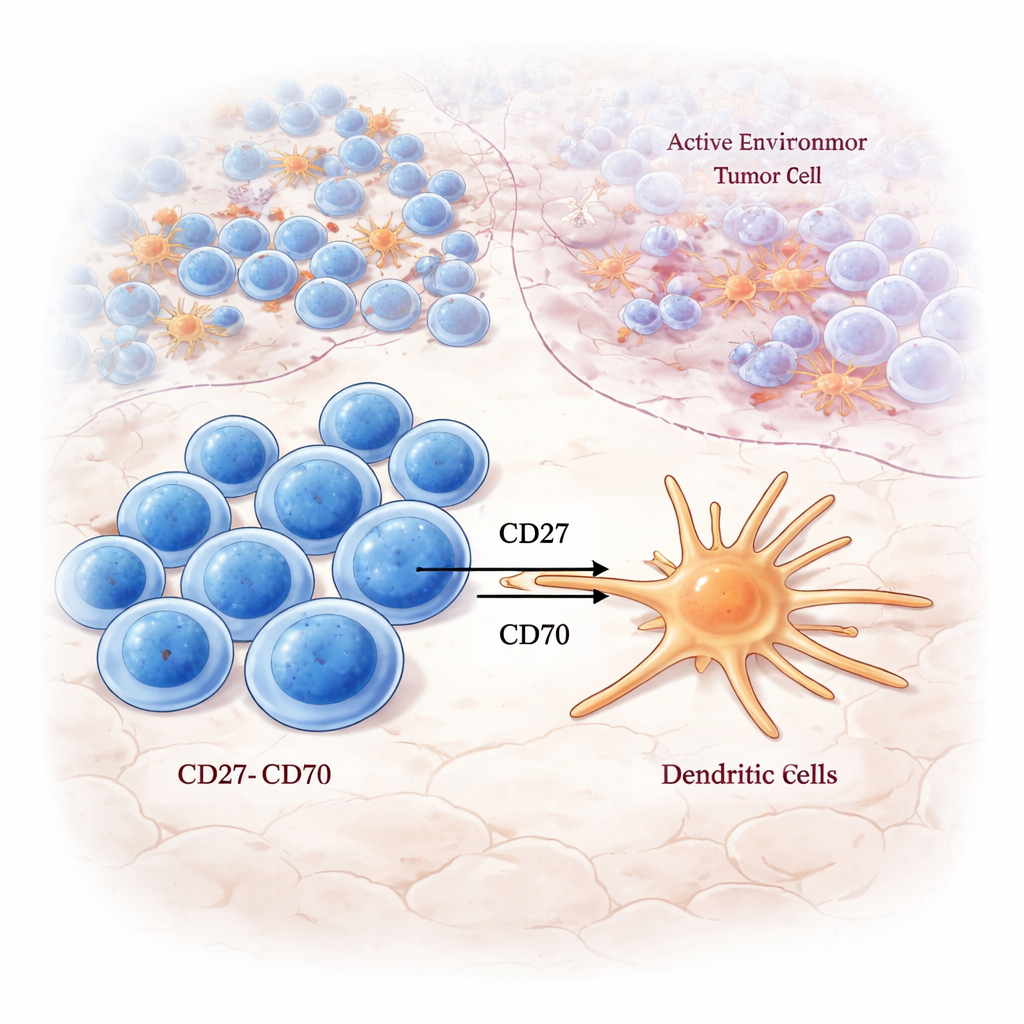
Wo naive T‑Zellen lernen zu kämpfen
Bei genauerer Betrachtung der LAR zeigten sich starke Aktivitäten in Signalwegen, die zentral für das Aktivieren von T‑Zellen sind: T‑Zell-Rezeptor-Signalisierung, Kostimulationswege und Antigenverarbeitung. Naive CD8‑T‑Zellen – Zellen, die noch nicht vollständig auf einen spezifischen Angriffsziel festgelegt sind – waren besonders mit diesen Aktivierungssignalen innerhalb der LAR verknüpft, aber nicht anderswo. Mittels mehrfarbiger Färbungen entdeckten die Autoren CD8‑T‑Zellen in der LAR, die Marker sowohl für Erneuerung als auch für Proliferation trugen, was darauf hindeutet, dass diese Region als lokaler Trainings- und Expansionsort dient, an dem frische, tumorbekämpfende Zellen herangebildet werden.
Zwei Ausprägungen der Immun-Nachbarschaft
Nicht alle LARs waren gleich. Als die Forschenden Patienten nach der zellulären Zusammensetzung ihrer LARs gruppierten, zeigten sich zwei Muster. In „Gruppe A“-Tumoren ähnelten die LARs klassischen Lymphknoten, reich an spezialisierten B‑Zellen und dendritischen Zellen, und die angrenzenden Krebsregionen waren mit aktivierten, kampfbereiten Lymphozyten gefüllt. In „Gruppe B“ waren die LARs weniger entwickelt, und das angrenzende Tumorgewebe enthielt mehr ruhende, weniger engagierte T‑Zellen. Fortgeschrittene computationale Analysen von Gewebebildern bestätigten, dass aktivierte Immunzellen physisch in der Nähe dieser reiferen LARs gehäuft auftraten, was darauf hindeutet, dass die lokale Architektur steuern kann, wie intensiv das Immunsystem den Tumor angreift.
Checkpoint‑Signale im Raum
Die Studie verfolgte außerdem, wo Immun‑„Schalter“ bekannt als Checkpoint‑Moleküle exprimiert werden. Stimulatore Paare wie CD27–CD70 konzentrierten sich in der LAR, insbesondere in Tumoren der Gruppe A, und verbanden erschöpfte, aber tumorreagierende CD8‑T‑Zellen mit dendritischen Zellen, die ihre Aktivität weiter steigern könnten. Im Gegensatz dazu waren viele inhibitorische Checkpoint‑Paare, wie TIGIT–NECTIN2 und LAG3–LGALS3, in der NCR, der krebsintensivsten Zone, angereichert. Das legt nahe, dass selbst wenn die T‑Zell‑Rezeptor‑Signalgebung vorhanden ist, die umgebende Checkpoint‑Landschaft die lokale Immunität je nach Tumorregion in Richtung Angriff oder Unterdrückung kippen kann.
Was das für Patienten bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: Wo Immunzellen und Signale innerhalb eines Tumors lokalisiert sind, kann ebenso entscheidend sein wie ihre Anzahl. Diese Arbeit zeigt, dass Magenkrebse unterschiedliche Immun‑Nachbarschaften enthalten und dass robuste, lymphknotenähnliche Regionen in Tumornähe mit aktiveren, besser positionierten T‑Zellen und günstigeren Verläufen verbunden sind. Indem man lernt, diese lymphozyten‑aggregierten Regionen zu erkennen und möglicherweise zu stärken, könnten künftige Therapien besser zugeschnitten werden — durch die Auswahl von Wirkstoffen, Kombinationen oder sogar gezielten Abgabeansätzen, die die internen immunologischen Stützpunkte des Tumors nutzen.
Zitation: Gao, S., Qin, S., Wang, D. et al. A spatially resolved atlas of gastric cancer characterises a lymphocyte-aggregated region. Nat Commun 17, 2059 (2026). https://doi.org/10.1038/s41467-026-68612-z
Schlüsselwörter: Magenkrebs, Tumormikroumgebung, tertiäre lymphoide Strukturen, räumliche Transkriptomik, Krebsimmuntherapie