Clear Sky Science · de
Divergente Alterung von nulliparen und paren Mammadrüsen offenbart IL33+ hybride Epithelzellen
Wie Schwangerschaft das lebenslange Brustkrebsrisiko umgestalten kann
Warum senkt eine frühe Geburt das lebenslange Brustkrebsrisiko einer Frau, während das schlichte Älterwerden es erhöht? Diese Studie nutzt Mäuse, um das zelluläre „Ökosystem“ der Brust im Zeitverlauf zu untersuchen und Tiere, die nie trächtig waren, mit solchen zu vergleichen, die Nachwuchs hatten. Indem die Forschenden verfolgen, wie sich einzelne Zellen mit Alter und Fortpflanzung verändern, entdecken sie einen seltenen, formwandelnden Zelltyp, der zur Erklärung beitragen könnte, warum Schwangerschaft langanhaltenden Schutz vor Brustkrebs vermittelt.
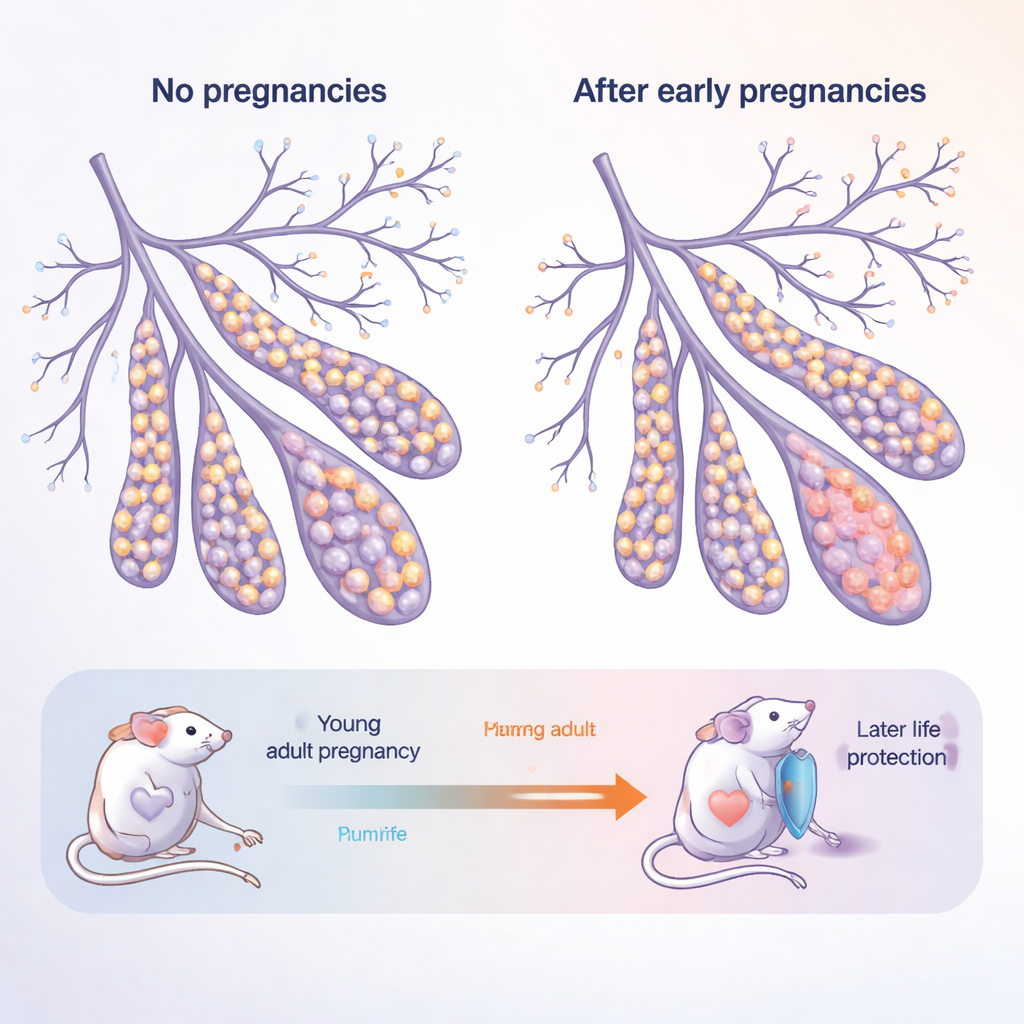
Die Brust als lebendes, sich veränderndes Gewebe
Die Mammadrüse ist kein statisches Organ: Sie wächst und remodelliert sich dramatisch in der Pubertät, während der Schwangerschaft und erneut nach dem Ende der Milchproduktion. Sie besteht aus zwei Hauptschichten von Epithelzellen, die die Gänge auskleiden: inneren „luminalen“ Zellen, die mit Milch und Hormonen in Kontakt stehen, und äußeren „basalen“ Zellen, die Struktur liefern und Stammzell‑ähnliche Zellen beherbergen. Die Autor:innen untersuchten junge adulte Mäuse und ältere, „postmenopausale“ Mäuse, jeweils entweder nie trächtig (nullipar) oder mehrfach trächtig gewesen (par). Dieses Design ahmt eine Frau nach, die in ihren Zwanzigern entbindet und dann in ihre Fünfziger und darüber hinaus altert.
Wie Altern und Schwangerschaft das Gewebe in unterschiedliche Richtungen ziehen
Als Mäuse mit zunehmendem Alter nie trächtig waren, verschob sich ihre Mammadrüse zugunsten eines höheren Anteils an basalen Zellen und weniger luminalen Zellen. Diese älteren, nie‑trächtigen Drüsen produzierten außerdem deutlich mehr Organoide—miniaturisierte 3D‑Strukturen, die aus einzelnen Zellen gezüchtet werden—was darauf hindeutet, dass ihre Zellen ungewöhnlich proliferationsbereit waren. Im Gegensatz dazu zeigten Mäuse, die Schwangerschaften durchlaufen hatten, eine „normalisierte“ Balance: der altersbedingte Anstieg basaler Zellen war abgeschwächt und ihre Zellen bildeten weniger Organoide. Das deutet darauf hin, dass Schwangerschaft eine bleibende Spur hinterlässt, die sowohl die Zelldifferenzierungsentscheidungen verändert als auch das regenerative und potenziell krebsanfällige Potenzial eindämmt.
Die Entdeckung hybrider, formwandelnder Zellen
Um tiefer zu blicken, nutzte das Team Einzelzell‑RNA‑Sequenzierung, um bei Tausenden einzelner Mammazellen abzulesen, welche Gene aktiv sind. Neben den erwarteten luminalen, basalen, Immun‑ und stromalen Zellen fanden sie eine seltene Gruppe, die sich nicht klar einer der beiden Hauptschichten zuordnen ließ. Diese Zellen exprimierten Marker sowohl der luminalen als auch der basalen Linien und erhielten daher den Namen „hybride“ Epithelzellen. Auffällig war, dass diese Hybriden mit dem Alter in nie‑trächtigen Mäusen zunahmen, in gleich alten Mäusen mit Schwangerschaftserfahrung jedoch viel seltener vorkamen. Die Hybriden exprimierten stark ein Gen namens Il33, das das Signalmolekül IL‑33 codiert, zusammen mit Markern, die mit frühen Entwicklungsstadien und hoher Plastizität verknüpft sind—also der Fähigkeit, Identität oder Verhalten zu wechseln.
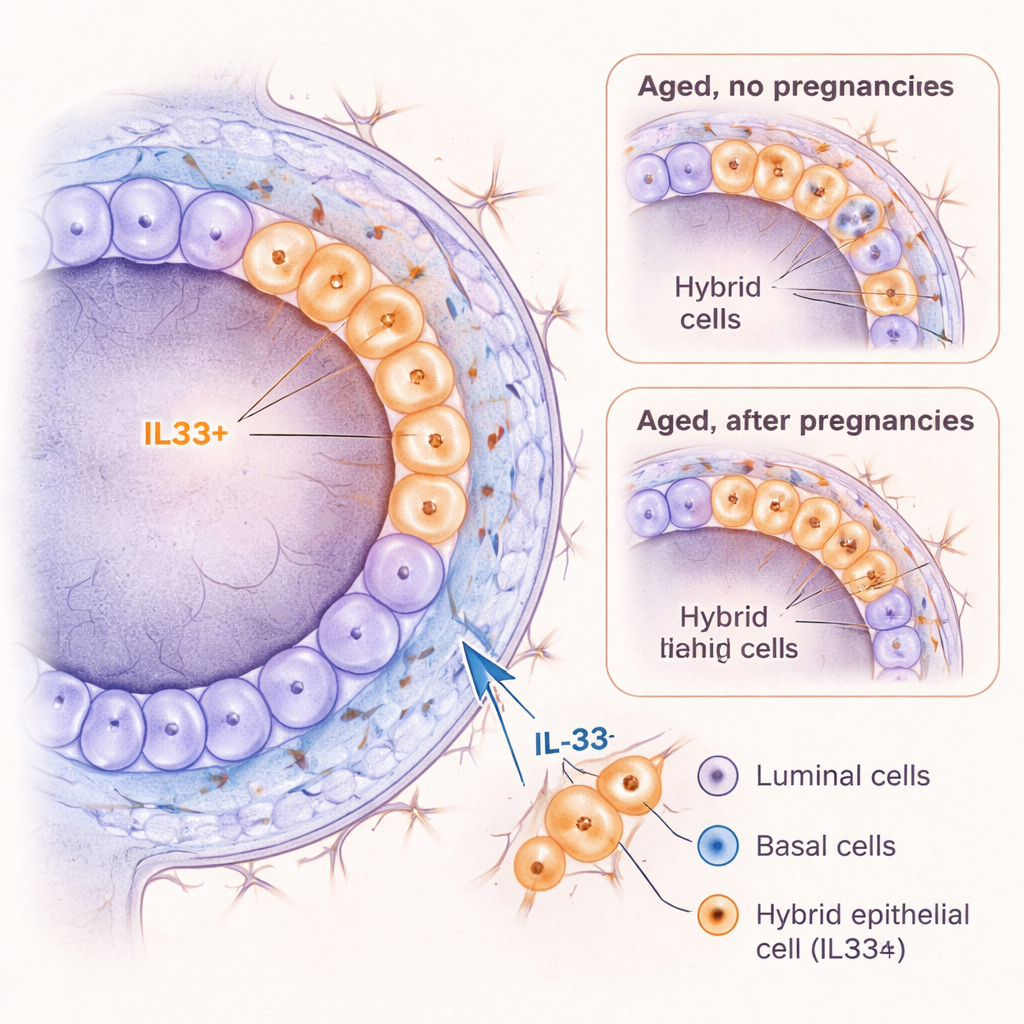
IL‑33 als Treiber riskanter Zellzustände
Da IL‑33 in anderen Organen mit Entzündung und Krebs in Verbindung gebracht wurde, fragten die Forschenden, ob es Mammazellen aktiv in einen hybrid‑ähnlichen Zustand treiben kann. Als sie junge murine Mammazellen in 3D‑Kultur mit IL‑33 behandelten, bildeten Zellen der Basalschicht mehr Organoide, behielten eine primitivere Identität und produzierten mehr Zellen mit dem Hybridmarker KRT6A. In lebenden jungen Mäusen führten kurzfristige IL‑33‑Injektionen dazu, dass sich die Gänge weiteten und eine Teilungswelle ausgelöst wurde, begleitet von einem temporären Anstieg KRT6A‑positiver Hybridzellen und einer Verschiebung hin zu mehr basal‑ähnlichen Zellen. Wichtig ist, dass IL‑33 das Wachstum von Zellen mit einer krebsspezifischen Mutation (Verlust des Tumorsuppressorgens Trp53) zusätzlich förderte. Zusammengenommen deuten diese Befunde darauf hin, dass IL‑33 einen plastischen, proliferativen Zellzustand fördert, der besonders verwundbar für eine kanzeröse Transformation sein könnte.
Anhaltspunkte aus menschlichem Brustgewebe
Um zu prüfen, ob ähnliche Zellen beim Menschen existieren, analysierten die Autor:innen mehrere große Einzelzell‑Datensätze aus normalem menschlichem Brustgewebe neu. Sie identifizierten eine kleine Population menschlicher Epithelzellen, die wie die Maus‑Hybriden sowohl luminale als auch basale Merkmale zeigten und IL33 sowie verwandte Gene exprimierten. IL33‑positive Zellen wurden in mehreren Datensätzen mit dem Alter häufiger. In primären humanen Mammazellen, die im Labor kultiviert wurden, erhöhte IL‑33 die Organoidbildung, verschob die Zellen zu einem basal‑ähnlichen Profil und reicherte CD44‑positive Zellen an—einen Marker, der oft mit unreifen, stammzellähnlichen Zellen im Brustkrebs assoziiert ist. Obwohl die verfügbaren Humanproben keinen sauberen Test erlaubten, wie frühe Schwangerschaft diese Population verändert, sind die Parallelen zu den Mäusen auffällig.
Was das für das Verständnis des Brustkrebsschutzes bedeutet
Für Lesende ohne Fachhintergrund lautet die zentrale Botschaft: Schwangerschaft scheint die Art und Weise, wie Brustgewebe altert, neu zu verdrahten. Bei Mäusen verhindert eine frühe Schwangerschaft das Ansammeln von IL‑33‑reichen Hybridzellen, die die Grenze zwischen den Hauptzellschichten der Brust verwischen und sich sehr flexibel und wachstumsbereit verhalten. IL‑33 selbst kann Zellen in diesen riskanten, formwandelnden Zustand drängen, besonders wenn krebsspezifische Mutationen vorliegen. Indem Schwangerschaft die Anzahl oder Persistenz dieser Hybridzellen reduziert, könnte sie die Wahrscheinlichkeit senken, dass im alternden Brustgewebe zur falschen Zeit die falsche Zelle vorhanden ist—eine, die kurz davorsteht, in Krebs überzugehen. Dieser mechanistische Einblick könnte künftig Strategien anleiten, die den schützenden Effekt einer frühen Schwangerschaft nachahmen, ohne dass eine Schwangerschaft erforderlich wäre.
Zitation: Olander, A., Medina, P., Haro Acosta, V. et al. Divergent aging of nulliparous and parous mammary glands reveals IL33+ hybrid epithelial cells. Nat Commun 17, 1898 (2026). https://doi.org/10.1038/s41467-026-68611-0
Schlüsselwörter: Brustalterung, Schwangerschaft und Brustkrebs, Mammäre Stammzellen, IL-33-Signalgebung, hybride Epithelzellen