Clear Sky Science · de
ZFP57 ist ein Regulator des postnatalen Wachstums und der lebenslangen Gesundheit
Wie frühe Milch die lebenslange Gesundheit prägt
Was sich in den ersten Lebenstagen abspielt, kann noch Jahrzehnte nachhallen. Diese Studie zeigt, dass ein einzelnes maternales Protein, genannt ZFP57, mitbestimmt, wie gut sich die Mammadrüse entwickelt, was in die Muttermilch gelangt und wie die Nachkommen wachsen und über die Lebenszeit mit Energie umgehen. Indem die Forschenden den Einfluss dieses Proteins von der trächtigen Mutter bis zu den säugenden Jungen zurückverfolgen, offenbaren sie eine verborgene genetische Ebene unterhalb der bekannten Vorteile früher Ernährung.
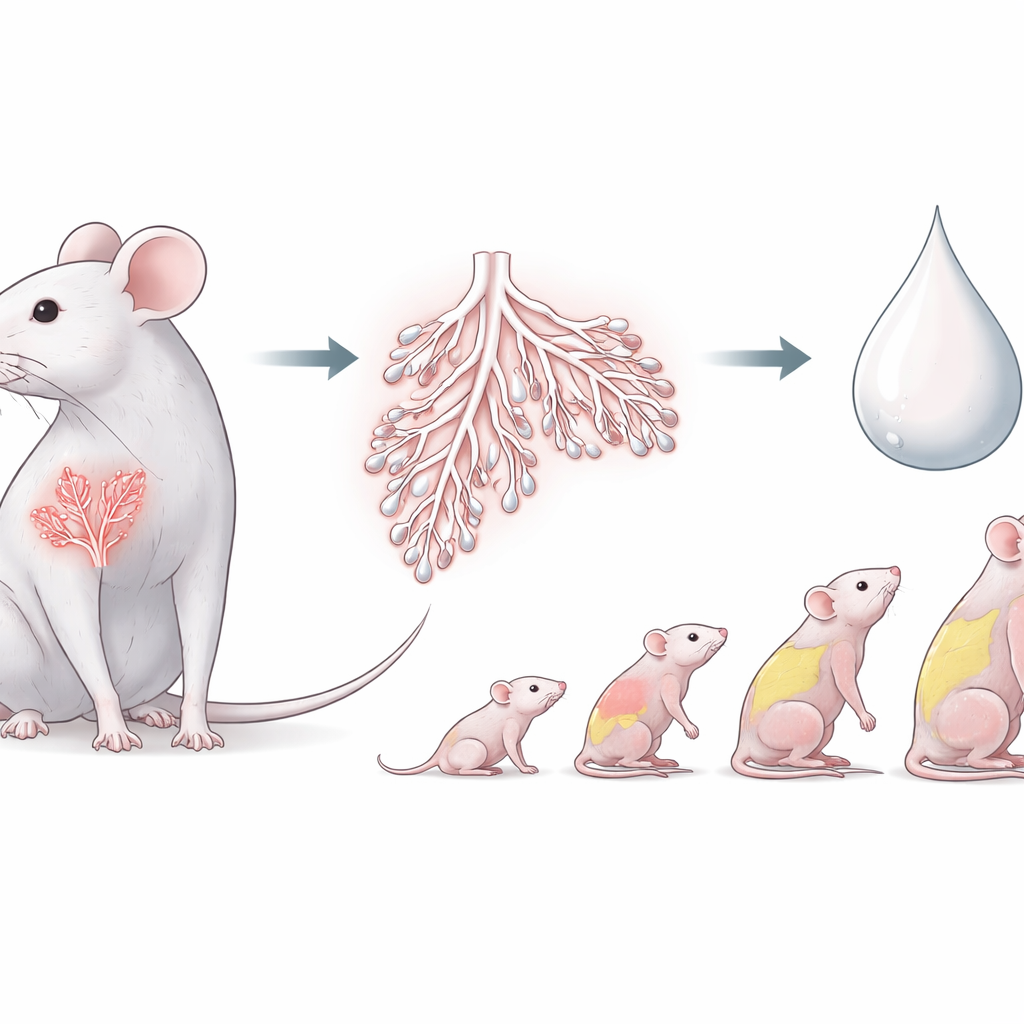
Ein Wächter des Wachstums vor und nach der Geburt
ZFP57 war bereits als zentraler Regulator der „genomischen Prägung“ bekannt, eines chemischen Markierungssystems, das bestimmten Genen sagt, ob sie von der Mutter oder dem Vater stammen. Diese Markierungen sind entscheidend für normales Wachstum vor der Geburt. Die neue Arbeit stellt die Frage, ob ZFP57 auch später wichtig ist, nach der Geburt, wenn Mütter ihre Jungen über Milch versorgen. An Mäusen zeigten die Autorinnen und Autoren, dass ZFP57 nicht nur in Embryonen und der Plazenta aktiv ist, sondern auch in adulten Geweben, einschließlich Gehirn und Mammadrüse. Das legt nahe, dass dasselbe Molekül, das das fetale Wachstum mitsteuert, auch die postnatale Ernährung beeinflussen kann.
Wie die Brustdrüse der Mutter auf das Stillen vorbereitet ist
Das Team untersuchte Mammadrüsen von normalen und Zfp57-defizienten Weibchen über Schlüsselphasen hinweg: vor der Schwangerschaft, während der Gestation und in der frühen Laktation. Sie sortierten verschiedene Zelltypen und bestimmten die Aktivitätsniveaus von Tausenden Genen. Während die grobe Drüsenentwicklung weiterhin stattfand, waren die feinen Details gestört, wenn ZFP57 fehlte. Vor der Schwangerschaft zeigten die Mutanten ungewöhnlich dichte Verzweigungen und eine vorzeitige Aktivierung von Genen, die normalerweise erst später zur Vorbereitung der Milchproduktion eingeschaltet werden. Während der Gestation kehrte sich das Muster um: Verzweigungen und milchbezogene Genaktivität nahmen ab und viele Zellen durchliefen programmierte Zelltodeswege. Diese Veränderungen störten das Gleichgewicht der Zelltypen, die ein gesundes milchproduzierendes Organ aufbauen und erhalten.
Milchqualität, Wachstumsverläufe und mismatched Mütter
Diese strukturellen und molekularen Verschiebungen äußerten sich in veränderter Milch und veränderten Jungen. Zfp57-defiziente Mütter produzierten Milch mit höheren Anteilen oxidierter Fette und niedrigeren Gehalten bestimmter Phospholipide, die helfen, Lipide in Tröpfchen zu verpacken. Von solchen Müttern gesäubte Jungen wuchsen anfangs langsamer, und manche gediehen nicht. Doch eine Gruppe von Nachkommen, die eine spezifische Zfp57-Mutation trug und in Zfp57-defizienten Mutterleibern herangewachsen war, reagierte sehr anders: Trotz früher Saugprobleme und verzögerter sichtbarer Milchaufnahme nahmen sie während der Laktation übermäßig zu. Kreuzpflegungs-Experimente, bei denen Neugeborene zwischen Müttern unterschiedlicher Genotypen ausgetauscht wurden, zeigten, dass das Wachstum am besten war, wenn der genetische Hintergrund der säugenden Mutter zu den Bedingungen passte, die im Mutterleib bestanden. Wurden Junge, die an eine mütterliche Umgebung angepasst waren, von einer genetisch anderen Mutter gesäugt, wurden ihr Wachstum und ihr Stoffwechsel oft in extreme Richtungen gedrängt.
Von früher Ernährung zum Stoffwechsel im Erwachsenenalter
Die Geschichte endete nicht beim Absetzen. Die Forschenden verfolgten Mäuse sechs Monate lang, was etwa dem frühen Erwachsenenalter beim Menschen entspricht. Nachkommen, die in Zfp57-defizienten Müttern entwickelt wurden und selbst die veränderte Zfp57-Kopie trugen, zeigten anhaltende Veränderungen: mehr Körperfett, weniger fettfreie Masse und eine stärkere Abhängigkeit davon, Fett statt Kohlenhydrate zu verbrennen, selbst bei gleicher Standarddiät wie die Kontrollen. Einige entfernten Zucker aus dem Blut weniger effizient, ein Kennzeichen schlechter Glukosetoleranz, das mit dem metabolischen Syndrom verknüpft ist. Bemerkenswerterweise waren diese langfristigen Probleme am stärksten, wenn solche Jungen zur Pflege bei normalen Müttern gegeben worden waren, was hervorhebt, wie eine Diskrepanz zwischen pränataler Umgebung und postnataler Ernährung ungesunde Bahnen verfestigen kann.
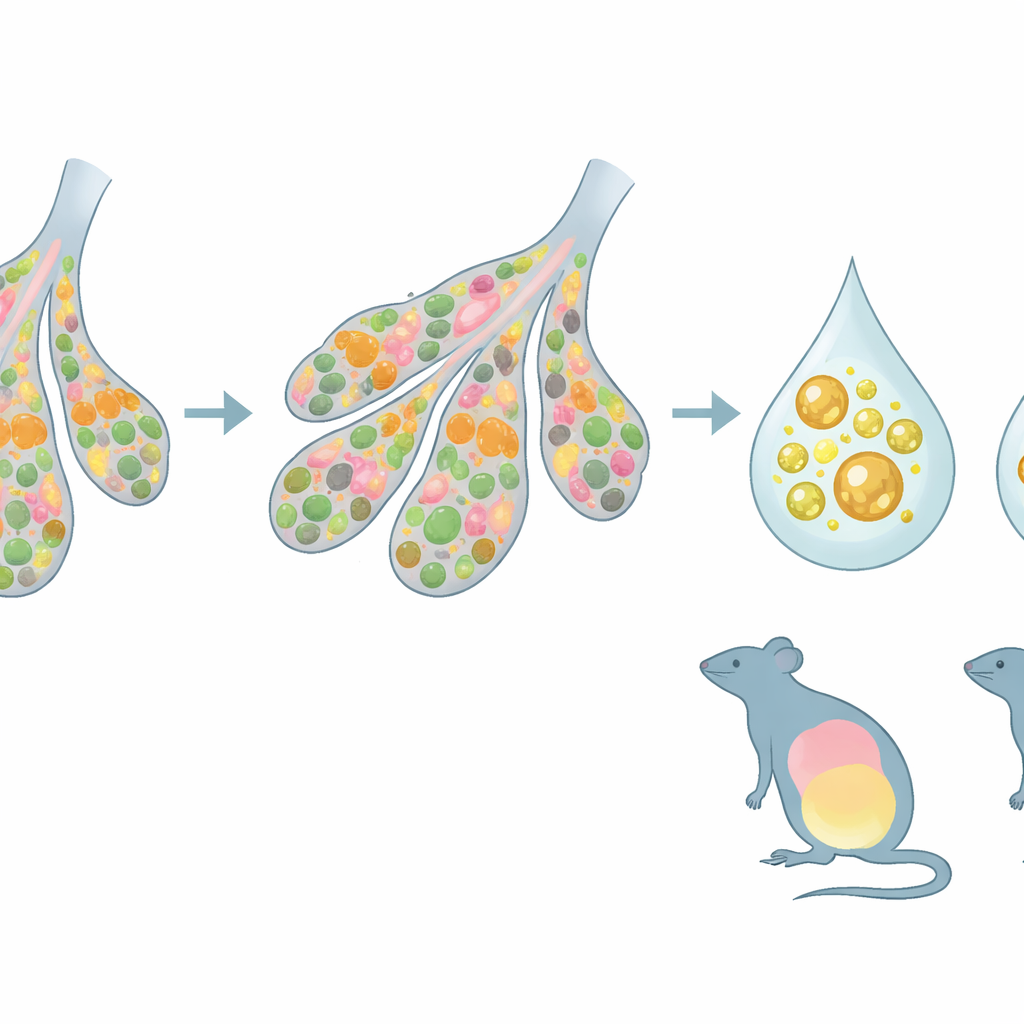
Warum das für die menschliche Gesundheit wichtig ist
Indem diese Arbeit eine Rolle für ZFP57 bei der Gestaltung der Funktion der Mammadrüse und der Milchzusammensetzung enthüllt — unabhängig von seinen klassischen Prägungsaufgaben — verknüpft sie ein maternales Gen mit der Kontrolle von Ressourcen vor und nach der Geburt. Sie stützt die Idee, dass Mütter und Nachkommen genetisch aufeinander abgestimmt sind: Die Gebärmutterumgebung und die Milchversorgung sind aufeinander zugeschnitten, und das Zerbrechen dieser Übereinstimmung kann dauerhafte Kosten nach sich ziehen. Obwohl die Studie an Mäusen durchgeführt wurde, ist ZFP57 auch beim Menschen wichtig, wo Mutationen mit Problemen des frühen Stoffwechsels in Verbindung gebracht werden. Die Befunde legen nahe, dass einige lebenslange Risiken für Fettleibigkeit und Diabetes nicht nur aus der Ernährung selbst entstehen, sondern daraus, wie unsere Gene die frühe Ernährung konfigurieren und wie gut prä- und postnatale Umgebungen aufeinander abgestimmt sind.
Zitation: Hanin, G., AlSulaiti, B., Costello, K.R. et al. ZFP57 is a regulator of postnatal growth and life-long health. Nat Commun 17, 2080 (2026). https://doi.org/10.1038/s41467-026-68608-9
Schlüsselwörter: Ernährung im frühen Leben, Epigenetik, Mammadrüse, metabolische Gesundheit, genomische Prägung