Clear Sky Science · de
Erweiterung der Wirkstoffpalette bei Antikörper-Wirkstoff-Konjugaten durch Abgabe von hydroxylierten Wirkstoffen über selbstimmolative Phosphoramidate
Schlauere Lenkwaffen gegen Krebs
Krebsmedikamente können außerordentlich wirksam sein, verhalten sich aber oft wie Teppichbombardement: Sie treffen gesundes Gewebe fast genauso stark wie Tumore. Antikörper–Wirkstoff-Konjugate (ADCs) wurden entwickelt, um dieses Problem zu lösen, indem ein potentes Medikament an einen Antikörper gebunden wird, der gezielt Krebszellen ansteuert — so wird die Behandlung zur Lenkwaffe. Dieser Artikel beschreibt einen neuen chemischen »Stecker« zwischen Antikörper und Wirkstoff, der diese Lenkwaffen präziser und flexibler macht und damit den Einsatz vieler weiterer Krebswirkstoffe ermöglicht, die heutige ADCs nicht transportieren können.
Warum heutige zielgerichtete Wirkstoffe noch begrenzt sind
ADCs bestehen aus drei Teilen: einem Antikörper, der ein Merkmal auf Krebszellen erkennt, einem giftigen Wirkstoff (der »Payload«) und einem chemischen Linker, der beides verbindet. Die meisten zugelassenen ADCs verwenden nur einige wenige Arten von Payloads, die DNA schädigen oder die Zellteilung auf ähnliche Weise blockieren. Ein Hauptgrund ist der Linker: Er muss den Wirkstoff während der Zirkulation im Blut fest halten und ihn erst nach Aufnahme in die Tumorzelle sauber freigeben. Bestehende Linker funktionieren gut nur mit bestimmten chemischen Gruppen an Wirkstoffen, insbesondere Aminen, und tun sich oft schwer mit vielen Medikamenten, die Alkoholgruppen (–OH) enthalten. Dadurch bleiben zahlreiche vielversprechende Krebswirkstoffe ungenutzt, weil sie sich mit aktuellen ADC-Designs nicht sicher oder effizient liefern lassen.
Ein Trick aus antiviralen Medikamenten übernehmen
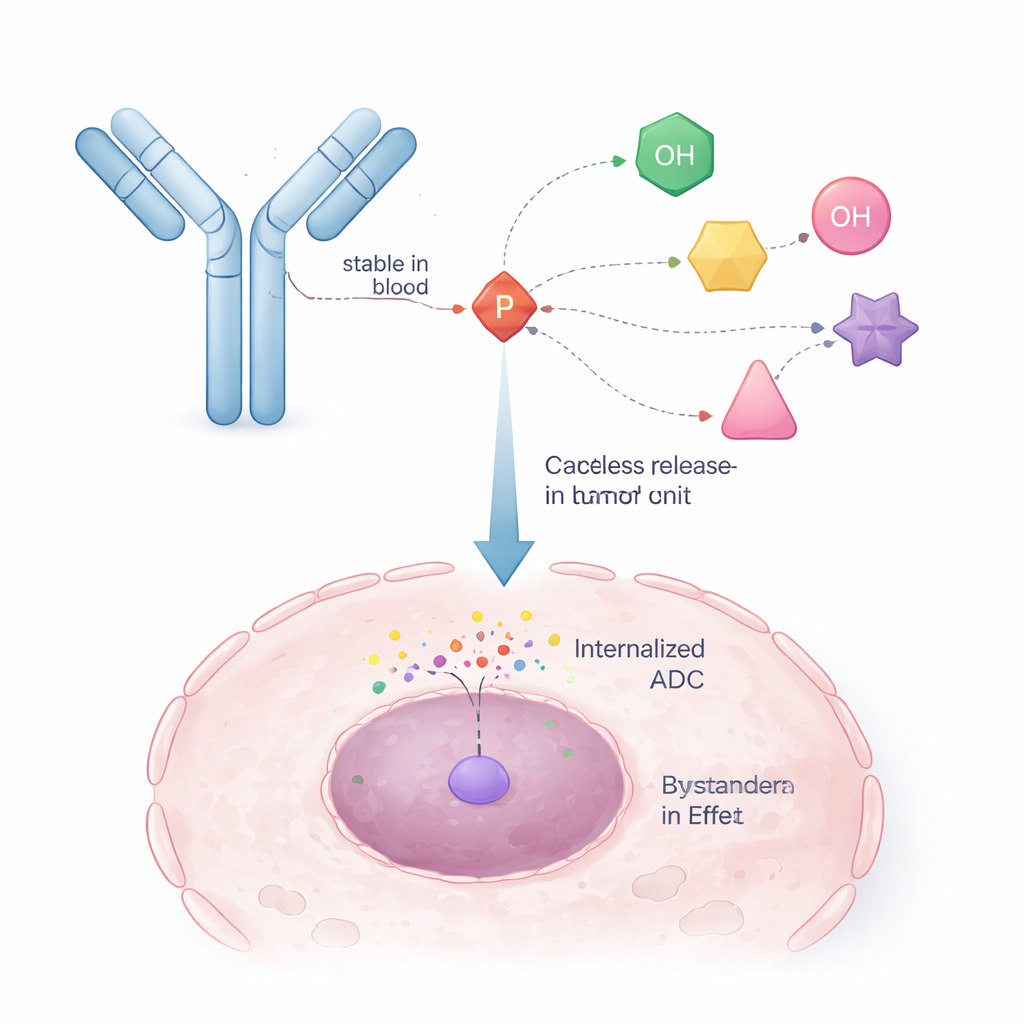
Die Forschenden griffen zu einer Strategie, die sich bereits in antiviralen Arzneien bewährt hat: den ProTide-Ansatz. Bei diesen Medikamenten maskiert eine phosphorhaltige chemische Einheit vorübergehend eine geladene Phosphatgruppe, sodass das Molekül in Zellen gelangen kann und sich erst dort wieder in seine aktive Form verwandelt. Die Autorinnen und Autoren überarbeiteten dieses Konzept so, dass ein Arm des Phosphorkerns an den Antikörper bindet, während die anderen Arme das Krebsmedikament tragen. So entsteht ein »selbstimmolativer« Linker: Sobald ein innerer Auslöser (etwa ein Enzym in der Tumorzelle) einen kleinen Teil der Struktur abschneidet, kollabiert die Phosphoreinheit kontrolliert und setzt das ursprüngliche Wirkstoffmolekül mit wiederhergestellter, unveränderter Alkoholgruppe frei.
Entwicklung eines vielseitigen chemischen Steckers
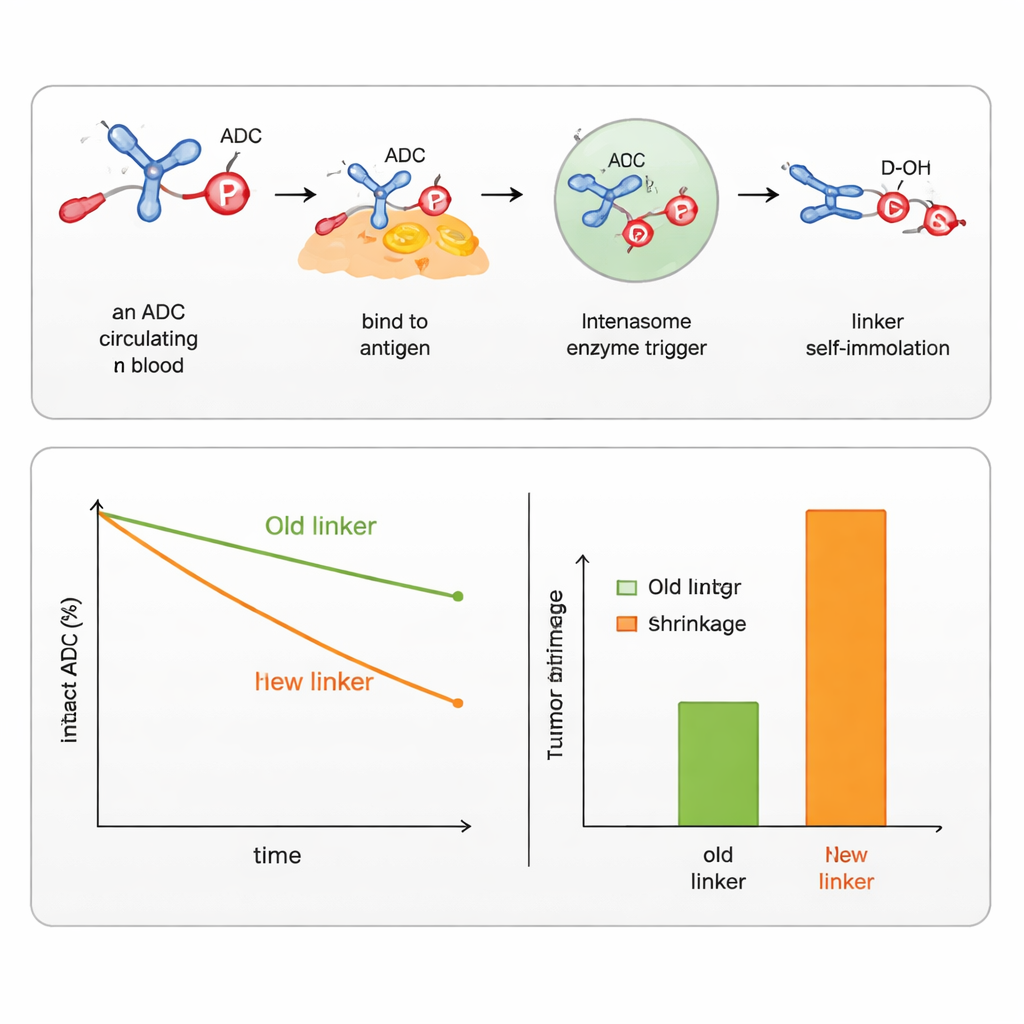
Das Team zeigte, dass sich durch Abstimmung der Gruppen um das Phosphoratom die Stabilität des Linkers im Blut und die Geschwindigkeit seines Zerfalls in Zellen feinjustieren lassen. Sie entwarfen Varianten, die auf mehrere in Tumorzellen häufig vorkommende Auslöser reagieren, darunter Esterasen und Proteasen (Enzyme, die bestimmte Bindungen schneiden), sowie Enzyme, die Zuckergruppen erkennen, oder reduzierte Bedingungen in Zellkompartimenten. Mit diesen Designs gelang es ihnen, sowohl aromatische Alkohole (wie das Chemotherapeutikum SN38) als auch aliphatische Alkohole (wie DXd, der Payload in einem zugelassenen Brustkrebs‑ADC) anzubringen und freizusetzen. Im direkten Vergleich mit kommerziellen Linkern für SN38 und DXd hielten die neuen Phosphoramidat‑Linker die Wirkstoffe länger im Serum gebunden, lieferten mehr Wirkstoff in Tumoren und erzielten stärkere Tumorverkleinerungen bei Mäusen, während die Schädigung gesunden Gewebes geringer ausfiel.
Viele neue Krebswirkstoff‑Payloads erschließbar
Um die Breite der Anwendbarkeit zu testen, bauten die Forschenden ADCs mit zehn verschiedenen Wirkstoffen, die alle mindestens eine –OH‑Gruppe besitzen, aber im Tumor sehr unterschiedlich wirken. Dazu gehörten Inhibitoren der DNA‑Synthese, der Proteinfaltung (HSP90), des Energiestoffwechsels (NAMPT und DHODH) und der Proteintranslation sowie bekannte Wirkstoffe wie Paclitaxel und Gemcitabin. Trotz der großen strukturellen Vielfalt konnten sie einheitliche ADCs mit hoher Wirkstoffbeladung für alle herstellen. In Zellversuchen über verschiedene Krebsarten zeigten die meisten dieser ADCs Nanomolar- oder sogar sub‑Nanomolar‑Wirkstärken und eine deutliche Selektivität für Zellen, die das Antikörperziel exprimieren, was bestätigt, dass der Linker zuverlässig aktiven Wirkstoff in den richtigen Zellen freisetzt.
Gemcitabin als Demonstrationsbeispiel
Gemcitabin ist eine weitverbreitete Chemotherapie, wird in konventioneller Form aber so schnell aus dem Körper eliminiert, dass Patientinnen und Patienten hohe wiederholte Dosen erhalten müssen, was die sicher verabreichbare Menge begrenzt. Mit dem Phosphoramidat‑Linker befestigten die Autorinnen und Autoren Gemcitabin an einen HER2‑bindenden Antikörper an zwei verschiedenen Alkoholpositionen und zeigten, dass beide Varianten ihre volle Aktivität wiedererlangen, sobald sie in Krebszellen gelangen. In Mausmodellen mit HER2‑positiven Tumoren führte eine einzelne Dosis des Gemcitabin‑ADCs — mit etwa tausendfach geringerer Gesamtmenge an Gemcitabin als bei typischen Freiwirkstoff‑Regimen — zu starker und selektiver Tumorkontrolle. Das Verhalten des ADCs im Blut entsprach weitgehend dem des nackten Antikörpers, und hohe Dosen wurden in Ratten gut toleriert, was auf einen breiten Sicherheitsabstand hindeutet.
Was das für die künftige Krebstherapie bedeutet
Für Nicht‑Fachleute lautet die Kernbotschaft: Diese Arbeit liefert einen neuen, sehr anpassungsfähigen chemischen Verbinder, der es Antikörpern erlaubt, eine wesentlich größere Bandbreite von Krebswirkstoffen zu transportieren — und das sicherer. Indem sichergestellt wird, dass Wirkstoffe während der Zirkulation befestigt bleiben und erst nach Aufnahme in die Tumorzelle sauber freigesetzt werden, erhöhen Phosphoramidat‑Linker die Menge an Wirkstoff, die den Tumor erreicht, und verringern Kollateralschäden am gesunden Gewebe. Ebenso wichtig: Sie ermöglichen es, bereits potente kleinmolekulare Wirkstoffe mit sehr unterschiedlichen Formen und Wirkmechanismen als zielgerichtete Therapien neu zu nutzen. Das könnte die Auswahl an verfügbaren ADCs für Patientinnen und Patienten stark erweitern und helfen, Tumore zu bekämpfen, die gegen das heutige begrenzte Payload‑Spektrum resistent geworden sind.
Zitation: Ochtrop, P., Jagtap, A.P., Felber, J.G. et al. Expanding the payload scope in antibody-drug conjugates by delivery of hydroxy-containing drugs through self-immolative phosphoramidates. Nat Commun 17, 759 (2026). https://doi.org/10.1038/s41467-026-68605-y
Schlüsselwörter: Antikörper–Wirkstoff-Konjugate, Krebsmedikamenten‑Transport, selbstimmolative Linker, Phosphoramidat‑Chemie, gezielte Chemotherapie