Clear Sky Science · de
Ligandgesteuerte regiodivergente und enantioselektive C–H‑Cyanierung sekundärer Amine
Warum das Ändern winziger Bindungen für große Medikamente wichtig ist
Viele Bestseller‑Medikamente enthalten kleine, stickstoffhaltige Bausteine, die als Amine bezeichnet werden. Feine Änderungen in der Art und Weise, wie die Atome um diese Amine herum verknüpft sind, können ein schwaches Medikament in eine sehr wirksame, präzise Therapie verwandeln – oder es in ein inaktives oder sogar schädliches Molekül umwandeln. Dieser Beitrag beschreibt eine neue Methode, diese Aminbausteine gezielt zu modifizieren, sodass Chemiker genau wählen können, an welcher Stelle des Moleküls reagiert wird und welche spiegelbildliche Form (Enantiomer) entsteht – beides entscheidend für die Entwicklung sichererer und wirksamerer Arzneimittel.
Eine Stelle auf einem dicht gepackten Molekül auswählen
Amine in Wirkstoffen besitzen häufig mehrere sehr ähnliche Kohlenstoff‑Wasserstoff (C–H)‑Bindungen, die sich normalerweise fast gleich verhalten. Chemiker möchten gern genau eines dieser Wasserstoffe gegen eine nützliche Gruppe, etwa eine Cyano‑Gruppe (–CN), austauschen, ohne den Rest des Moleküls zu stören. Das ist schwierig, weil Standardreaktionen dazu neigen, an der reaktivsten Stelle abzulaufen, die die Molekülstruktur vorgibt, und nicht dort, wo der Chemiker es wünscht. Die Autoren arbeiten hier mit einfachen, flexiblen sekundären Aminen, die am Stickstoff zwei unterschiedliche Alkylketten tragen. Sie zeigen, dass sich aus demselben Amin durch Wahl des Liganden am Kupferkatalysator die Reaktion gezielt an eine von zwei benachbarten Positionen lenken lässt – entweder neben einer kleinen N‑Methyl‑Gruppe (die sogenannte α′‑Stelle) oder ein Kohlenstoffatom weiter entfernt an der anderen Kette (die β‑Stelle).
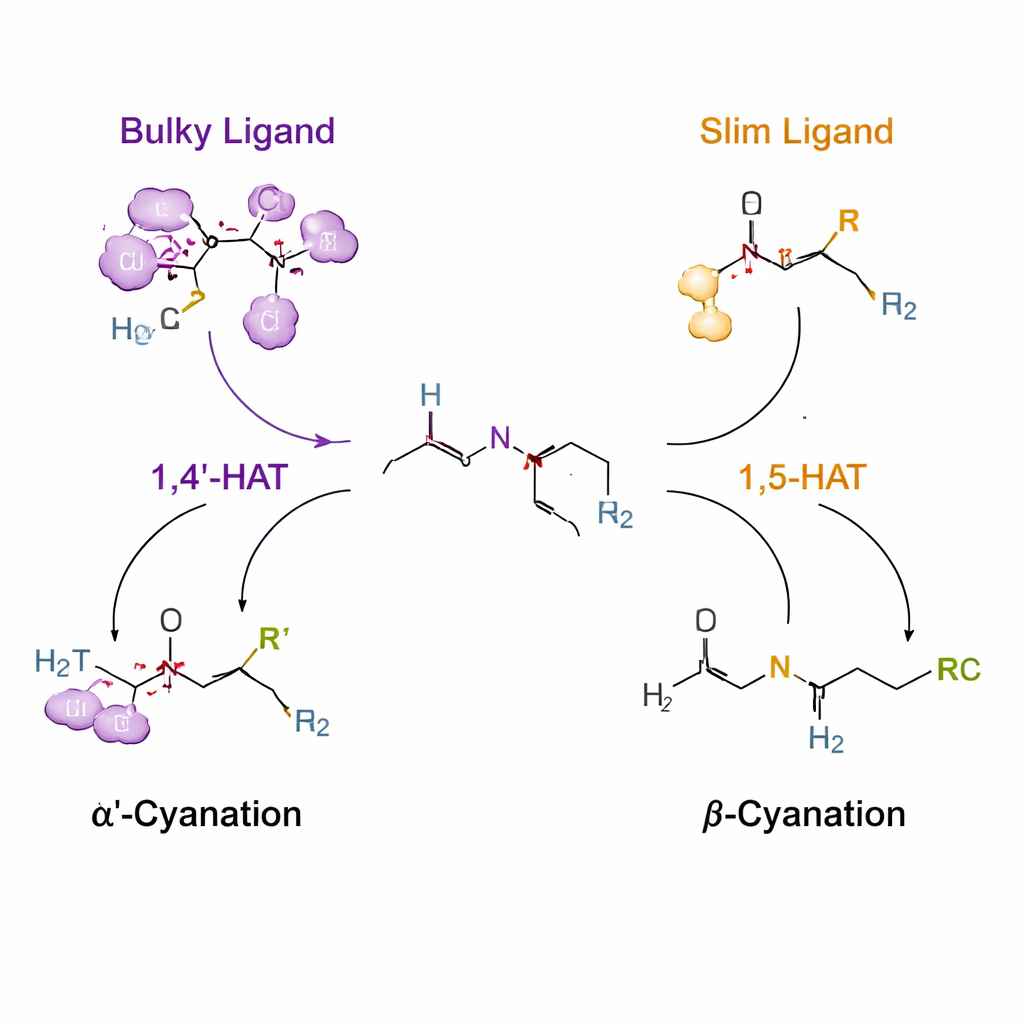
Gesteuerte Wasserstoff‑„Sprünge“ zur Lenkung der Reaktivität
Der Schlüsseltrick beruht auf einem Prozess namens Wasserstoffatomübertragung (HAT), bei dem ein kurzlebiges, am Stickstoff zentriertes Radikal ein Wasserstoffatom von einem benachbarten Kohlenstoff ‚pflückt‘. Solche Radikale bevorzugen normalerweise eine bestimmte Reichweite, wobei ein sechs‑gliedriger „Greifbereich“ (1,5‑HAT) bevorzugt wird. Die Autoren versehen das Amin mit einem temporären Harnstoff‑ und Chlorhandle, sodass unter Kupferkatalyse dieses Stickstoffradikal entsteht und Wasserstoff entweder an der α′‑ oder der β‑Position abstrahieren kann. Durch die Gestaltung der Liganden – organische Moleküle, die das Kupfer umgeben – formen sie die Umgebung des Radikals neu. Ein sehr sperriger Ligand (genannt L14) drängt das System zu einem ungewöhnlichen 1,4′‑HAT‑Schritt, der die N‑Methyl‑Gruppe ins Visier nimmt und eine selektive α′‑Cyanierung liefert. Schlankere Liganden (wie L8) erlauben den konventionellen 1,5‑HAT‑Weg und steuern die Reaktion stattdessen zur β‑Position.
Von Positionskontrolle zur Kontrolle der Händigkeit
Neben der Wahl des Reaktionsorts strebt das Team auch die Kontrolle der Händigkeit (Chiralität) an, was wichtig ist, da viele Wirkstoffe als links‑ und rechtsdrehende Formen existieren, die im Körper unterschiedlich wirken. Dafür führen sie chirale Liganden – also Liganden mit eigener Händigkeit – in das Kupferkomplexsystem ein. Zwei solche Liganden, L24 und L41, erzeugen eine starke Bevorzugung eines Enantiomers, wenn die Reaktion eine Cyano‑Gruppe an β‑Positionen einführt, einschließlich benachbarter Positionen zu aromatischen Ringen (benzylic) und allylischer Positionen (neben C=C‑Bindungen). Über eine breite Palette von Aminausgangsstoffen liefert die Methode β‑cyanierte Produkte mit ausgezeichneter Selektivität sowohl für die Stelle als auch für die Händigkeit und funktioniert auch im Grammmaßstab, was die Praktikabilität und Robustheit für die Synthese zeigt.
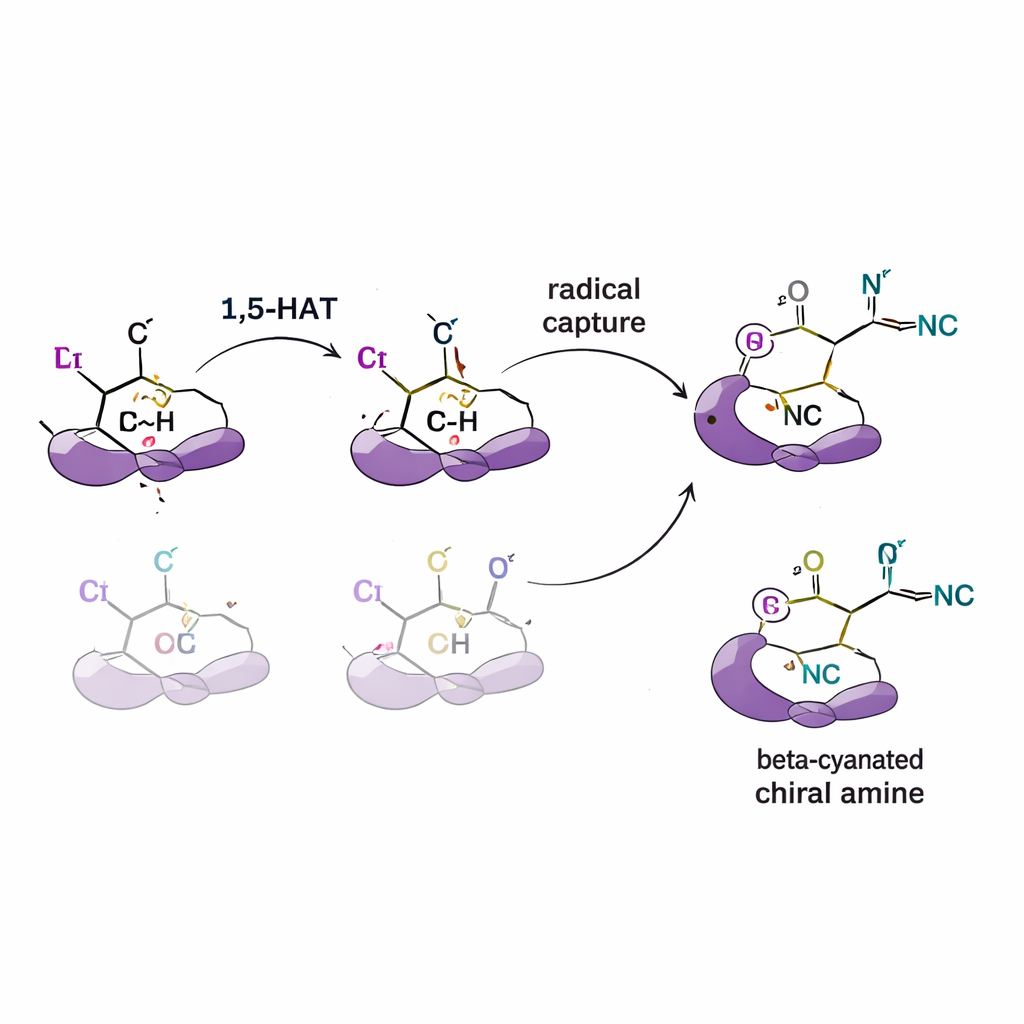
Untersuchung des Mechanismus hinter der Selektivität
Um zu klären, wie diese Kontrolle zustande kommt, führen die Autoren eine Reihe mechanistischer Experimente durch. Durch Zugabe von Radikal‑„Fallen“ bestätigen sie, dass reaktive Radikalzwischenstufen tatsächlich beteiligt sind. Mit Substraten, bei denen bestimmte Wasserstoffe durch Deuterium (eine schwerere Wasserstoffisotop) ersetzt sind, beobachten sie kinetische Isotopeneffekte, die darauf hindeuten, dass der Wasserstoffübertragungsschritt der langsame, die Selektivität bestimmende Schritt ist. Markierungsversuche zeigen außerdem, dass der Wasserstoff in einem einzelnen, gerichteten Schritt bewegt wird und nicht zwischen Positionen hin und her shuttlelt. Ergänzende Computersimulationen (Dichtefunktionaltheorie) stützen diese Befunde und zeigen, dass Form und Sperrigkeit des Liganden die Energien konkurrierender Wasserstoffübertragungswege und die Art beeinflussen, wie das Radikal dann mit Kupfer und Cyanid kombiniert, wodurch ein bevorzugtes Enantiomer entsteht.
Was das für die zukünftige Wirkstoffentwicklung bedeutet
Insgesamt führt diese Arbeit eine flexible Strategie ein, um verbreitete Aminfunktionen an zwei eng verwandten Stellen gezielt und auf Abruf umzubauen, mit feiner Kontrolle über die molekulare Händigkeit. Durch den einfachen Austausch des Liganden an einem Kupferkatalysator können Chemiker wählen, ob eine Cyano‑Gruppe an einer kleinen N‑Methyl‑Einheit oder am benachbarten Kohlenstoff einer anderen Seitenkette platziert wird, und das über viele komplexe, wirkstoffähnliche Moleküle hinweg. Da Cyano‑Gruppen wertvolle Sprungbretter zu vielen anderen Funktionalitäten sind, sollte dieser ‚Dial‑a‑site‘‑ und ‚Dial‑a‑hand‘‑Ansatz das Erkunden und Optimieren neuer Medikamente, die auf denselben grundlegenden Amin‑Skeletten aufgebaut sind, erleichtern.
Zitation: Mao, YJ., Chen, X., Li, HL. et al. Ligand-controlled regiodivergent and enantioselective C–H cyanation of secondary amines. Nat Commun 17, 1869 (2026). https://doi.org/10.1038/s41467-026-68598-8
Schlüsselwörter: Funktionalisierung von Aminen, Wasserstoffatomübertragung, Kupferkatalyse, enantioselektive Cyanierung, medizinische Chemie