Clear Sky Science · de
Duale genomische Lokalisationen und genregulatorische Funktionen von MBD‑2 mit und ohne NuRD in Caenorhabditis elegans, das keine DNA‑Methylierung besitzt
Wie winzige Würmer die Regeln der Genkontrolle neu schreiben
Unsere Zellen nutzen chemische Markierungen an DNA und Proteinen, um sich zu merken, welche Gene ein‑ oder ausgeschaltet sein sollen. Eine der bekanntesten Markierungen, die DNA‑Methylierung, fehlt bei einigen Tieren – dennoch wachsen und vermehren sie sich normal. Diese Studie untersucht, wie ein kleiner Wurm, Caenorhabditis elegans, die Genkontrolle ohne DNA‑Methylierung handhabt und enthüllt ein unerwartet flexibles Ersatzsystem, das unsere Sicht auf die Epigenetik verändern könnte.
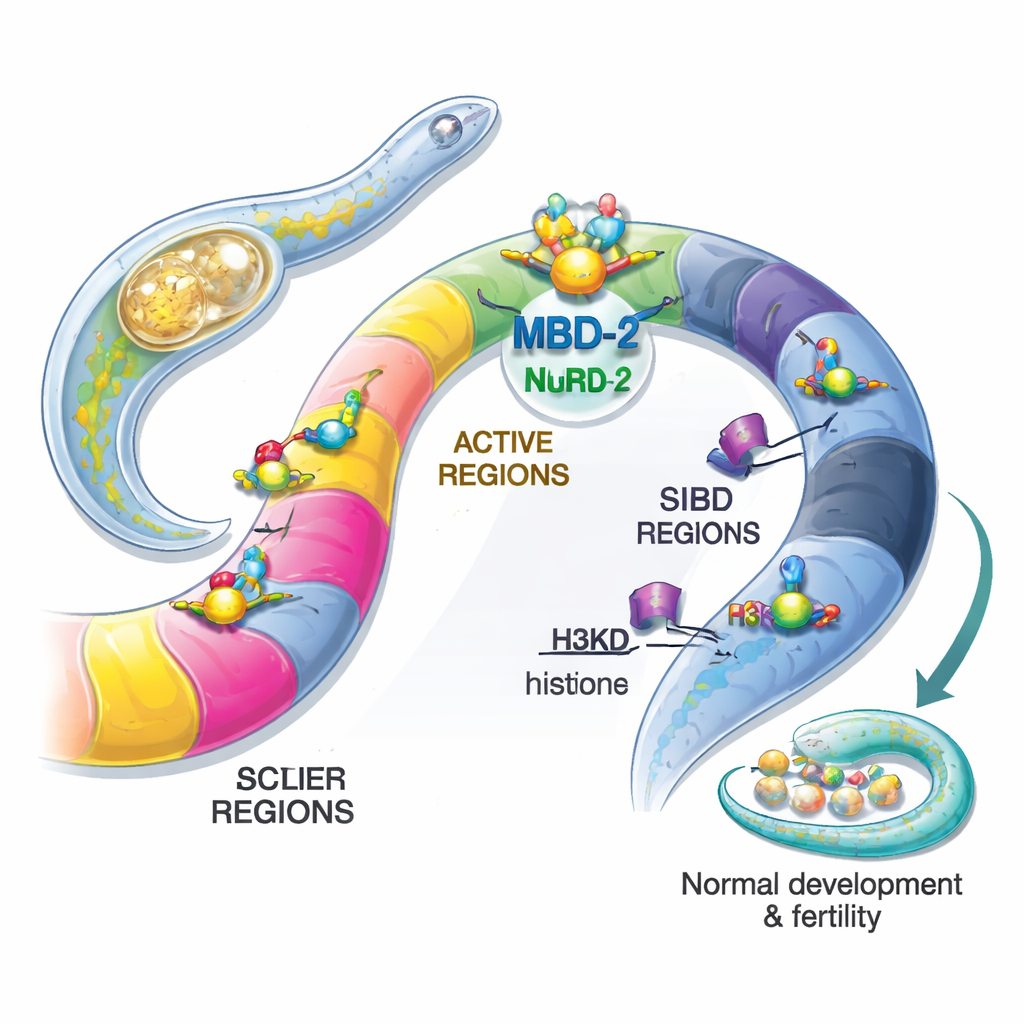
Ein fehlendes DNA‑Signal wirft eine große Frage auf
Bei Säugetieren hilft eine chemische Markierung namens 5‑Methylcytosin (5mC), Gene während der Entwicklung stummzuschalten, die X‑Chromosom‑Inaktivierung zu steuern und sich gegen springende Gene zu wehren. Proteine namens MBD2 und MBD3 erkennen diese Markierungen und rekrutieren einen großen Proteinkomplex, das NuRD‑Komplex, der Chromatin umgestalten und deaktivieren kann. Seltsamerweise haben viele Wirbellose, darunter C. elegans und Fruchtfliegen, 5mC und die dafür verantwortlichen Enzyme verloren – dennoch besitzen sie ein MBD2/3‑ähnliches Protein. Das wirft ein Rätsel auf: Warum behält man einen „DNA‑Methylierungsleser“ in einem Genom, das DNA‑Methylierung nicht mehr nutzt, und welche Funktion erfüllt er stattdessen?
Ein Gerüstprotein, ohne das Würmer nicht leben können
Die Autoren konzentrierten sich auf die Wurmversion dieses Proteins, genannt MBD‑2. Im Gegensatz zu seinen Verwandten bei Säugetieren hat Wurm‑MBD‑2 die klassische methylbindende Domäne verloren, die 5mC erkennt, behält aber flexible und coiled‑coil‑Abschnitte, die an andere Proteine andocken können. Durch das Anheften fluoreszenter Marker an MBD‑2 zeigten die Forscher, dass es in den Zellkernen fast aller Zellen während des gesamten Lebens des Wurms präsent ist, was auf eine breite Rolle in der Genregulation hindeutet. Mithilfe gentechnischer Veränderungen erzeugten sie Würmer, denen MBD‑2 vollständig fehlte, oder denen nur die coiled‑coil‑Region fehlte, die die Verbindung zu NuRD vermittelt. Beide Mutationen führten zu schweren Problemen: die Tiere waren klein, bewegten sich schlecht, entwickelten missgebildete Fortpflanzungsorgane und waren größtenteils steril. Das zeigte, dass MBD‑2 für normale Entwicklung und Fruchtbarkeit unerlässlich ist – selbst ohne DNA‑Methylierung.
Den NuRD‑Apparat in einer methylierungsfreien Welt rekonstruieren
Um zu prüfen, ob Wurm‑MBD‑2 weiterhin mit NuRD zusammenarbeitet, zogen die Autoren markiertes MBD‑2 aus Wurmextrakten und identifizierten seine Partner mittels Massenspektrometrie. Die meisten bekannten NuRD‑Komponenten waren vorhanden, was bestätigt, dass MBD‑2 als zentrales Gerüst in diesem Komplex dient, ähnlich wie MBD2/3 bei Säugetieren. Beim Entfernen der coiled‑coil‑Region gingen viele dieser Interaktionen verloren, insbesondere jene mit Proteinen, die Nukleosomen umstrukturieren. Parallel dazu zeigte groß angelegte RNA‑Sequenzierung, dass mehr als ein Viertel aller Wurmgene in MBD‑2‑Mutanten ihre Aktivität veränderten, wobei deutlich mehr Gene angeschaltet als abgeschaltet wurden. Dieses Muster deutet darauf hin, dass MBD‑2, oft in Zusammenarbeit mit NuRD, allgemein als Repressor wirkt, um ungewollte Gene stillzuhalten, gleichzeitig aber auch die richtige Aktivität einer Untergruppe hoch exprimierter Gene unterstützt.
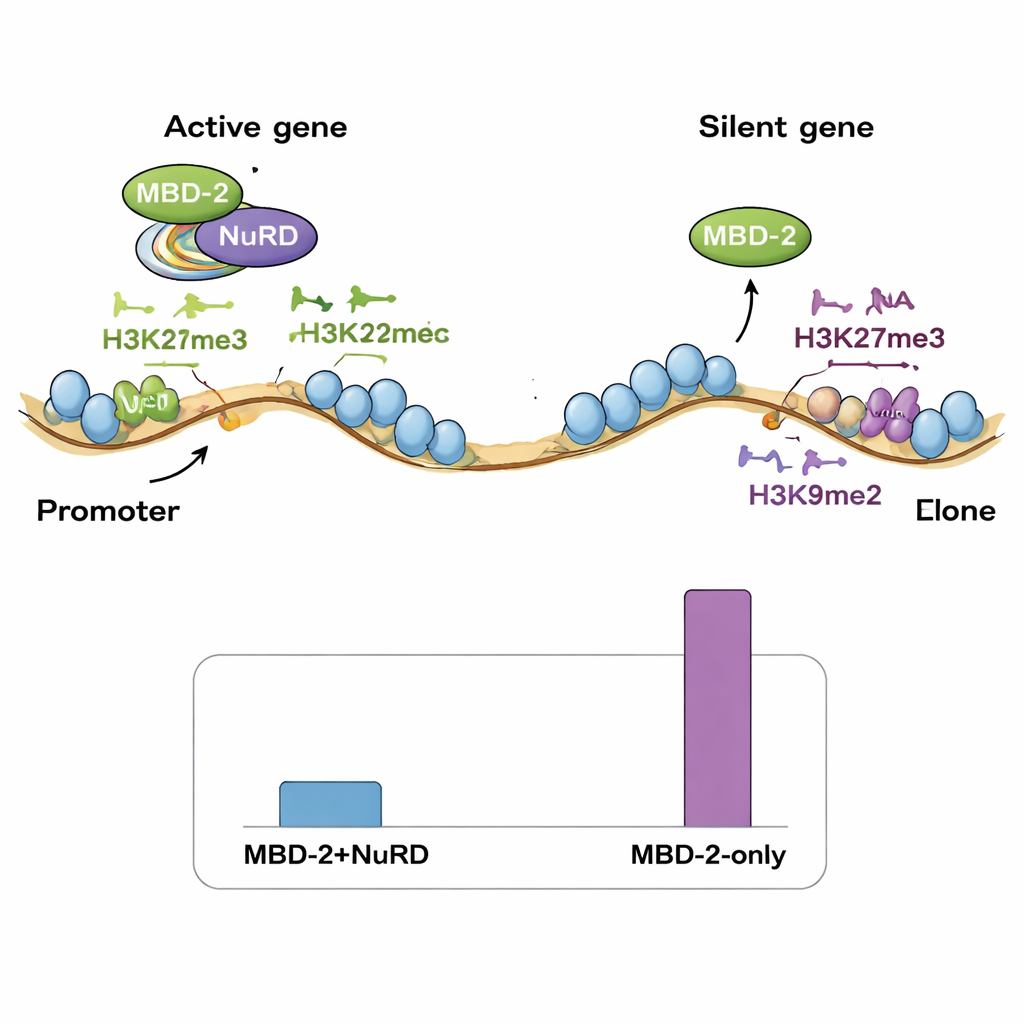
Zwei Bindungsmodi im Genom
Anschließend kartierten die Forscher mittels ChIP‑seq, wo MBD‑2 im Genom sitzt, und verglichen diese Orte mit vorhandenen Karten von NuRD‑Komponenten und verschiedenen Histonmarken. Überraschenderweise stimmte nur ein kleiner Bruchteil der MBD‑2‑Stellen eng mit NuRD‑Proteinen und Markern offener, aktiver Chromatinregionen überein. Die große Mehrheit der MBD‑2‑Stellen lag anderswo, in chromosomalen „Armen“, die reich an repressiven Histonmarken wie H3K27me3 und H3K9me2/3 sind. Mit anderen Worten zeigt MBD‑2 ein doppeltes Verhalten: An einer Minderheit von Stellen reist es mit NuRD, um aktive Gene feinzujustieren, an vielen weiteren Stellen bindet es unabhängig in bereits stummen Regionen. Auch das Bindungsmuster innerhalb von Genen ist bedeutsam – wenn MBD‑2 nahe dem Genstart konzentriert ist, führt der Verlust des Proteins eher zur Aktivierung dieser Gene, während Bindung tiefer in Genkörpern oft mit einer verminderten Genexpression einhergeht, wenn MBD‑2 entfernt wird.
Ein evolutionäres Backup für fehlende DNA‑Methylierung
Die Autoren schlagen vor, dass in Arten, die die DNA‑Methylierung verloren haben, repressive Histonmarken – insbesondere H3K27me3 – möglicherweise expandiert sind, um eine ähnliche regulatorische Funktion zu übernehmen. Wurm‑MBD‑2 scheint umfunktioniert worden zu sein: Anstatt 5mC auf der DNA zu lesen, assoziiert es jetzt mit Chromatinregionen, die durch spezifische Histonmodifikationen markiert sind, während es über seine konservierten Protein‑Interaktionsdomänen weiterhin das NuRD‑Komplex verankert. Diese Arbeit zeigt, dass ein altes Gen‑Stummschaltungs‑Werkzeug über die Evolution hinweg umverdrahtet werden kann: Die chemische Markierung auf der DNA kann verschwinden, aber die zugehörige Proteinausstattung überlebt, indem sie auf alternative Signale umsteigt. Für Nicht‑Spezialisten lautet die Kernbotschaft: Genregulation ist bemerkenswert anpassungsfähig – Zellen können einen wichtigen epigenetischen Marker verlieren und dennoch die komplexe Kontrolle von Tausenden Genen aufrechterhalten, indem sie stärker auf andere Chromatin‑Marken und auf die vielseitigen Gerüstfunktionen von Proteinen wie MBD‑2 setzen.
Zitation: Tsui, H.N., Wong, C.Y.Y., Zheng, C. et al. Dual genomic localizations and gene regulatory functions of MBD-2 with and without NuRD in Caenorhabditis elegans which lacks DNA methylation. Nat Commun 17, 1875 (2026). https://doi.org/10.1038/s41467-026-68592-0
Schlüsselwörter: Epigenetik, Chromatin, Genregulation, C. elegans, Histonmodifikation