Clear Sky Science · de
Ein hochdynamisches mononukleares nicht‑Hämeisen‑Enzym für die zweistufige Isonitril‑Biosynthese
Wie Bakterien exotische chemische Werkzeuge bauen
Isonitrile sind kleine, aber wirkungsvolle chemische Gruppen, die sich wie Schweizer Taschenmesser verhalten: Sie können Metalle binden, auf vielfältige Weise reagieren und dienen häufig als „Wirkstück“ potenter natürlicher Antibiotika und Toxine. Einige krankheitserregende Bakterien, darunter der Tuberkuloseerreger Mycobacterium tuberculosis, hängen Isonitrile an Fettsäuren, um daraus Metalle vom Wirt abzuzweigen. Dieser Beitrag untersucht, wie eines ihrer Enzyme, genannt Rv0097, diese ungewöhnlich anspruchsvolle Chemie in zwei sorgfältig choreografierten Schritten vollzieht.
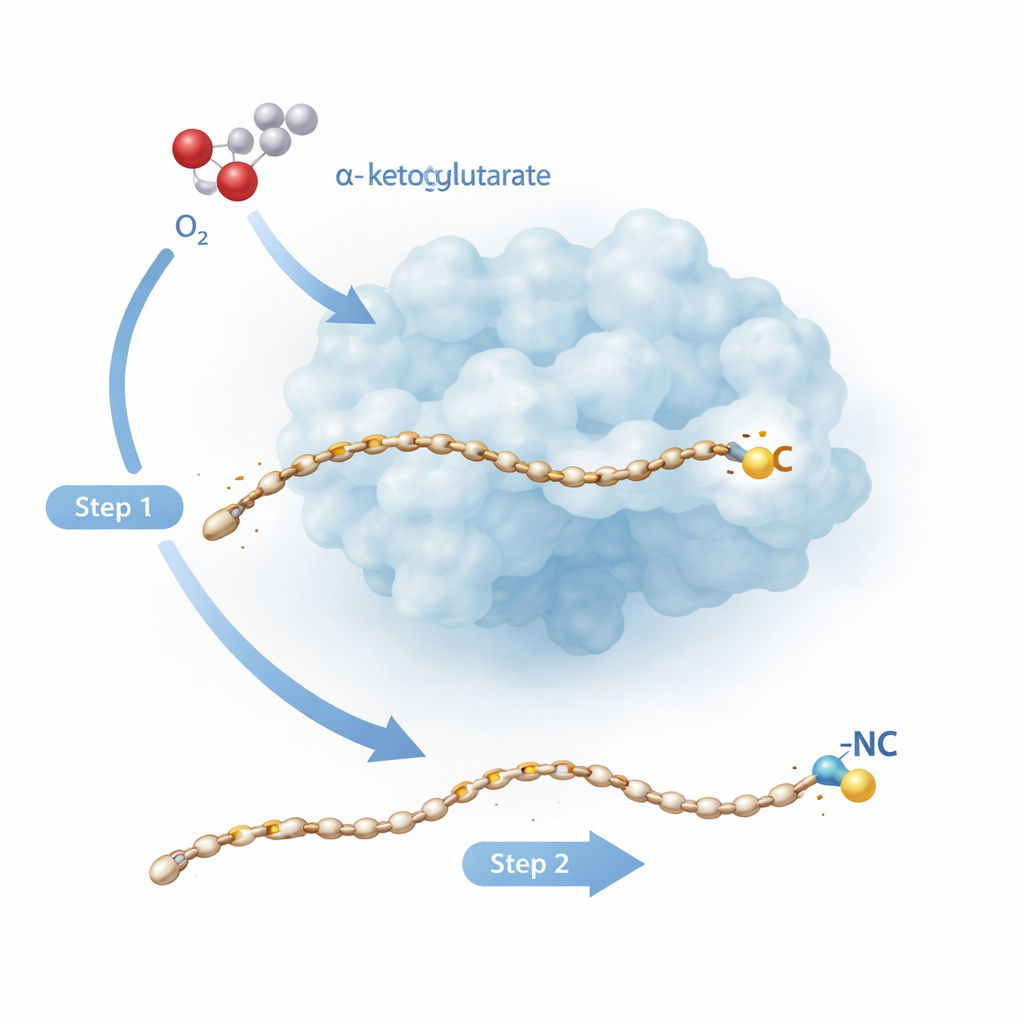
Eine zweistufige molekulare Umwandlung
Rv0097 gehört zu einer großen Familie eisenabhängiger Enzyme, die normalerweise einfachere Aufgaben ausführen, etwa das Einfügen von Sauerstoff an einer einzelnen Position eines Moleküls. Hier ist die Aufgabe anspruchsvoller: Aus einem „Glycyl–Fettsäure“‑Baustein muss das Enzym eine völlig neue Isonitril‑Gruppe erzeugen, wobei beide Schlüsselatome — das Kohlenstoff‑ und das Stickstoffatom — aus demselben kleinen Glycinfragment stammen. Frühere Arbeiten an einem verwandten Enzym, ScoE, legten nahe, dass dies nicht in einem Schritt möglich ist. Stattdessen sind zwei getrennte Reaktions‑„Halbzyklen“ erforderlich, jeweils angetrieben von einer Eisen‑Sauerstoff‑Spezies, die entsteht, wenn das Enzym das Hilfsmolekül α‑Ketoglutarat aufspaltet und mit Luftsauerstoff kombiniert. Die neue Studie widmet sich dem Tuberkuloseenzym Rv0097, um auf atomarer Auflösung zu beobachten, wie ein Enzym diese zwei radikalischen Schritte hintereinander am selben Substrat ausführt, ohne die Kontrolle zu verlieren.
Das Enzym im Moment des Geschehens einfrieren
Mithilfe der Röntgenkristallographie hielten die Forscher sechzehn hochauflösende Momentaufnahmen von Rv0097 in verschiedenen Zuständen fest: leer, gebunden an sein Fettsäuresubstrat (ein zehn Kohlenstoffatome enthaltendes Molekül namens CADA), gebunden an das Hilfsmolekül α‑Ketoglutarat und in Kombinationen, die vergängliche Reaktionszwischenstufen nachbilden. Diese Strukturen zeigen, dass Rv0097 eine gespaltene Persönlichkeit besitzt. Im Ruhezustand ist sein aktives Zentrum größtenteils verschlossen, wobei eine Schlüsselaminosäure (Phenylalanin 102) zwischen zwei Orientierungen wechselt, die die lange Fettsäureschlaufe trocken halten und für hydrophobe Wechselwirkung bereitstellen. Wenn CADA bindet, rastet dieses Residuum in eine einzige Orientierung ein, und der polare „Kopf“ des Substrats wird von geladenen Seitenketten verankert, während sein öliger Schwanz sich in einen engen Tunnel legt. Mutationen dieses Sperrpaars (F102 und ein nahegelegenes Glycin, G204) blockieren entweder die Tasche oder lassen zu viel Wasser eindringen, verringern die Aktivität drastisch und verändern die bevorzugten Kettenlängen des Enzyms.
Bewegliche Deckel und dynamische Schleifen
Über die Substrattasche hinaus verhält sich Rv0097 wie eine winzige Maschine mit beweglichen Türen. Das Team beobachtete „offene“ und „geschlossene“ Konformationen, in denen zwei deckelartige Bereiche sich über das aktive Zentrum auseinander‑ bzw. zusammenklappen. Das Öffnen legt das Eisenzentrum frei und schafft einen Weg für α‑Ketoglutarat und Substrat hinein; das Schließen schützt die Chemie vor dem umgebenden Wasser, sobald die Reaktion im Gange ist. Zwei flexible Oberflächenschleifen, die His‑Schleife und die Arg‑Schleife nach den Histidin‑ bzw. Argininresten benannt, fungieren als zusätzliches Tor. In einigen Strukturen schwenken diese Schleifen nach innen, sodass das Arginin α‑Ketoglutarat greifen kann; in anderen schwenken sie nach außen und schaffen offenbar einen Seitenkanal, durch den verbrauchte Hilfsfragmente (Succinat und Kohlendioxid) entweichen und frisches α‑Ketoglutarat für den zweiten Schritt eintreten kann — und das alles, während das aus dem Substrat stammende Zwischenprodukt fixiert bleibt.
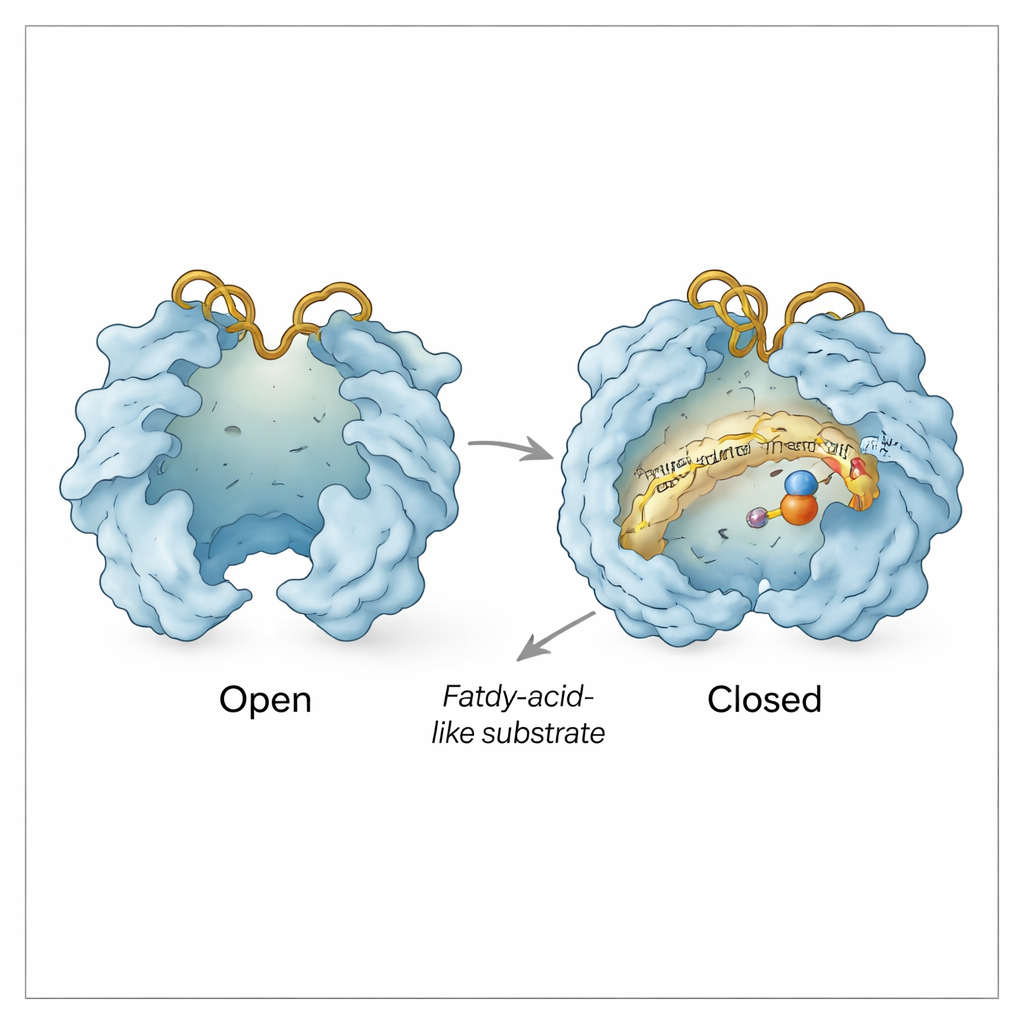
Schutz eines fragilen Zwischenprodukts
Biochemische Tests stützen dieses Strukturkonzept. Die erste Halbreaktion wandelt CADA in ein hochreaktives Imin‑Zwischenprodukt um, das schnell zerfällt, wenn es in Lösung abwandert. Durch chemisches Einfangen seines Abbauprodukts zeigen die Autoren, dass der Großteil dieses Zwischenprodukts nur nachweisbar ist, solange das Enzym noch vorhanden ist — was darauf hindeutet, dass es zwischen den beiden Halbreaktionen gebunden und geschützt im Inneren von Rv0097 verbleibt. Die Strukturen erklären, wie das geschieht: Subtile Umpositionierungen der His‑ und Arg‑Schleifen, zusammen mit kleinen Verschiebungen benachbarter Reste, scheinen das Zwischenprodukt in eine geschützte Höhlung einzuschließen und gleichzeitig kleinen Molekülen wie α‑Ketoglutarat, Succinat und Kohlendioxid den Austausch über kontrollierte Kanäle zu ermöglichen.
Warum das für TB und darüber hinaus wichtig ist
Zusammen enthüllen diese Ergebnisse Rv0097 als ein hochdynamisches, einproteiniges Fließband, das eisenbasierte Chemie zweimal hintereinander am selben Substrat nutzt, ohne jemals ein gefährliches Zwischenprodukt freizugeben. Für Tuberkulosebakterien begründet diese Präzision die Herstellung von isonitril‑modifizierten Molekülen, die ihnen helfen, im Körper lebenswichtige Metalle zu beschaffen; genetische Studien deuten darauf hin, dass der Weg für ihr Überleben während der Infektion wichtig ist. Für Chemiker und Wirkstoffdesigner bietet die Arbeit eine Blaupause, verwandte Enzyme zu konstruieren, um neue isonitrilhaltige Verbindungen herzustellen, und legt nahe, dass das Stören von Rv0097s beweglichen Deckeln und Toren ein Weg sein könnte, neue Antibiotika zu entwickeln.
Zitation: Ye, N., Del Rio Flores, A., Zhang, W. et al. A highly dynamic mononuclear non-heme iron enzyme for the two-step isonitrile biosynthesis. Nat Commun 17, 2034 (2026). https://doi.org/10.1038/s41467-026-68588-w
Schlüsselwörter: Isonitril‑Biosynthese, nicht‑Hämeisen‑Enzym, Mycobacterium tuberculosis, Enzymdynamik, metall‑chelatisierende Naturstoffe