Clear Sky Science · de
Störung der Eisen-Homöostase macht Bauchspeicheldrüsenkrebs empfindlicher für irreversible Elektroporation
Strom und Eisen gegen einen tödlichen Krebs einsetzen
Bauchspeicheldrüsenkrebs gehört zu den am schwersten zu behandelnden Krebserkrankungen, und selbst aggressive lokal wirkende Therapien verhindern oft nicht ein Wiederauftreten. Diese Studie untersucht einen neuen Ansatz, um ein vorhandenes Verfahren — die irreversible Elektroporation, die Tumore mit kurzen, starken elektrischen Impulsen abtötet — wirksamer und sicherer zu machen. Indem die Forschenden geschickt den Eisenstoffwechsel der Krebszellen stören, zeigen sie, dass sich überlebende Zellen in eine destruktive Form des Zelltods drücken lassen, was die Wahrscheinlichkeit eines Tumorrezidivs potenziell verringern könnte.
Warum elektrische Impulse allein nicht ausreichen
Die irreversible Elektroporation (IRE) behandelt Tumore, indem dünne Elektroden in oder um den Krebs eingeführt und schnelle, hochspannungsstarke Pulse abgegeben werden. Diese Pulse erzeugen permanente Löcher in Zellmembranen, töten viele Krebszellen und lösen eine Immunantwort aus. Das elektrische Feld ist jedoch nicht gleichmäßig. Bereiche mit etwas schwächeren Pulsen können Zellen am Leben lassen, und diese Überlebenden können einen neuen Tumor begründen. Als das Team pankreatische Krebszellen und Tumore von Mäusen untersuchte, die einem subletalen elektrischen Feld ausgesetzt waren, stellten sie fest, dass diese Zellen statt durch einen eisengetriebenen Prozess namens Ferroptose zu sterben, ein breites antioxidatives Schutzprogramm aktivierten. Wichtige Schutzgene, einschließlich solcher, die helfen, eisenbedingte Schäden zu neutralisieren, wurden hochreguliert, sodass die Zellen den Angriff überstanden und sich erholten.
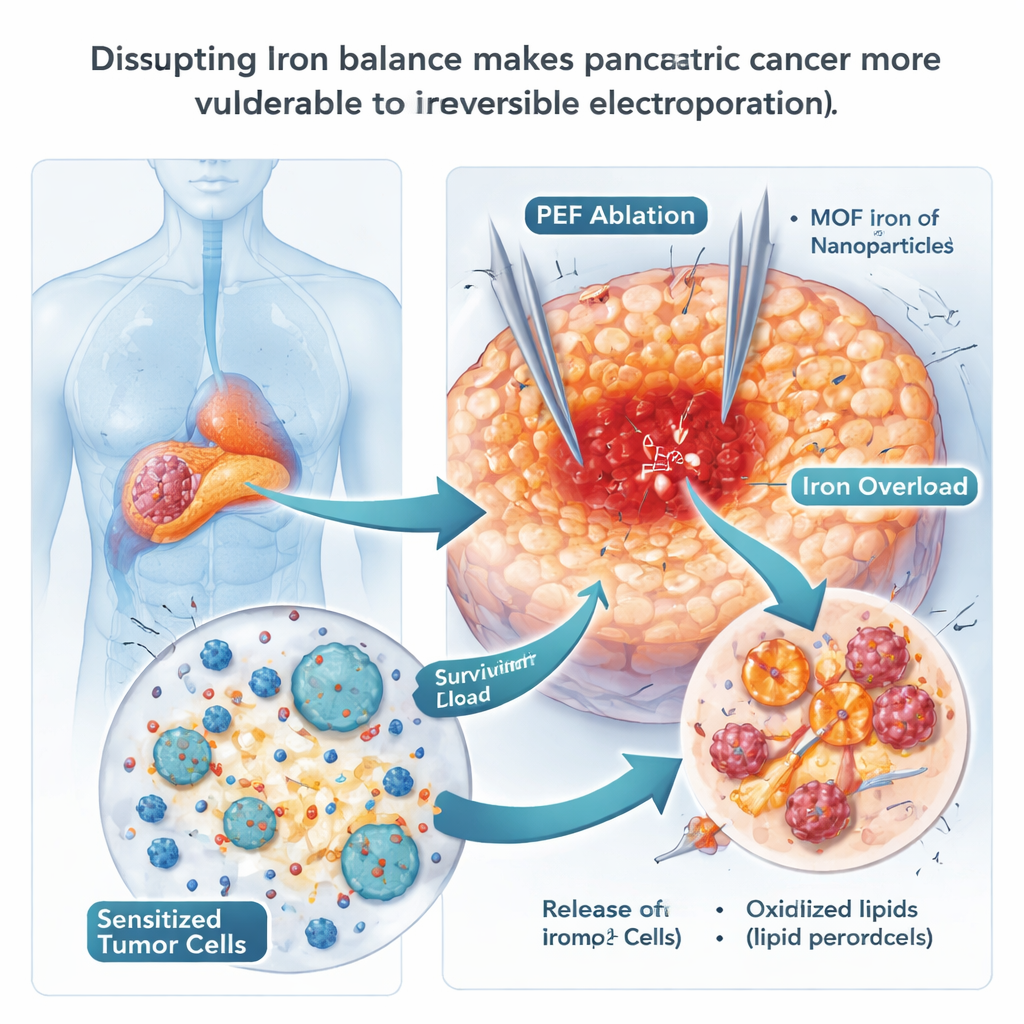
Eisen-Nanopartikel einsetzen, um Zellen zur Zerstörung zu treiben
Da Ferroptose vom Eisen abhängt, testeten die Wissenschaftler, ob eisenreiche Nanopartikel Krebszellen über die Kante treiben könnten. Sie verwendeten speziell entwickelte Metall–organische Gerüstpartikel mit Eisen (MOF-Fe), die in den sauren Zellkompartimenten schnell Eisen freisetzen. In Zellkulturen akkumulierten pankreatische Krebszellen, die diese Partikel aufnahmen, freies Eisen und oxidierte Membranlipide — klassische Merkmale der Ferroptose — und bildeten deutlich weniger Kolonien. In Mäusen verzögerte die Kombination von MOF-Fe mit IRE das Tumorwachstum länger als jede Einzelbehandlung, und die Tumore zeigten mehr Anzeichen oxidativer Schäden. Dieser Vorteil war jedoch vorübergehend: Nach etwa drei Wochen begannen die Tumore wieder zu wachsen, was darauf hindeutet, dass der Krebs Wege fand, sich an die Eisenüberladung anzupassen.
Das zelluläre Eisen-„Safe“ ins Visier nehmen
Um diese Resistenz zu verstehen, analysierte das Team die Proteine, die sich nach der MOF-Fe-Behandlung veränderten. Auffällig war die Ferritin-Schwerekette 1 (FTH1), ein Teil des zellulären Eisenspeicherkoplexes — das molekulare Äquivalent eines feuerfesten Safes für überschüssiges Eisen. Bei experimentell erhöhten FTH1-Spiegeln wurden Krebszellen widerstandsfähiger gegen Ferroptose; bei Erniedrigung von FTH1 wurden sie empfindlicher. Das machte FTH1 zu einem zentralen Schutzschild gegen eisengetriebenen Tod. Die Forschenden entwickelten daraufhin ein Designer-Molekül, C20U4V, aufgebaut aus Arachidonsäure (einem stark oxidierbaren Fett) gekoppelt an ein PROTAC-Gerüst, das gezielt bestimmte Proteine an die zellulären Abbaumaschinen dirigiert. In Gegenwart von MOF-Fe band C20U4V Ferritin und rekrutierte es zur Markierung und Zerstörung, wodurch FTH1-Spiegel stark sanken und die Zelle daran gehindert wurde, Eisen sicher einzuschließen.
Von Zellkulturen zu Mini-Tumoren und Mäusen
Wurden MOF-Fe und C20U4V kombiniert, zeigten pankreatische Krebszellen höhere oxidative Belastung, mehr geschädigte Membranlipide, angeschlagene Mitochondrien und eine stark reduzierte Fähigkeit zur Wiederherstellung. Diese Synergie zeigte sich auch in dreidimensionalen, patientenabgeleiteten Organoiden — winzigen, tumorausähnlichen Strukturen aus echten Patientenproben — wo das Medikamentpaar sowohl Größe als auch Zahl der Organoide zum Einsturz brachte. Da C20U4V ölig und wasserunlöslich ist, verpackte das Team es in reaktive-sauerstoff-empfindliche Mizellen (M-C20U4V), die im Blut zirkulieren und das Medikament in gestresstem, geschädigtem Tumorgewebe freisetzen können. In Mausmodellen mit subkutan und intrapancreatisch implantierten Pankreastumoren verkleinerte eine Dreifachkombination aus IRE, MOF-Fe und M-C20U4V die Tumore deutlich wirksamer und verlängerte das Überleben im Vergleich zu ein- oder zweifachen Behandlungen. Die behandelten Tumore zeigten weniger teilende Zellen, mehr Marker der Ferroptose und eine stärkere Infiltration durch T‑Zellen und andere Immunzellen, was darauf hinweist, dass die Strategie nicht nur Krebszellen direkt tötet, sondern auch das Immunsystem unterstützt, den Tumor zu erkennen und anzugreifen.
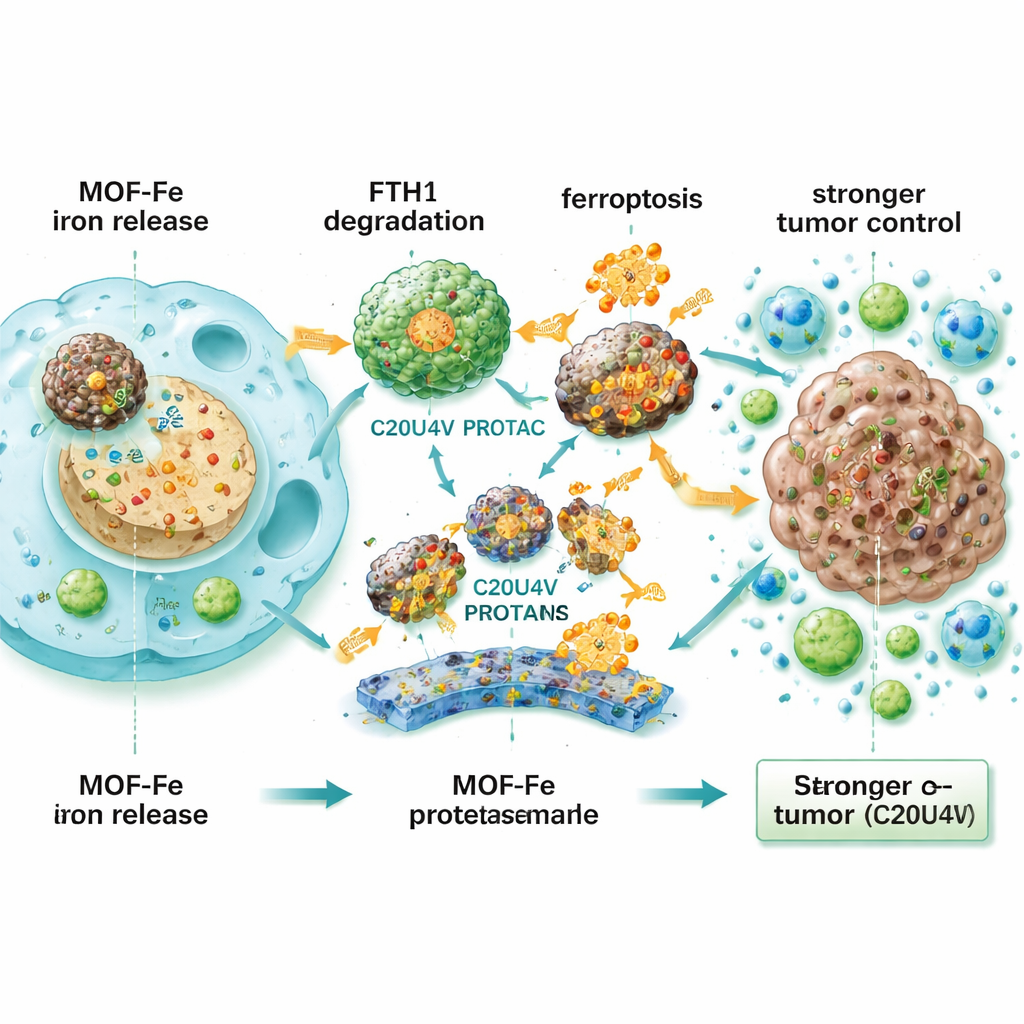
Was das für Patientinnen und Patienten bedeuten könnte
Für Nichtfachleute ist die Kernaussage einfach: Pankreastumore entkommen nach elektrischer Impulsablation oft, weil einige Krebszellen überleben und sich rasch anpassen. Diese Arbeit zeigt, dass das Beladen dieser Zellen mit Eisen und das gleichzeitige Ausschalten ihres eisen-sicheren Tresors sie in einen selbstzerstörerischen Zustand treiben kann, dem sie kaum widerstehen. Obwohl dieser Ansatz noch experimentell ist und umfassende Sicherheits- und Praxistests am Menschen erfordern würde, deutet er darauf hin, dass das gezielte Modifizieren des Umgangs von Tumoren mit einem grundlegenden Element wie Eisen eine unvollkommene lokale Therapie in einen entscheidenderen Schlag gegen einen der tödlichsten Krebsarten verwandeln könnte.
Zitation: Li, L., Su, S., Wang, Z. et al. Disruption of iron homeostasis sensitizes pancreatic cancer to irreversible electroporation. Nat Commun 17, 1866 (2026). https://doi.org/10.1038/s41467-026-68585-z
Schlüsselwörter: Bauchspeicheldrüsenkrebs, irreversible Elektroporation, Ferroptose, Eisen-Nanopartikel, PROTAC-Therapie