Clear Sky Science · de
Humane Typ‑1‑angeborene Lymphozyten steuern die Differenzierung von Leukämiestammzellen und begrenzen die Entstehung von akuter myeloischer Leukämie
Warum unsere eigenen Immunzellen bei Leukämie wichtig sind
Die akute myeloische Leukämie (AML) ist eine aggressive Blutkrebserkrankung, die selbst nach intensiver Chemotherapie häufig zurückkehrt. Eine treibende Kraft ist ein kleiner Bestand an „Starter“-Leukämiezellen, die die Krankheit wieder neu entfachen können. Diese Studie zeigt, dass ein weniger bekanntes Element des Immunsystems, die Typ‑1‑angeborenen Lymphozyten (ILC1), diese Starterzellen von gefährlichen Wachstumswegen weglenken und in experimentellen Modellen das Voranschreiten der Leukämie verlangsamen können. Die Arbeit beschreibt außerdem einen möglichen Weg, hilfreiche ILC1s aus gespendetem Nabelschnurblut herzustellen, als potenzielle künftige Therapie.
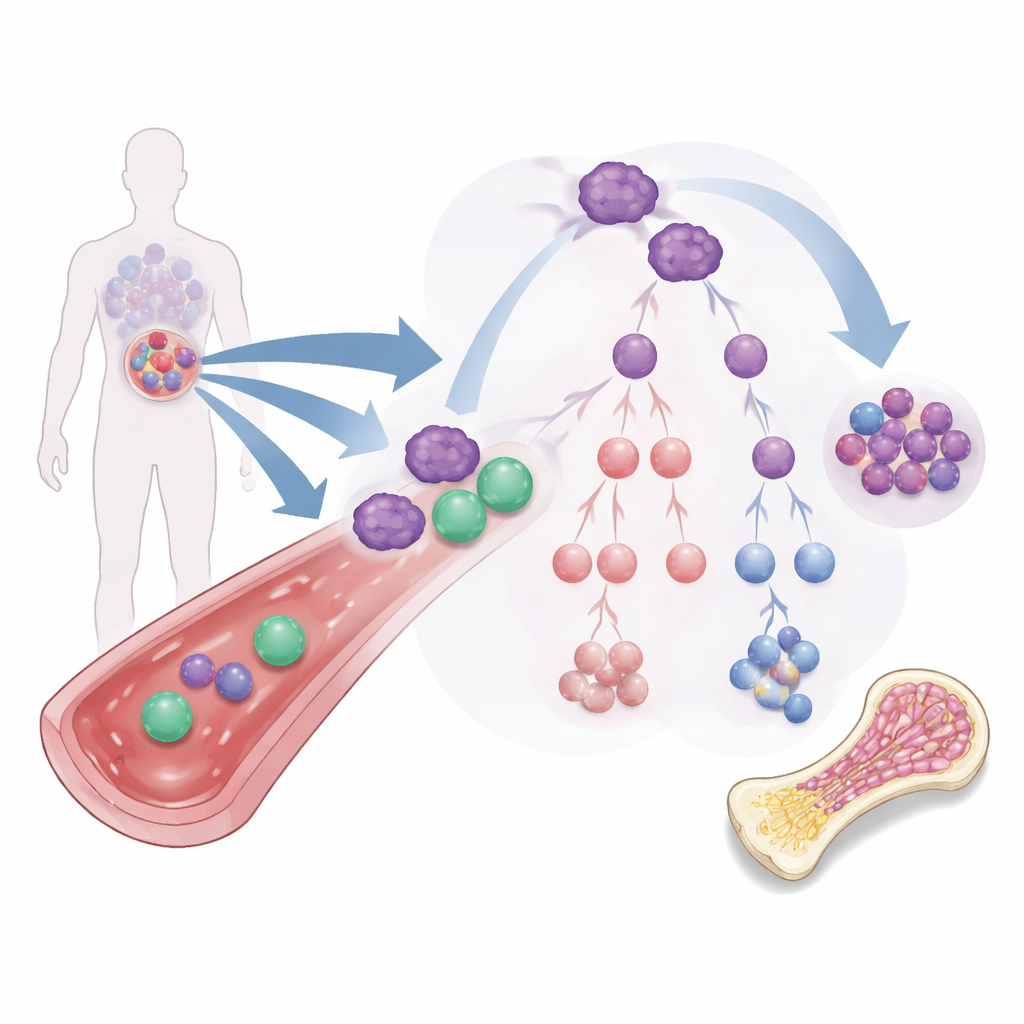
Das Problem hartnäckiger Leukämiestarterzellen
Die meisten AML‑Behandlungen zielen auf die Masse der Leukämiezellen im Blut und Knochenmark ab. Eine seltenere Untergruppe, bekannt als Leukämiestammzellen, verhält sich eher wie Samen: Sie können sich selbst erneuern, sind resistent gegen Standardmedikamente und können den Krebs wieder aufbauen. Diese Zellen können sich entlang mehrerer Entwicklungszweige in unterschiedliche leukämische Zelltypen differenzieren, von denen einige weiterhin die Fähigkeit zur Selbsterneuerung besitzen oder den Krebs vor dem Immunsystem abschirmen. Wegen dieses verzweigten „Familienstammbaums“ reicht es nicht aus, die sichtbare Leukämie zu verkleinern; Therapien müssen das Schicksal dieser Starterzellen verändern oder sie vollständig entfernen.
Eine fehlende Verteidigungslinie bei Patientinnen und Patienten
ILC1s sind schnell reagierende Immunzellen, die keine vorherige Exposition benötigen, um Bedrohungen zu erkennen. Die Forschenden verglichen ILC1s im Blut gesunder Freiwilliger mit denen von AML‑Patientinnen und -Patienten. Sie fanden, dass Betroffene insgesamt weniger ILC1s hatten und die vorhandenen Zellen weniger aktiv waren. Mithilfe von Einzelzell‑RNA‑Sequenzierung und Durchflusszytometrie zeigte das Team, dass die ILC1s der Patientinnen und Patienten geringere Mengen zentraler Tötungsmoleküle und wichtiger Immunbotenstoffe produzierten und weniger Aktivierungsrezeptoren auf ihrer Oberfläche zeigten. Bemerkenswert war, dass Patientinnen und Patienten mit höheren Anteilen an ILC1s tendenziell weniger Leukämiezellen aufwiesen — ein Hinweis darauf, dass diese Zellen in funktionellem Zustand dazu beitragen, die Erkrankung in Schach zu halten.
Wie gesunde ILC1s Leukämiezellen von schädlichen Pfaden ablenken
Um zu verstehen, was ILC1s konkret mit Leukämiestammzellen tun, kultivierte das Team beide Zelltypen gemeinsam im Labor. ILC1s von gesunden Spendern vernichteten die Stammzellen nicht einfach; stattdessen veränderten sie deren Reifung. Ein ILC1‑Signal, genannt TNFα, drängte die Stammzellen in einen intermediären Zustand und verringerte ihre Umwandlung in gefährlichere, schnell teilende Leukämiezellen. Es schränkte außerdem die Fähigkeit der Stammzellen ein, sich in makrophagenähnliche Zellen zu verwandeln, die normalerweise Immunantworten dämpfen und die Leukämie fördern. Ein weiteres Signal, IFNγ, begrenzte das Voranschreiten der Stammzellen in bestimmte hoch therapieresistente Formen. Als die Forschenden diese Signale mit Antikörpern blockierten, verschwanden die schützenden Effekte — ein Beleg dafür, dass ILC1s die Leukämieentwicklung über spezifische chemische Botschaften steuern.
Nabelschnurblut als Basis einer Immuntherapie
Da natürliche ILC1s im Erwachsenenblut selten sind, suchte das Team nach einer erneuerbaren Quelle. Sie zeigten, dass Stammzellen aus gespendetem Nabelschnurblut in Kultur zu einer speziellen ILC1‑Untergruppe differenziert werden können, die ein Oberflächenmarker namens CD161 nicht trägt, aber dennoch die passenden Transkriptionsfaktoren und Tötungswerkzeuge besitzt. Diese im Labor gezüchteten ILC1s vermehrten sich etwa 700‑fach, griffen Leukämiestammzellen an, schonten dabei jedoch normale blutbildende Stammzellen, und wiesen starke cytotoxische Moleküle auf. Nach Transfer in spezialisierte Mäuse, die menschliche Leukämiestammzellen trugen, reduzierten diese ILC1s das Leukämiewachstum und verlängerten das Überleben — ein Effekt, der von IFNγ abhängig war. In Direktvergleichen waren sie mindestens so wirksam wie ähnlich hergestellte natürliche Killerzellen.
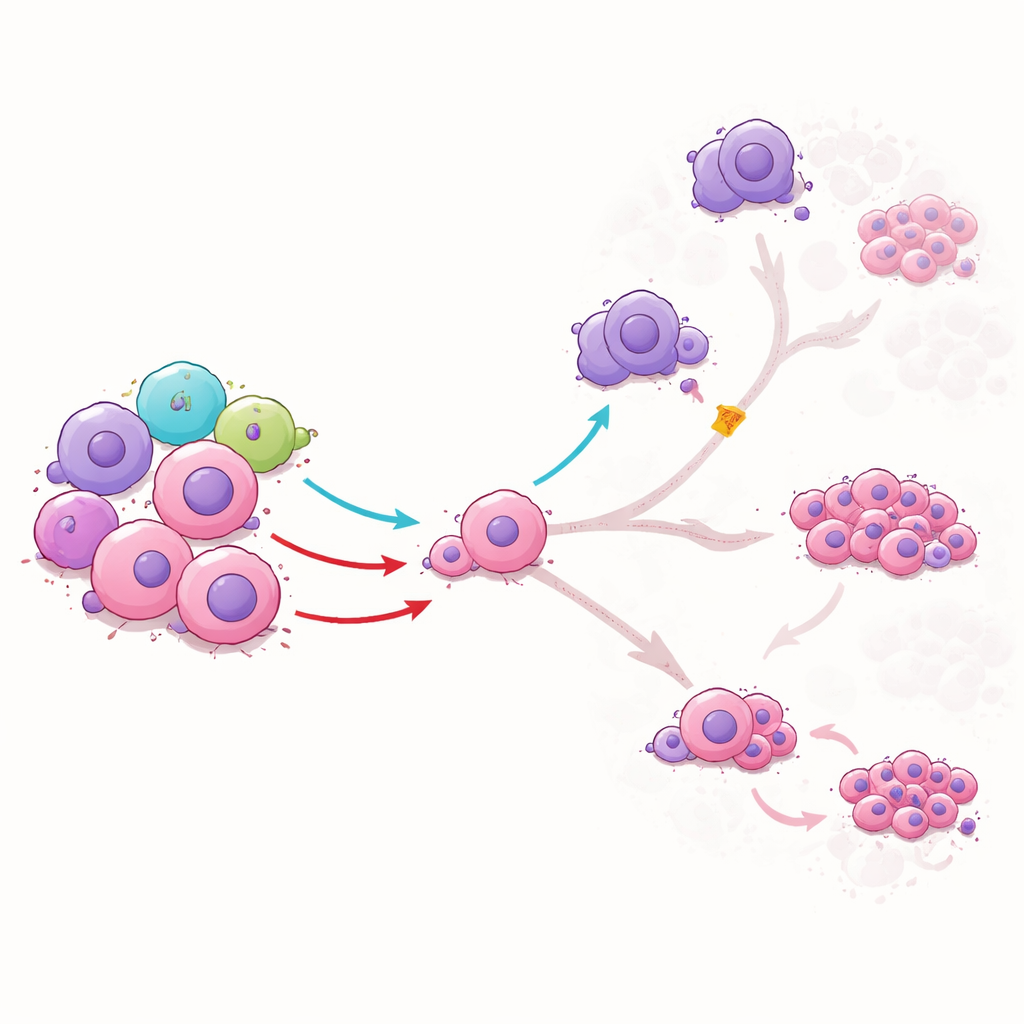
Was das für künftige Behandlungen bedeuten könnte
Insgesamt zeigt die Studie, dass bei AML eine natürliche immunologische Bremse — die ILC1‑Population — sowohl reduziert als auch geschwächt ist. Wenn sie von gesunden Spendern zugeführt oder aus Nabelschnurblut erzeugt werden, können ILC1s Leukämiestammzellen von den schädlichsten und therapieresistentesten Entwicklungspfaden abbringen, die leukämiefördernden makrophagenähnlichen Zellen verringern und die Erkrankung in Mausmodellen verlangsamen. Für Laien lautet die zentrale Botschaft: Forschende lernen nicht nur, Krebszellen zu töten, sondern auch, die frühesten Leukämiesamen mithilfe körpereigener Schnellreaktions‑Immunzellen in weniger gefährliche Richtungen zu „coachen“. Mit weiterer Entwicklung sowie sicherer und skalierbarer Herstellung könnten ILC1‑basierte Zelltherapien eines Tages bestehende Behandlungen ergänzen, um ein Wiederkehren von AML zu verhindern.
Zitation: Li, Z., Ma, R., Tang, H. et al. Human type-1 innate lymphoid cells control leukemia stem cell differentiation and limit acute myeloid leukemia development. Nat Commun 17, 2377 (2026). https://doi.org/10.1038/s41467-026-68582-2
Schlüsselwörter: akute myeloische Leukämie, Leukämiestammzellen, angeborene Lymphozyten, Krebsimmuntherapie, Nabelschnurblut