Clear Sky Science · de
Identifizierung von Chlamydia pneumoniae und Aktivierung des NLRP3-Inflammasoms in der Netzhaut bei Alzheimer-Krankheit
Warum Keime im Auge für das Gedächtnis wichtig sind
Alzheimer-Krankheit wird meist als Problem von Plaques und Neurofibrillenbündeln im Gehirn verstanden. Diese Studie legt nahe, dass ein verbreitetes, Lungenentzündungen verursachendes Bakterium, Chlamydia pneumoniae, sich unbemerkt im lichtempfindlichen Gewebe im hinteren Auge — der Netzhaut — niederlassen und dort die Entzündungen und Nervenschäden fördern kann, die bei Alzheimer beobachtet werden. Da die Netzhaut nichtinvasiv bildgebend untersucht werden kann, deutet diese Arbeit darauf hin, dass Augenuntersuchungen eines Tages helfen könnten, infektiös bedingte Gehirnerkrankungen zu erkennen und frühe Therapien zu steuern.
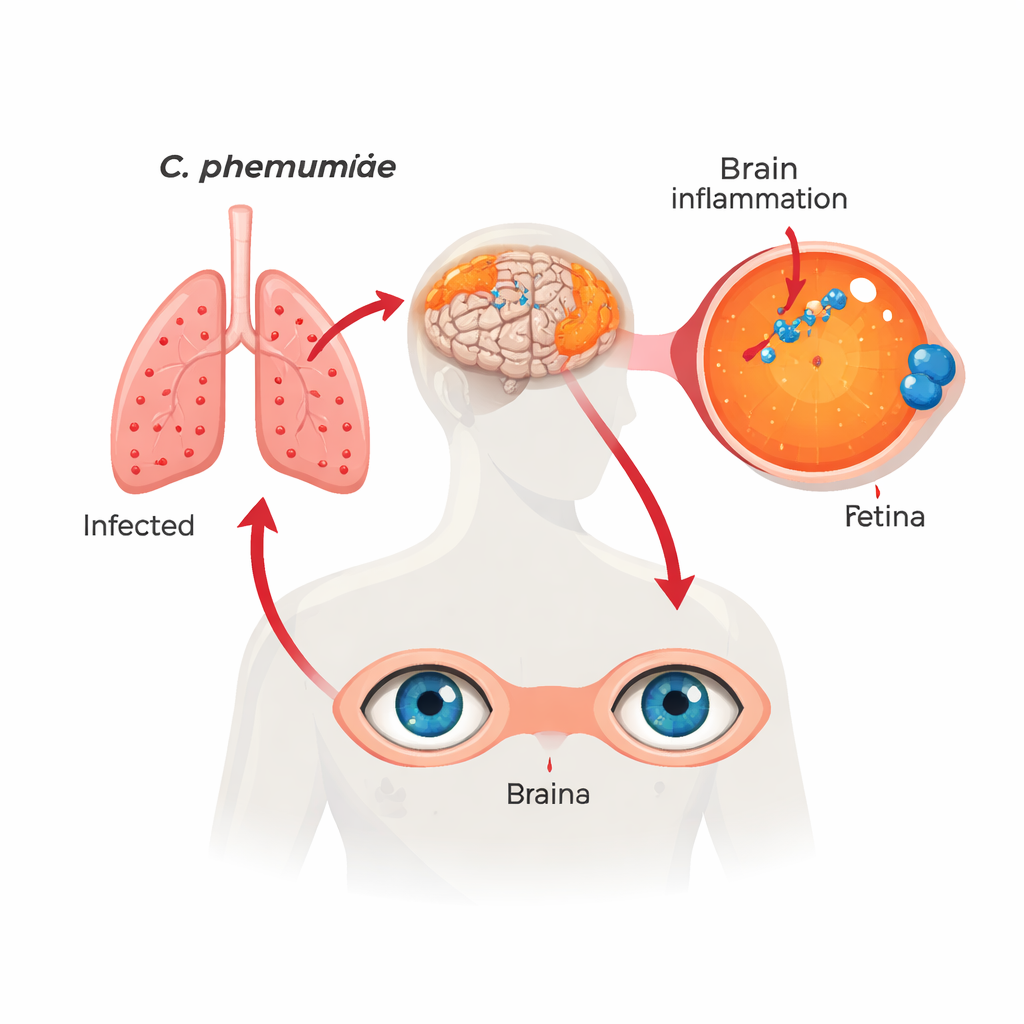
Eine bekannte Infektion an einem unerwarteten Ort
Die Forschenden untersuchten Netzhäute und passende Gehirnproben von mehr als 100 Verstorbenen mit normaler Kognition, leichter kognitiver Beeinträchtigung oder Alzheimer-Demenz. Mit mehreren unabhängigen Methoden — darunter spezielle Antikörper, genetische Sonden, Färbeverfahren und DNA-Tests — fanden sie eindeutige Hinweise auf Chlamydia pneumoniae innerhalb retinaler Zellen. Diese bakteriellen „Inklusionen“ traten am häufigsten und in größter Zahl bei Personen mit Alzheimer auf, weniger bei denen mit leichter Beeinträchtigung und am seltensten bei denen mit erhaltener kognitiver Gesundheit. Die Menge an Bakterien in der Netzhaut spiegelte eng die im Gehirn gefundene Menge wider, was darauf hindeutet, dass sowohl Auge als auch Gehirn Teil derselben lang andauernden Infektion sind.
Zusammenhänge zwischen Bakterien, Plaques und Denkvermögen
Das Auffinden des Erregers war nur der erste Schritt; die entscheidende Frage war, ob das für die Krankheit relevant ist. Das Team maß klassische Alzheimer-Marker in denselben Geweben. Sie beobachteten, dass eine höhere bakterielle Last in der Netzhaut mit mehr Amyloid‑Beta-Ablagerungen — dem klebrigen Protein, das Plaques bildet — sowie bestimmten abnormalen Tau-Formen einherging. Personen mit stärkerem bakteriellen Signal im Gehirn wiesen zudem mehr Nervenzellverstrickungen, schwerere Alzheimer-Pathologie und stärkere Gehirnatrophie auf. Klinisch erzielten diejenigen mit höherer bakterieller Belastung der Netzhaut niedrigere Gedächtnis- und Denkleistungen und hatten fortgeschrittenere Demenz. Träger der APOE ε4-Genvariante, eines starken genetischen Risikofaktors für Alzheimer, trugen in Netzhaut und Gehirn mehr von dem Bakterium, was auf eine Gen–Infektion-Interaktion hindeutet.
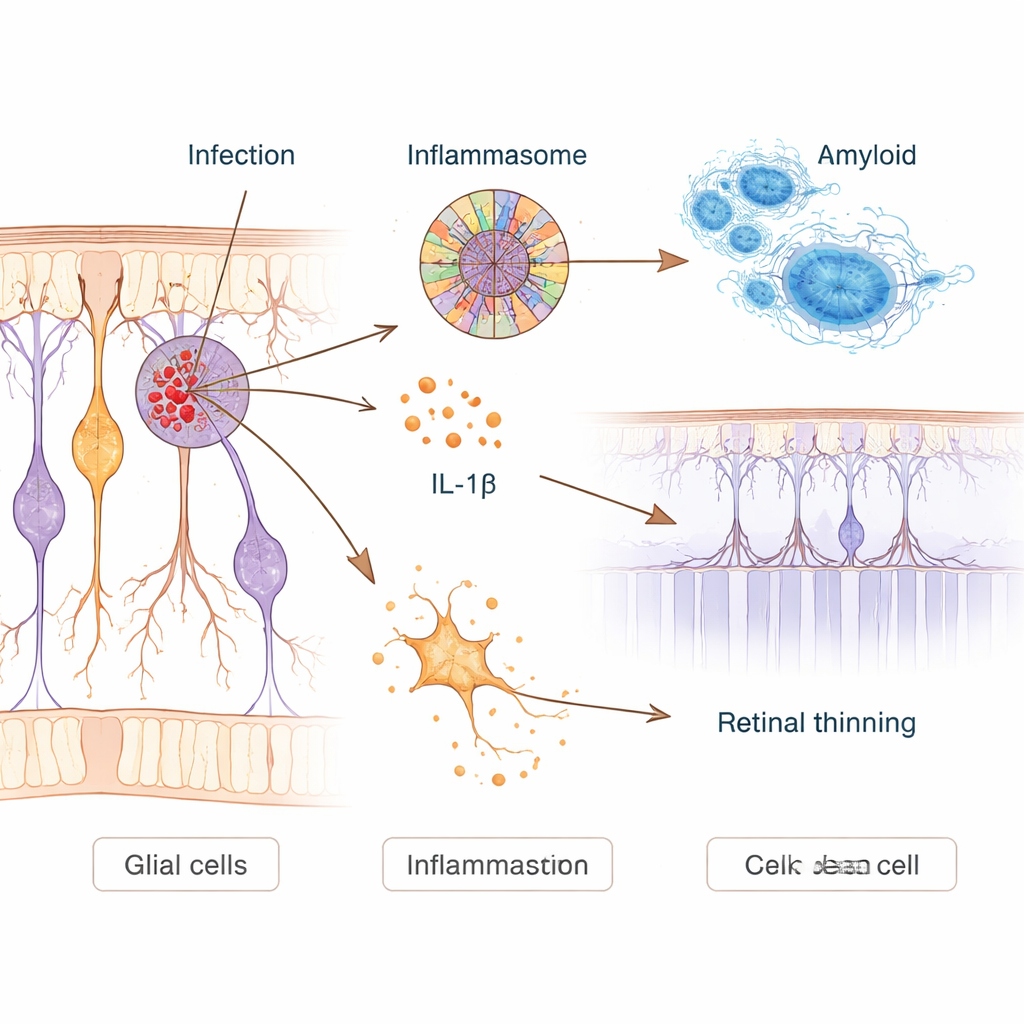
Wie eine Infektion toxische Entzündung auslösen kann
Um Ursache und Wirkung zu klären, infizierten die Wissenschaftler menschliche, nervähnliche Zellen im Labor sowie Alzheimer-Modellmäuse mit Chlamydia pneumoniae. In kultivierten Neuronen führte die Infektion zu gesteigerter Produktion von Amyloid‑Beta und aktivierte ein molekulares Alarmsystem, das NLRP3-Inflammasom genannt wird. Dieses System wirkt wie ein zellulärer Auslöser: Einmal aktiviert, setzt es entzündliche Botenstoffe wie Interleukin‑1β frei und kann Löcher in Zellmembranen reißen, was zu einer explosiven Form des Zelltods führt. Infizierte Neuronen zeigten klare Zeichen von Membranschäden und Aktivierung dieser Wege. Bei Mäusen reichte eine einmalige nasale Gabe des Bakteriums aus, damit es das Gehirn erreichte, dort Amyloid-Plaques verstärkte, Immunzellen aktivierte und Monate später die Leistung in gedächtnis- und sehbezogenen Labyrinthen verschlechterte.
Retinale Immunzellen unter Druck
In menschlichen Augen kartierten die Forschenden, wie die Infektion mit den lokalen Stütz- und Schutzzellen der Neuronen interagierte. Sternförmige Astrozyten und Müller-Zellen sowie Mikroglia — die ortsansässigen „Aufräum“-Zellen von Gehirn und Netzhaut — sammelten sich um infizierte Stellen. Chemische Signale des NLRP3-Inflammasoms und seiner downstream-Death‑Wege waren in Netzhäuten von Alzheimer-Patienten stark erhöht und bereits bei Personen mit leichter kognitiver Beeinträchtigung im Ansteigen begriffen. Viele infizierte Zellen trugen Marker sowohl für die feurige „Pyroptose“ als auch für die bekanntere Apoptose. Obwohl in Alzheimer-Netzhäuten mehr Mikroglia rekrutiert wurden, schien jedes Bakterium von weniger Mikroglia kontaktiert oder aufgenommen zu werden als in gesunden Augen, was darauf hindeutet, dass das Aufräumsystem mit Fortschreiten der Krankheit überlastet oder beeinträchtigt wird.
Das Auge nutzen, um die Gesundheit des Gehirns abzulesen
Da die Netzhaut bei lebenden Menschen hochauflösend bildgebend zugänglich ist, fragten die Forschenden, ob retinaale Messwerte in Bezug auf Chlamydia pneumoniae helfen könnten, den Alzheimer-Status vorherzusagen. Sie nutzten maschinelle Lernmodelle, um retinaale Infektionsniveaus mit Markern wie Amyloid‑Beta-Ablagerungen, Entzündung und lokaler Gewebsdünnung zu kombinieren. Bestimmte Kombinationen — vor allem retinaale Bakterien zusammen mit Amyloid — unterschieden Alzheimer-Patienten von Kontrollen mit hoher Genauigkeit und korrelierten mit Krankheitsstadium und kognitiven Testergebnissen. Obwohl weitere Arbeiten und größere Studien nötig sind, deuten die Ergebnisse darauf hin, dass ein einfacher augenbasierter Test eines Tages nicht nur klassische Alzheimer-Veränderungen, sondern auch eine verborgene infektiöse Komponente aufdecken könnte, und so den Weg für frühere Antibiotikagaben oder Wirkstoffe, die das Inflammasom dämpfen, bei gefährdeten Personen öffnen würde.
Was das für Patientinnen und Patienten bedeuten könnte
Für Nicht‑Spezialisten ist die Kernaussage, dass Alzheimer nicht allein von fehlgeleiteten Proteinen getrieben sein muss; langanhaltende Infektionen könnten wie Brennstoff auf ein bereits schwelendes Feuer wirken. Diese Studie liefert starke Hinweise darauf, dass ein verbreitetes Atemwegsbakterium sich in Netzhaut und Gehirn ansiedeln, schädliche Entzündungen entfachen und bei anfälligen Personen den Gedächtnisverlust verschlechtern kann. Wenn künftige klinische Studien bestätigen, dass die Behandlung solcher Infektionen oder das Blockieren des Inflammasom‑Wegs den Abbau verlangsamt, könnten routinemäßige Netzhautbildgebung und gezielte Therapien Teil eines proaktiveren, personalisierten Ansatzes zur Verhinderung oder Verzögerung von Demenz werden.
Zitation: Gaire, B.P., Koronyo, Y., Vit, JP. et al. Identification of Chlamydia pneumoniae and NLRP3 inflammasome activation in Alzheimer’s disease retina. Nat Commun 17, 771 (2026). https://doi.org/10.1038/s41467-026-68580-4
Schlüsselwörter: Alzheimer-Krankheit, Netzhaut, Chlamydia pneumoniae, Neuroinflammation, Amyloid‑Beta