Clear Sky Science · de
HIF erhält einen transkriptionellen Regelkreis der EPAS1-Expression beim klarzelligen Nierenzellkarzinom
Warum Nierenkrebs genauer betrachtet werden muss
Das klarzellige Nierenzellkarzinom ist die häufigste Form von Nierenkrebs, und viele Patientinnen und Patienten erhalten inzwischen Medikamente, die ein Protein namens HIF‑2α blockieren. Diese Arzneien können Tumoren verkleinern, wirken aber nicht bei allen gleichermaßen gut. Diese Studie stellt eine einfache, aber wichtige Frage: Was bewirkt, dass manche Nierentumoren so viel HIF‑2α produzieren, und kann das Verständnis dieses "Ein/Aus-Schalters" helfen, vorherzusagen, wer am meisten von der Behandlung profitiert und wie neue Therapien gestaltet werden können?
Der Sauerstoffsensor, der aus dem Ruder läuft
Gesunde Nierenzellen nutzen ein Sicherheitsprotein namens VHL, um Sauerstoff-Sensoren, die als HIFs bekannt sind, streng zu kontrollieren. Wenn ausreichend Sauerstoff vorhanden ist, markiert VHL HIF-Proteine zur Zerstörung und verhindert so, dass sie Gene aktivieren, die Blutgefäßwachstum und Zellteilung fördern. Beim klarzelligen Nierenkrebs geht VHL in der Regel verloren oder ist geschädigt. Infolgedessen entkommt ein Mitglied der HIF-Familie, HIF‑2α (kodiert durch das EPAS1-Gen), der Zerstörung und reichert sich an. Frühere Arbeiten zeigten, dass hohe HIF‑2α-Aktivität mit schnellerem Tumorwachstum und schlechteren Ergebnissen verbunden ist und dass die Blockade von HIF‑2α Tumoren bei einigen Patienten verlangsamen oder stoppen kann. Die molekularen Schritte, die die Aktivität des EPAS1-Gens in Nierentumoren steigern, waren jedoch bislang nicht gut verstanden.
Ein verborgener DNA-Schalter für ein Krebsgen
Mithilfe von Tumorproben von Patientinnen und Patienten, Einzelzelldaten und Krebszellmodellen zeigen die Autorinnen und Autoren, dass die HIF‑2α-mRNA in klarzelligen Nierentumoren deutlich höher ist als in normalem Nierengewebe oder anderen Nierentumorarten. Sie durchforsten dann den EPAS1-Genbereich des Genoms nach chemischen und strukturellen Markern, die aktive regulatorische DNA anzeigen. Dadurch wird ein starker Enhancer sichtbar — eine Art Fernschalter für Gene — der etwa 70.000 DNA-Basenpaare stromaufwärts von EPAS1 liegt und spezifisch in klarzelligen Tumoren aktiv ist. In Tumorzellen ist die Chromatinstruktur an diesem Enhancer offen, mit Aktivierungsmarken versehen und bildet physische Schleifen zum EPAS1-Promotor, während diese Region in normalen Nierentubuluszellen weitgehend still ist. Die Aktivität dieses Enhancers korreliert in großen Krebsdatensätzen mit höheren EPAS1-Werten. 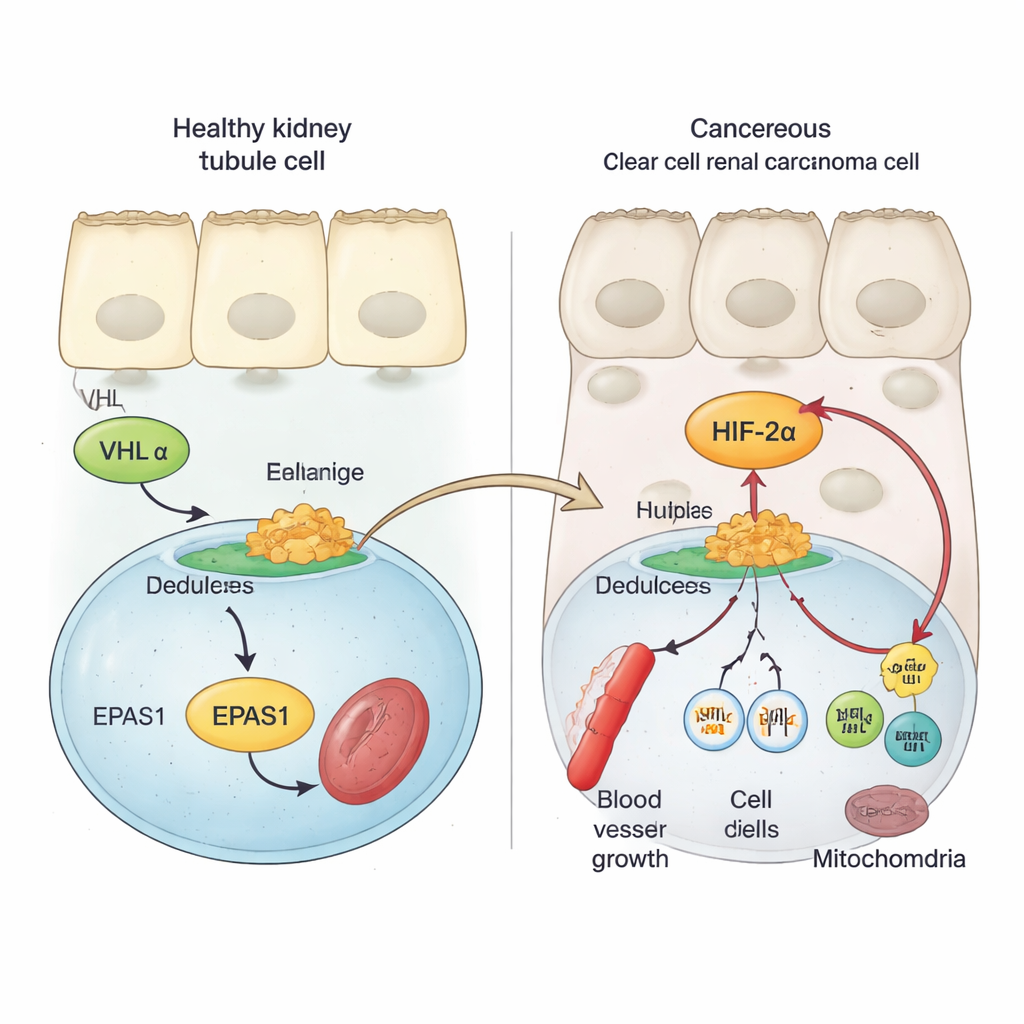
Ein sich selbst verstärkender Kreislauf, angetrieben von Nieren-Identitätsfaktoren
Die Studie zeigt, dass HIF-Proteine mehr tun, als nur auf Sauerstoffmangel zu reagieren — sie fördern tatsächlich ihre eigene Produktion. Wenn die Forschenden VHL wiederherstellen oder ein wichtiges HIF-Partnerprotein (HIF‑1β) entfernen, fallen die EPAS1-Werte und der Enhancer wird weniger zugänglich. Direkte Kartierungen von Protein–DNA-Kontakten zeigen, dass HIF an zwei Enhancer-Regionen stromaufwärts von EPAS1 bindet, einschließlich des klarzell-spezifischen Enhancers. In Nierentumorzellen ist dieser Enhancer außerdem von PAX8 und HNF‑1β besetzt, Transkriptionsfaktoren, die die Identität von Nierenzellen definieren und bekanntermaßen das Tumorwachstum unterstützen. Das Stören von PAX8 oder HNF‑1β bzw. das Mutieren ihrer Bindungsstellen innerhalb des Enhancers reduziert HIF‑2α-RNA und -Protein und schwächt die Enhancer-Aktivität. Zusammen enthüllen diese Befunde einen auto-regulatorischen Schaltkreis: HIF‑2α wirkt zusammen mit nieren-spezifischen Linienfaktoren, erhöht die Aktivität eines EPAS1-Enhancers, der wiederum mehr HIF‑2α-Produktion antreibt.
Genetisches Risiko und Tumorverhalten konvergieren auf denselben Kreislauf
Der EPAS1-Bereich wurde in genomweiten Studien schon lange als Hotspot für Nierenkrebsrisiko identifiziert, wobei bestimmte vererbte Varianten mit erhöhten Krebsraten und mit VHL-Mutationen in Tumoren verknüpft sind. Durch die Kombination genetischer Daten mit Genexpressionsmessungen zeigen die Autorinnen und Autoren, dass Personen mit der Hochrisiko-Version einer Schlüsselvarianten im EPAS1-Bereich tendenziell höhere HIF‑2α-Werte in ihren Tumoren haben — und sogar in normalen Nierentubuluszellen, wenn HIF experimentell stabilisiert wird. Das deutet darauf hin, dass erbliche DNA-Unterschiede die Empfindlichkeit des Enhancers modulieren können und manche Nieren darauf vorbereiten, nach dem Verlust von VHL stärker HIF‑2α hochzufahren. Experimente in Glioblastomzellen zeigen, dass derselbe Enhancer auch in bestimmten Hirntumoren aktiviert werden kann, was nahelegt, dass dieses regulatorische Modul in anderen Krebserkrankungen wiederverwendet wird, in denen HIF‑2α eine Rolle spielt. 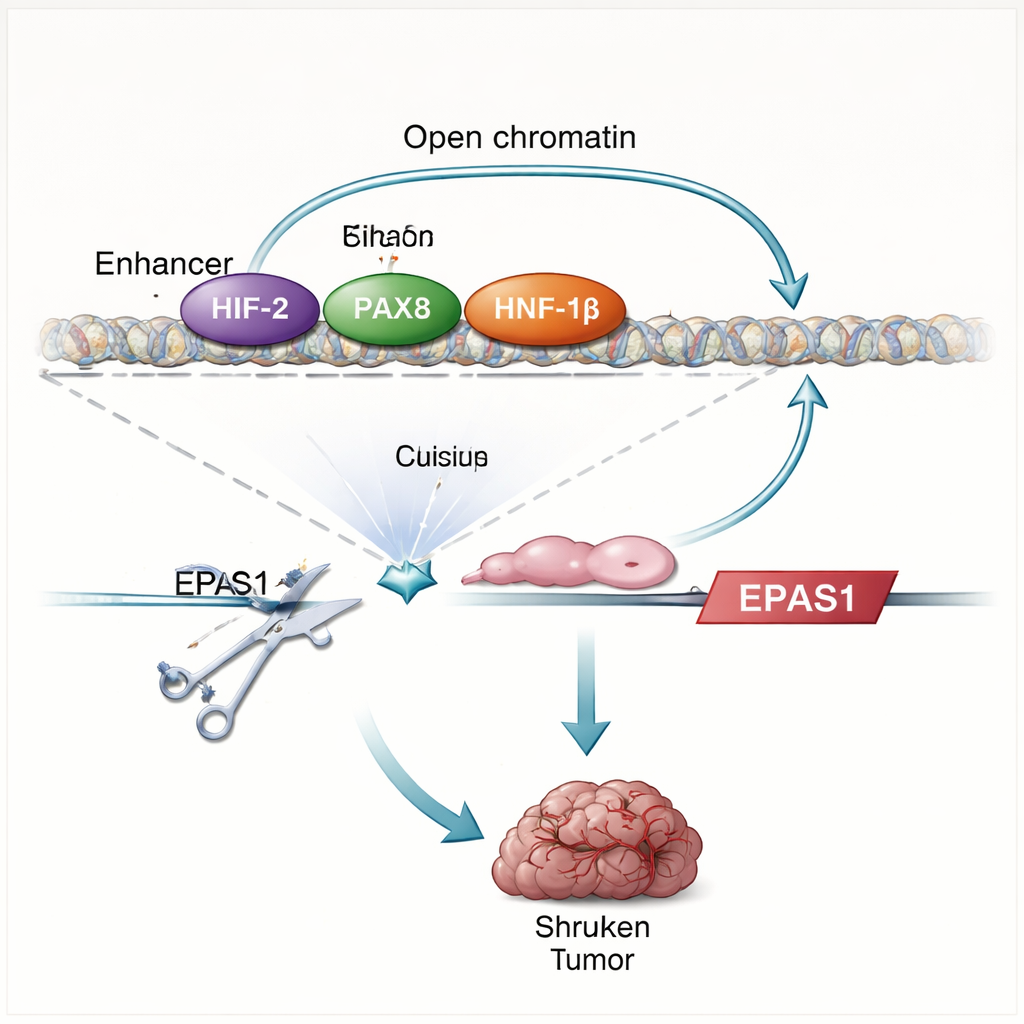
Den Kreislauf unterbrechen, um Tumorwachstum zu stoppen
Um zu testen, wie essentiell dieser Enhancer ist, verwenden die Forschenden die CRISPR-Genombearbeitung, um die HIF-Bindungsmotive innerhalb des Enhancers in Nierenkrebszelllinien und frischen Tumorzellen von Patientinnen und Patienten zu beschädigen. Dieser Eingriff reduziert die HIF‑2α-RNA um etwa ein Drittel bis die Hälfte, senkt die Spiegel bekannter HIF‑2α-Zielgene wie CCND1 und VEGFA und schwächt das breitere Hypoxie-Genprogramm. Wenn editierte Zellen in Mäuse implantiert werden, bilden sie größtenteils keine Tumoren, im starken Gegensatz zu Kontrollzellen. Das Muster der Genveränderungen nach Enhancer-Störung spiegelt die Effekte einer direkten Blockade von HIF‑2α mit einem klinischen Wirkstoff eng wider und unterstreicht, dass dieses einzelne DNA-Element ein Haupttreiber des HIF‑2α-Signalwegs in diesen Tumoren ist.
Was das für Patientinnen, Patienten und Therapien bedeutet
Für Nicht-Fachleute ist die Kernbotschaft, dass die Autorinnen und Autoren einen sich selbst verstärkenden DNA-Schalter entdeckt haben, der ein bedeutendes krebsförderndes Protein, HIF‑2α, in klarzelligen Nierentumoren eingeschaltet hält. Dieser Schalter hängt sowohl vom Verlust der VHL-Sicherungsbremse als auch von nieren-spezifischen Helferproteinen ab und wird durch vererbte genetische Varianten beeinflusst. Da der Enhancer in vielen klarzelligen Tumoren hochaktiv ist und eng mit der Stärke des HIF‑2α-Signalwegs verknüpft ist, könnte die Messung seiner Aktivität — oder das direkte Anvisieren — helfen, Patientinnen und Patienten zu identifizieren, die am meisten von bestehenden HIF‑2α-Inhibitoren profitieren, und neue Wege eröffnen, diesen Signalweg zu blockieren, wenn Tumoren medikamentenresistent werden.
Zitation: Naas, S., Krüger, R., Grampp, S. et al. HIF sustain a transcriptional regulatory circuit of EPAS1 expression in renal clear cell carcinoma. Nat Commun 17, 1764 (2026). https://doi.org/10.1038/s41467-026-68576-0
Schlüsselwörter: klarzelliges Nierenzellkarzinom, HIF-2α, EPAS1-Enhancer, VHL-Mutation, Genetik von Nierenkrebs