Clear Sky Science · de
Der Toll-Signalweg von Insekten aktiviert antibakterielle Immunität gegen den Huanglongbing-Erreger der Zitrusgewächse
Wie winzige Insekten ein großes Zitrusproblem beeinflussen
Citrus Huanglongbing, auch Zitrus‑Greening genannt, ist eine der zerstörerischsten Krankheiten, die Orangen‑ und andere Zitrushaine weltweit bedroht. Der Übeltäter ist ein schwer kultivierbares Bakterium, das im Pflanzensaft verborgen lebt und von einem saugenden Insekt, dem Asiatischen Zitruspsylliden, verbreitet wird. Diese Studie stellt eine einfache, aber entscheidende Frage: Wie erkennt dieses winzige Insekt das eindringende Bakterium, und warum gelingt es dem Mikroben, im Inneren des Insekts zu persistieren, ohne es zu töten? Die Antworten offenbaren ein überraschend ausgereiftes Immunwarnsystem im Insekt — und eine ebenso raffinierte Gegenmaßnahme des Bakteriums.
Die Krankheit, das Insekt und die verborgene Schlacht
Das Bakterium Candidatus Liberibacter asiaticus (CLas) lebt im Phloem, dem Pflanzengewebe, das zuckerreichen Saft transportiert. Asiatische Zitruspsylliden saugen an diesem Saft und übertragen das Bakterium von kranken auf gesunde Bäume. Junge Psylliden nehmen den Erreger am effizientesten auf, während adulte Tiere ihn besser weitergeben. Merkwürdigerweise macht CLas die Insekten offenbar nicht deutlich krank, was darauf hindeutet, dass das Immunsystem des Psylliden die Infektion gerade so kontrolliert, dass sowohl Wirt als auch Mikroben überleben. Bislang war nicht bekannt, wie das Insekt dieses spezielle Bakterium erkennt oder welche inneren Abwehrmechanismen es in Schach halten. 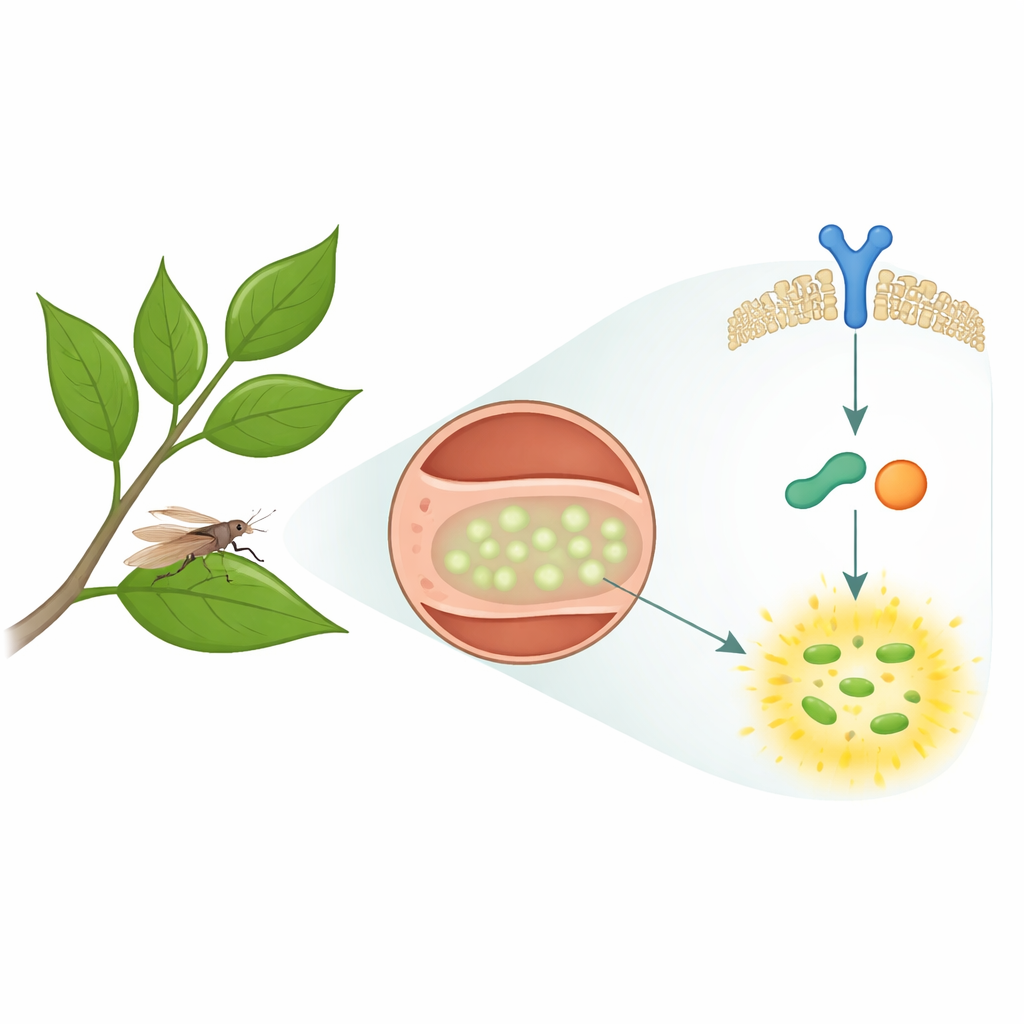
Ein direkter Frühwarnsensor auf den Zellen des Insekts
Die Forscher entdeckten, dass ein Rezeptorprotein auf den Psyllidenzellen, Toll8 genannt, als vorderster Sensor für CLas dient. Bei vielen Insekten sprechen ähnliche Rezeptoren nur indirekt an und sind auf andere Moleküle angewiesen, die zuerst eindringende Mikroben erkennen. Hier verhält sich Toll8 eher wie bekannte Immunsensoren bei Menschen und anderen Wirbeltieren. Es bindet direkt an ein kleines, fassförmiges Protein, das in der Außenmembran des Bakteriums sitzt. Wenn dieses Fassprotein Toll8 berührt, paaren sich die Rezeptoren an der Zelloberfläche und bilden ein Dimer, das ein internes Alarmsignal aktiviert. Die Stilllegung des Toll8‑Gens in Psylliden führte zu einem starken Anstieg der Bakterienzahlen, was zeigt, dass dieser einzelne Sensor ein Schlüsselbestandteil ihrer antibakteriellen Abwehr ist.
Vom Alarmsignal zu Abwehrwaffen
Sobald Toll8 aktiviert ist, löst es eine Kaskade innerhalb der Insektenzelle aus. Zunächst wird ein Adapterprotein namens MyD88 zum aktivierten Rezeptor gezogen und paart sich mit einer weiteren Kopie von sich selbst. Dieser Komplex rekrutiert dann eine Kinase — einen molekularen Schalter — namens IKKE, die chemisch aktiviert wird. IKKE verändert daraufhin einen Transkriptionsfaktor namens NFAT, sodass dieser in den Zellkern gelangen kann, wo das genetische Material gespeichert ist. Im Kern bindet NFAT an spezifische DNA‑Abschnitte und steigert die Aktivität mehrerer Abwehrgene. Zwei der wichtigsten Effektorprodukte sind Reeler, ein sezerniertes Protein, das Bakterien direkt abtöten kann, und die Stickstoffmonoxid‑Synthase (NOS), die Stickstoffmonoxid erzeugt, ein kleines, reaktives Gas mit breiter mikrobenabtötender Wirkung. Die Störung von MyD88, IKKE, NFAT, Reeler oder NOS führte jeweils zu vermehrter CLas‑Vermehrung und erhöhte die Wahrscheinlichkeit, dass Psylliden das Bakterium an neue Zitrusblätter weitergeben.
Wie das Bakterium zurückkämpft
CLas blieb in diesem Rüstungswettlauf nicht passiv. Das Team fand heraus, dass das Bakterium ein weiteres Protein namens SDE3230 in Psyllidenzellen freisetzt. Dieses Protein greift Toll8 nicht direkt an. Stattdessen bindet es an ein Wirtsenzym, eine E3‑Ubiquitin‑Ligase namens UBR5, dessen Aufgabe es ist, andere Proteine für den Abbau zu markieren. Mit Hilfe von SDE3230 versieht UBR5 MyD88 effizienter mit molekularen "Markierungen", die es zur zellulären Protein‑Zerlegungsmaschinerie schicken. Mit abnehmenden MyD88‑Spiegeln wird der gesamte Toll8–IKKE–NFAT‑Weg geschwächt, die Produktion von Reeler und Stickstoffmonoxid sinkt, und CLas erhält mehr Freiheit zu wachsen und zu persistieren. 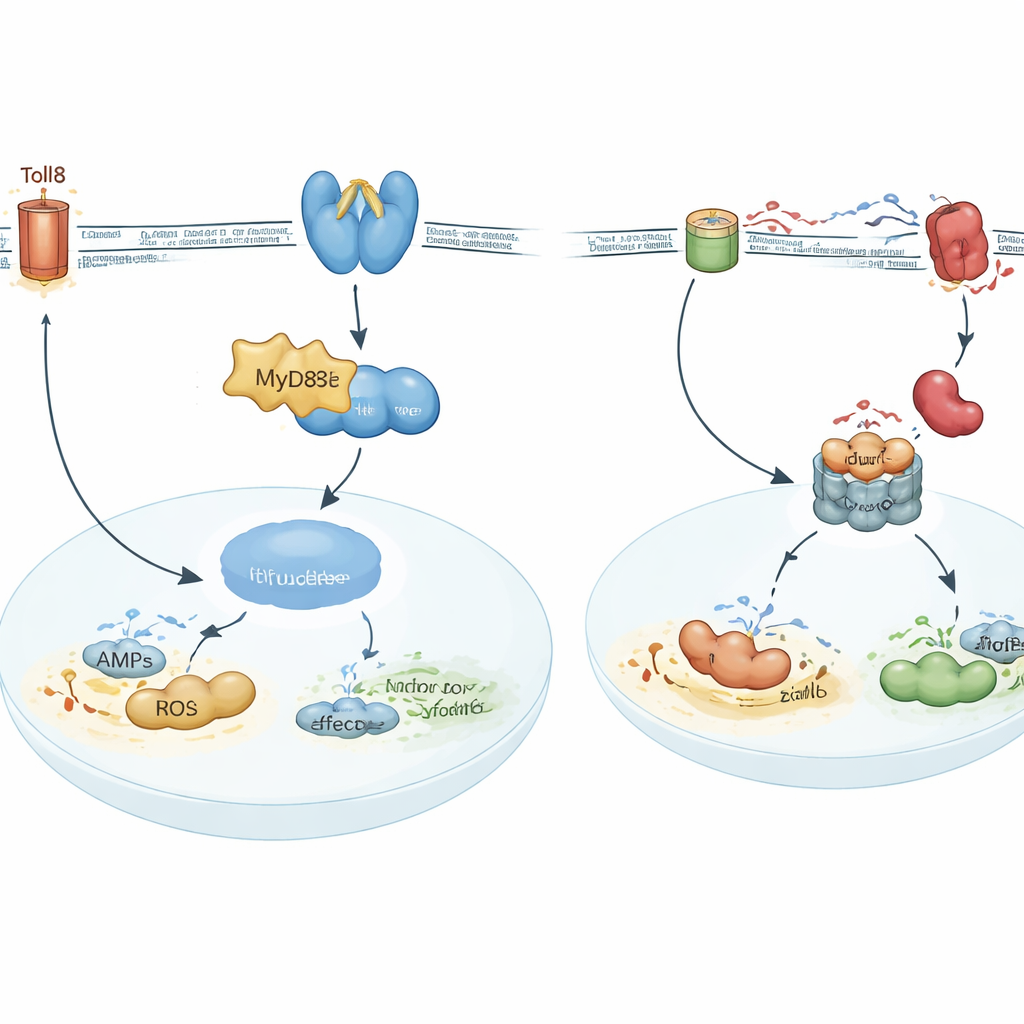
Was das für den Schutz von Zitrusbeständen bedeutet
Insgesamt zeigt die Studie ein komplexes Geben und Nehmen zwischen dem Zitrus‑Greening‑Bakterium und seinem Insektenvektor. Auf der einen Seite nutzt der Psyllide Toll8 als direkten Sensor zur Erkennung von CLas und leitet das Signal über MyD88, IKKE und NFAT weiter, um potente antibakterielle Mittel zu aktivieren. Auf der anderen Seite setzt CLas SDE3230 ein, um diesen Weg zu sabotieren, indem der Abbau von MyD88 beschleunigt wird und so die Abwehr des Insekts abgeschwächt wird — gerade genug, damit das Bakterium überleben und übertragen werden kann. Für den Laien lautet die zentrale Botschaft: Die Ausbreitung der Krankheit in Zitrushainen wird nicht nur durch Vorgänge im Baum bestimmt, sondern auch durch ein molekulares Duell im Insektenvektor. Das Verständnis dieses Duells eröffnet neue Möglichkeiten: Zukünftige Kontrollstrategien könnten die Toll8‑basierten Abwehrkräfte der Psylliden stärken oder die bakteriellen Tricks blockieren, die sie lahmlegen, und so die Ausbreitung von Zitrus‑Greening verlangsamen oder sogar stoppen.
Zitation: Du, Y., Sun, M., Xiao, Y. et al. The insect Toll pathway activates antibacterial immunity against the citrus Huanglongbing pathogen. Nat Commun 17, 2721 (2026). https://doi.org/10.1038/s41467-026-68575-1
Schlüsselwörter: Zitrus‑Greening, Asiatischer Zitruspsyllide, angeborene Immunität, Toll‑Signalgebung, vektorübertragene Bakterien