Clear Sky Science · de
Atroposelektive unterbrochene CuAAC-Reaktion mit zyklischen Diaryliodonium-Verbindungen
Warum diese neue Chemie wichtig ist
Chemikerinnen und Chemiker verlassen sich seit langem auf eine einfache „Click“-Reaktion, um molekulare Bausteine schnell und sauber zusammenzufügen — ein Trick, der von der Wirkstoffforschung bis zu selbstheilenden Materialien vieles möglich macht. Dieser Beitrag beschreibt eine geschickte Variation dieser klassischen Click-Reaktion, mit der sich komplexere, dreidimensionale Moleküle mit präziser Händigkeit herstellen lassen — Strukturen, die in modernen Arzneimitteln und fortschrittlichen Materialien besonders geschätzt werden.
Ein klassischer Click-Reaktion eine neue Aufgabe geben
Ausgangspunkt ist die kupferkatalysierte Azid–Alkin-Cycloaddition, meist kurz CuAAC genannt. Sie verbindet zwei kleine Komponenten — ein Azid und ein Alkin — zu einem fünfgliedrigen Ring, dem Triazol, unter milden Bedingungen und mit bemerkenswerter Zuverlässigkeit. Klassischerweise endet die Reaktion, sobald Kupfer den Triazolring gebildet hat. In den letzten Jahren haben Chemiker jedoch gelernt, diesen Prozess zu „unterbrechen“ und ein kurzlebiges Kupfer–Triazol-Intermediat mit einer dritten Komponente einzufangen, um aufwendigere Produkte zu bauen. Bislang konnten solche Unterbrechungen die molekulare Händigkeit (Chiralität) nicht allgemein steuern, was ihre Nützlichkeit für die Synthese anspruchsvoller, chiraler Moleküle begrenzte.
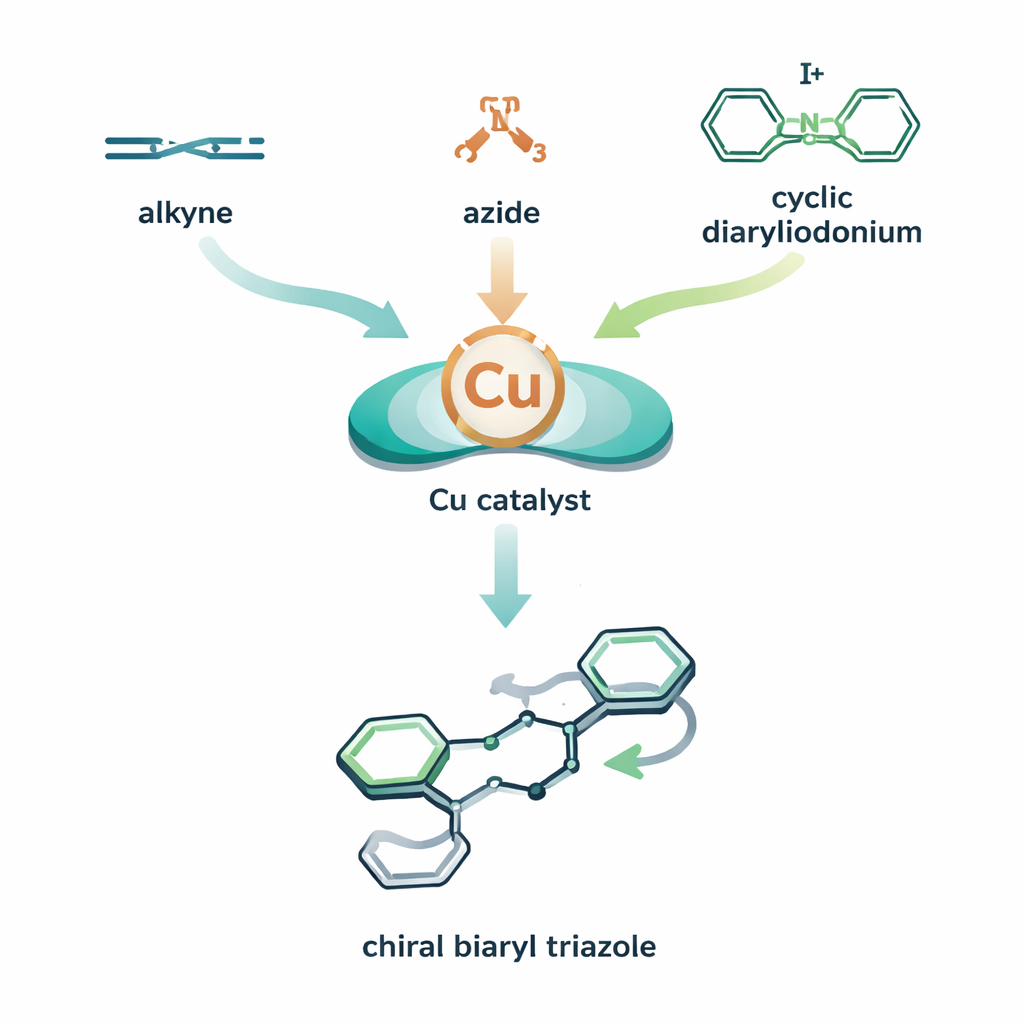
Ein dreiteiliges molekulares Puzzle mit Drehung
Die Autorinnen und Autoren kombinieren zwei kupferbasierte Reaktionszyklen zu einem einzigen, orchestrierten Prozess. In ihrem Konzept hilft ein Kupferkatalysator zunächst dem Alkin und dem Azid, ein Kupfer–Triazol-Intermediat zu bilden. Bevor dieses Intermediat neutralisiert wird, wird eine dritte Komponente — ein ringförmiges, hochreaktives, jodhaltiges Molekül, ein zyklisches Diaryliodonium — hinzugefügt. Kupfer inseriert in diesen Ring und öffnet ihn anschließend, wobei eines der aromatischen Ringe an das Triazol angefügt wird. Das Ergebnis ist ein biaryles Triazol: zwei Ringsysteme, verbunden über eine Bindung, die als chirale Achse wirken kann, ähnlich einer Schraubenflügel-Propellern, die nach links oder rechts gedreht sein kann. Durch die Kombination von Kupfer mit einem sorgfältig gewählten chiralen Liganden lenkt das Team den Prozess so, dass eine Form der Drehung deutlich bevorzugt wird und hohe Atroposelektivität (Kontrolle darüber, welche axiale „Hand“ entsteht) erreicht wird.
Prüfung von Flexibilität und Zuverlässigkeit der Methode
Um zu verstehen, wie allgemein diese Reaktion einsetzbar ist, variierten die Forschenden systematisch jede der drei Bausteine. Sie zeigten, dass viele verschiedene Alkine, einschließlich solcher mit elektronenspendenden, elektronenziehenden und heteroaromatischen Ringen, teilnehmen können und dennoch gute Ausbeuten sowie eine starke Präferenz für eine chirale Form liefern. Bestimmte sperrige Substitutionen verbesserten die Selektivität, konnten aber die Ausbeute verringern und zeigten damit einen Zielkonflikt zwischen sterischer Behinderung und Effizienz. Die Azidpartner funktionierten am besten, wenn sie von einfachen Ester- oder Amidgruppen oder von benzylichen Positionen abstammten; eine Reihe solcher Azide lieferte stark angereicherte chirale Produkte. Auch die zyklische Diaryliodonium-Komponente ließ sich abstimmen: Einige Substitutionen erhielten sowohl Ausbeute als auch Selektivität, während andere, besonders in der Nähe des reaktiven Jod-Zentrums, die Reaktion verlangsamten oder die Leistung minderten. Insgesamt lieferte die Studie eine breite Palette neuer atropoisomerer biaryler Triazole, die in einem Schritt zugänglich sind.
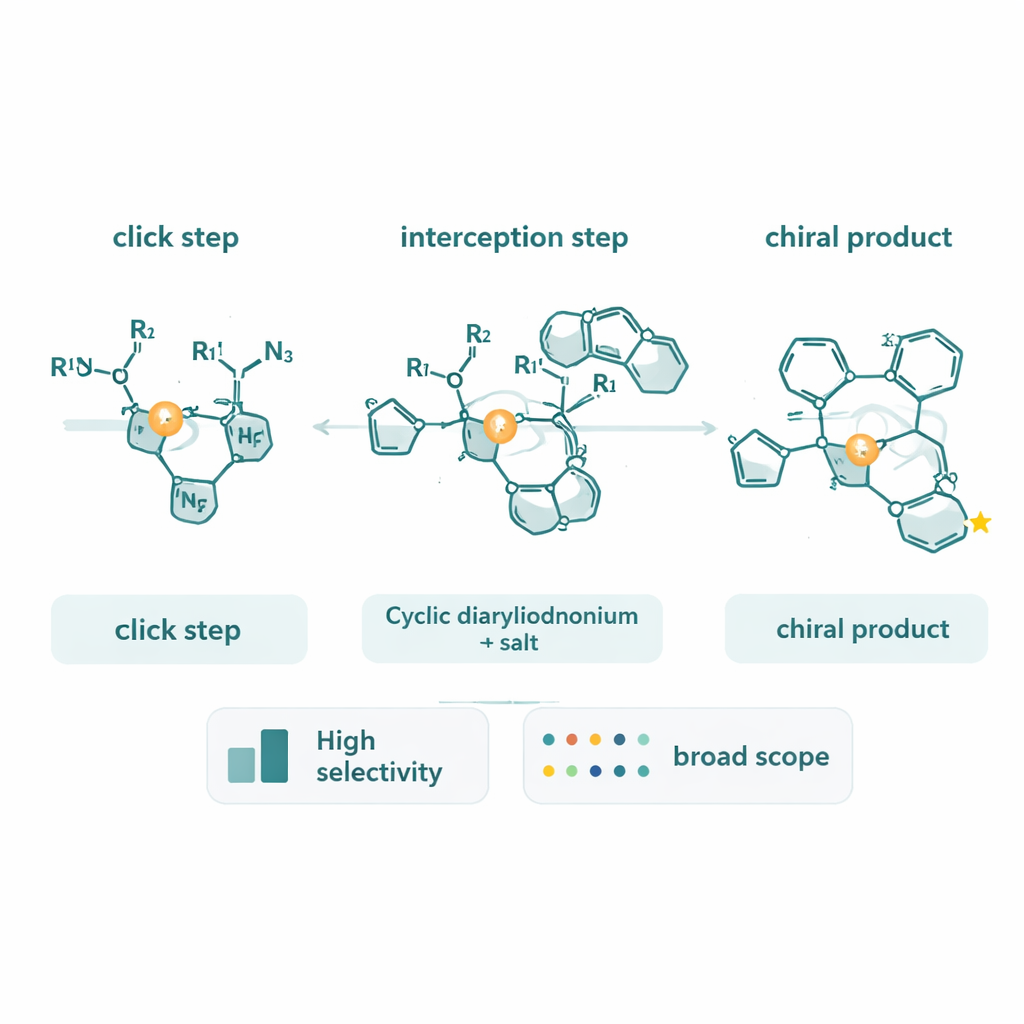
Ein Blick unter die Haube der Reaktion
Über die Herstellung neuer Moleküle hinaus widmete das Team erhebliche Anstrengungen der Frage, wie die Reaktion tatsächlich abläuft. Mit deuteriummarkierten Alkinen beobachteten sie einen ungewöhnlichen inversen kinetischen Isotopeneffekt, der auf einen geschwindigkeitsbestimmenden Schritt hindeutet, bei dem sich der Bindungscharakter des Alkin-Kohlenstoffs ändert, statt dass einfach eine C–H-Bindung gebrochen wird. Kalorimetriebasierte Analysen des Reaktionsverlaufs zeigten, dass die Reaktionsgeschwindigkeit stark von den Konzentrationen des Alkins und des Azids abhängt, aber nur schwach vom zyklischen Diaryliodonium. Diese Messungen stützen ein Bild, in dem die Bildung und Umwandlung des Kupfer–Triazol-Komplexes und dessen oxidative Addition in den Diaryliodonium-Ring gemeinsam das Tempo der Reaktion bestimmen. Sie fanden außerdem, dass die chiralen Triazolprodukte selbst am Kupfer anhaften und den Katalysator verlangsamen können, was Hinweise zur weiteren Optimierung des Systems liefert.
Was das für die Zukunft bedeutet
Anschaulich gesprochen haben die Forschenden einer bekannten Click-Reaktion einen neuen Trick beigebracht: Statt einfach zwei Teile zusammenzuklinken, hilft sie nun, drei Komponenten zu komplexen, propellerartigen Molekülen zusammenzusetzen und dabei nahezu ausschließlich eine bevorzugte Drehung zu erzeugen. Das bietet eine skalierbare Route zu chiralen biarylen Triazolen — Strukturen, die als potenzielle Wirkstoffmoleküle, Katalysatoren und funktionale Materialien wertvoll sind. Die mechanistischen Erkenntnisse — besonders wie das Schlüsselintermediat abgefangen wird und wie das Produkt den Katalysator „vergiften“ kann — bieten eine Wegkarte zur Entwicklung noch effizienterer und selektiverer Versionen dieser Chemie. Für Nichtfachleute ist die wichtigste Erkenntnis, dass ein bereits leistungsfähiges molekulares „Lego“-Werkzeug jetzt vielseitiger geworden ist und Chemikerinnen und Chemikern erlaubt, komplexere und nützlichere Formen mit feiner Kontrolle über deren dreidimensionale Gestalt zu bauen.
Zitation: Li, Y., Yang, S., Duan, L. et al. Atroposelective interrupted CuAAC reaction using cyclic diaryliodoniums. Nat Commun 17, 944 (2026). https://doi.org/10.1038/s41467-026-68574-2
Schlüsselwörter: Click-Chemie, Kupferkatalyse, chiraler Biaryl, Atropisomer, Triazol