Clear Sky Science · de
Ein mikro‑physiologischer menschlicher Mini‑Blase enthüllt das Zusammenspiel von Urin und Urothel bei Geweberesilienz und UPEC‑Rezidiven bei Harnwegsinfektionen
Warum der Zustand Ihres Urins wichtig ist
Die meisten von uns sehen Urin nur als Abfallprodukt, doch seine Zusammensetzung ändert sich ständig mit dem, was wir trinken, essen und wie gesund wir sind. Diese Studie zeigt, dass diese Veränderungen keine unverfängliche Hintergrundvariabilität sind: Sie können direkt beeinflussen, wie gut die Blase sich gegen Harnwegsinfektionen (HWI) verteidigt und wie leicht Infektionen nach einer Antibiotikabehandlung wiederkehren. Mithilfe einer winzigen, im Labor gezüchteten „Mini‑Blase“ zeigen die Forschenden, wie konzentrierter Urin das Blasengewebe still und leise schwächen kann und Krankheitserregern neue Wege eröffnet, sich zu verbergen und Behandlungen zu überdauern.
Eine Mini‑Blase im Labor aufbauen
Um diese verborgenen Dynamiken zu untersuchen, entwickelten die Forschenden eine daumengroße menschliche „Mini‑Blase“ auf einem mikrofluidischen Chip. Sie besäten menschliche Blasenoberflächenzellen in ein weiches 3D‑Gerüst und veranlassten sie, mehrere geordnete Schichten zu bilden, ähnlich der echten Blasenauskleidung. Die obersten „Schirmchen“-Zellen bildeten eine dichte, auslaufsichere Barriere, während tiefere Schichten Zellen enthielten, die das Gewebe im Laufe der Zeit erneuern können. Das Gerät ließ außerdem urinähnliche Flüssigkeit durch einen zentralen Kanal fließen und ermöglichte ein sanftes Dehnen und Entspannen des Gewebes, wodurch Füll‑ und Entleerungszyklen einer echten Blase nachgeahmt wurden. Strukturtests und hochauflösende Bildgebung bestätigten, dass dieses Mini‑Organ dem Vollorgan in vielerlei Hinsicht ähnelt.
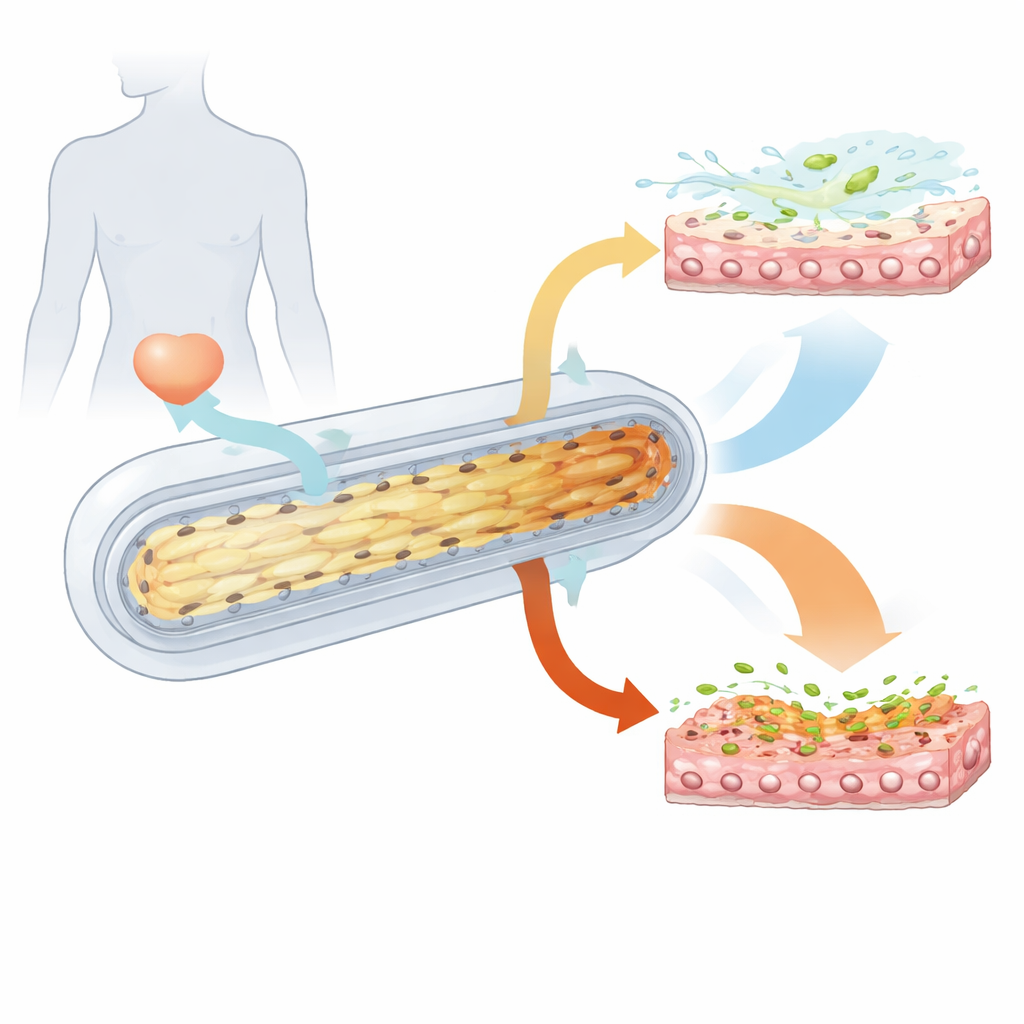
Wenn der Urin rau wird
Der menschliche Urin kann je nach Flüssigkeitsaufnahme und Gesundheitszustand stark verdünnt oder stark konzentriert sein. Die Forschenden stellten zwei synthetische Harnmischungen her: eine „niedrig‑gelöste“ und eine „hoch‑gelöste“, die den unteren bzw. oberen Bereich natürlicher Urinkonzentrationen abbilden. Wurden Mini‑Blasen über mehrere Tage in hoch‑gelöstem Urin belassen, verschlechterte sich das Gewebe allmählich. Mehr Zellen starben, die Gesamtzellzahl nahm ab und die normalerweise dichten Verbindungen zwischen den Zellen wurden undicht. Muster in der Genaktivität zeigten verminderte Zell‑Zell‑Adhäsion, schwächere Gewebeerneuerung und abgeschwächte angeborene Immunantworten. Im Gegensatz dazu förderte niedrig‑gelöster Urin das Zellwachstum, stärkere Tight Junctions und eine gesündere Differenzierung der Blasenschleimhaut. Kurz gesagt: wiederholte Exposition gegenüber sehr konzentriertem Urin machte das Gewebe strukturell schwächer und weniger bereit, eine frühe Immunabwehr zu starten.
Wie schwaches Gewebe Infektionen begünstigt
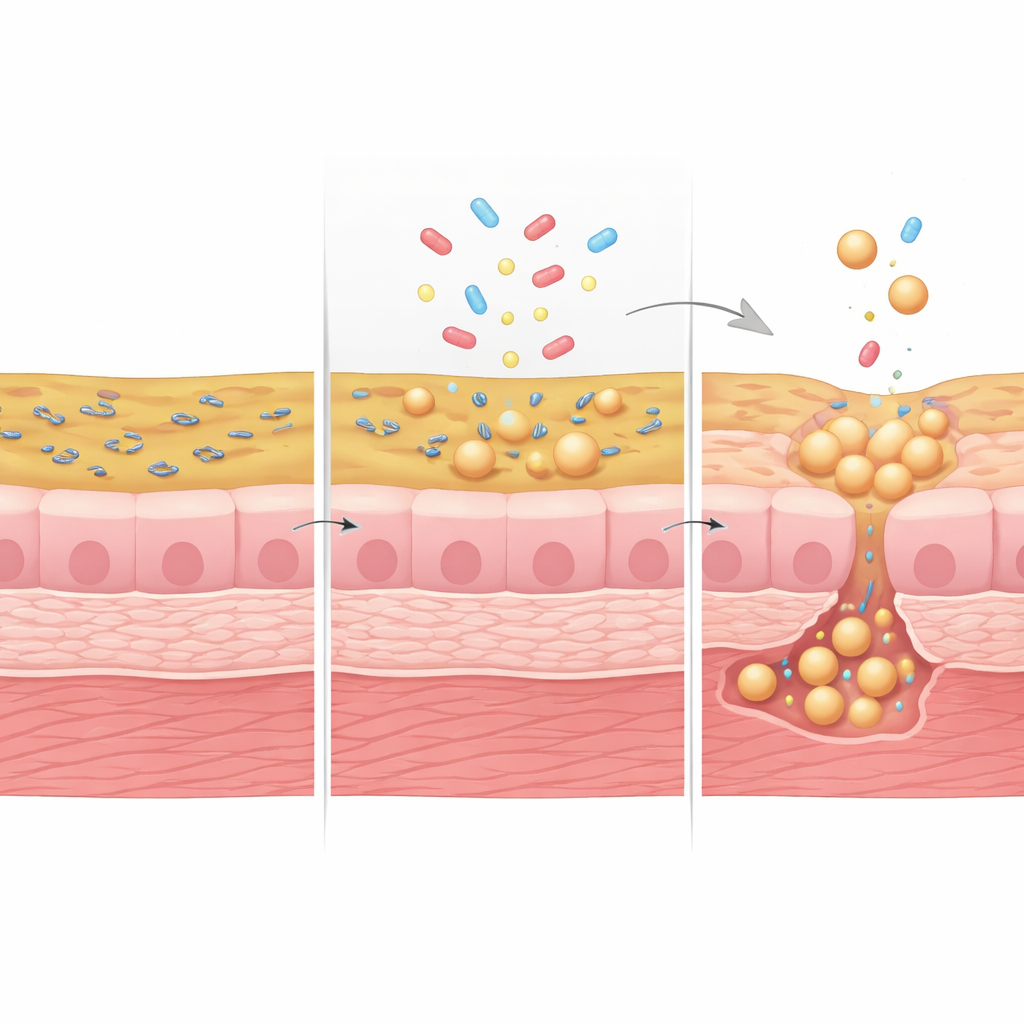
Das Team infizierte anschließend die Mini‑Blasen mit uropathogenen Escherichia coli (UPEC), dem wichtigsten bakteriellen Erreger von HWIs, und spülte den Kanal periodisch, um das Wasserlassen zu imitieren. Nach jedem „Entleeren“ wurden viele Bakterien ausgespült, doch einige blieben an der Blasenoberfläche haften oder drangen in das Epithel ein und bildeten allmählich eine versteckte, gewebsassoziierte Population. Indem die Forschenden den wichtigsten Haftmechanismus der Bakterien mit einem Zucker, D‑Mannose, blockierten, reduzierten sie diese eingebettete Population und beobachteten weniger Gewebeschäden — ein Hinweis darauf, dass Bakterien auf und in dem Gewebe helfen, den Urin zwischen den Entleerungen wieder zu besiedeln. Wenn Mini‑Blasen zuvor hoch‑gelöstem Urin ausgesetzt waren, drangen mehr Bakterien ins Gewebe ein und gängige Antibiotika wie Ciprofloxacin konnten sie schlechter beseitigen, obwohl frei schwimmende Bakterien im Urin weiterhin effektiv entfernt wurden.
Verborgene Überlebende nach Antibiotika
Die Beobachtungen wurden noch eindrücklicher mit Fosfomycin, einem häufig verschriebenen Antibiotikum, das die bakterielle Zellwand angreift. In hoch‑gelöstem Urin war Fosfomycin wenig wirksam bei der Reduktion der bakteriellen Last, und frei schwimmende Bakterien wandelten sich oft von stäbchenförmigen in große, fragile, zellwanddefiziente Kugeln. Ähnliche kugelige Formen wurden auch im Urin von Patientinnen und Patienten mit wiederkehrenden HWIs beobachtet. Mit fortgeschrittener 3D‑Elektronenmikroskopie kombiniert mit Fluoreszenzbildgebung fanden die Forschenden heraus, dass solche kugeligen Bakterien nicht nur im Urin schwebten, sondern sich auch zwischen und unter Blasenzellen tief in der Mini‑Blasenwand eingenistet hatten. Diese geschützten Formen überlebten die Behandlung und trugen später zum Wiederaufwachsen der Bakterien bei, was erklärt, warum Infektionen nach einer kurzzeitigen Besserung erneut aufflammen können.
Was das für Patientinnen und Patienten bedeutet
Diese Arbeit zeigt, dass die Umgebung der Blase nicht nur Kulisse ist, sondern aktiv den Verlauf von Infektion und Behandlung beeinflusst. Konzentrierter Urin schwächt die Blasenschleimhaut, dämpft ihre Immunabwehr und erlaubt Bakterien, tiefer einzudringen und spezielle, zellwanddefiziente Formen anzunehmen, die sowohl für Antibiotika als auch für Immunzellen schwer zu eliminieren sind. Die neue Mini‑Blasen‑Plattform macht deutlich, wie Urinzusammensetzung, Gewebe‑Gesundheit und bakterielles Verhalten eng verknüpft sind. Für Personen mit Neigung zu wiederkehrenden HWIs können Faktoren, die den Urin konzentrieren — etwa zu geringe Flüssigkeitszufuhr oder bestimmte Erkrankungen — still das Risiko erhöhen, indem sie die Geweberesilienz untergraben und versteckte Bakterienreservoire fördern. Das Verständnis und letztlich die gezielte Anpassung dieses Mikromilieus, kombiniert mit besseren Antibiotika‑Strategien, könnte entscheidend sein, um den Kreislauf wiederkehrender Infektionen zu durchbrechen.
Zitation: Paduthol, G., Nikolaev, M., Sharma, K. et al. A microphysiological human mini-bladder reveals urine-urothelium interplay in tissue resilience and UPEC recurrence in urinary tract infections. Nat Commun 17, 2322 (2026). https://doi.org/10.1038/s41467-026-68573-3
Schlüsselwörter: Harnwegsinfektion, Blasen‑Organoid, uropathogene E. coli, Antibiotika‑Toleranz, Urin‑Konzentration