Clear Sky Science · de
Biomarker für das Ansprechen auf neoadjuvantes Palbociclib plus Anastrozol bei endokrin‑resistentem, östrogenrezeptorpositivem/HER2‑negativem Brustkrebs: eine Phase‑2‑Studie
Warum diese Forschung für Patientinnen und Familien wichtig ist
Viele Frauen mit einer verbreiteten Form von Brustkrebs sprechen zunächst gut auf hormonsenkende Therapien an, doch die Tumoren werden mit der Zeit resistent und beginnen wieder zu wachsen. Diese Studie stellt eine drängende Frage: Kann das Hinzufügen eines neueren, den Zellzyklus blockierenden Medikaments zur Standardhormontherapie in diesen schwer behandelbaren Fällen helfen, und lassen sich im Tumor Vorzeichen finden, die vorhersagen, wer davon profitiert und wer nicht?
Ein genauerer Blick auf hartnäckige Brustkrebse
Die Studie konzentrierte sich auf östrogenrezeptor‑positive, HER2‑negative Brustkrebse, den häufigsten Subtyp. Alle 34 Patientinnen hatten bereits die standardmäßige präoperative Hormontherapie (einen Aromatasehemmer) erhalten, zeigten jedoch weiterhin aktive Tumorzellteilung, sodass der Krebs als „endokrin‑resistent“ eingestuft wurde. Die Teilnehmenden wurden vor der Operation mit einer Kombination aus dem Hormonpräparat Anastrozol und dem Zellzyklushemmer Palbociclib behandelt. Die Forschenden bestimmten die Teilungsrate der Tumorzellen mittels des Markers Ki67. Fiel Ki67 nach zwei Wochen auf sehr niedrige Werte, galt der Tumor als in „vollständigem Zellzyklus‑Stillstand“, was darauf hinweist, dass die Zellteilung effektiv unterdrückt war.
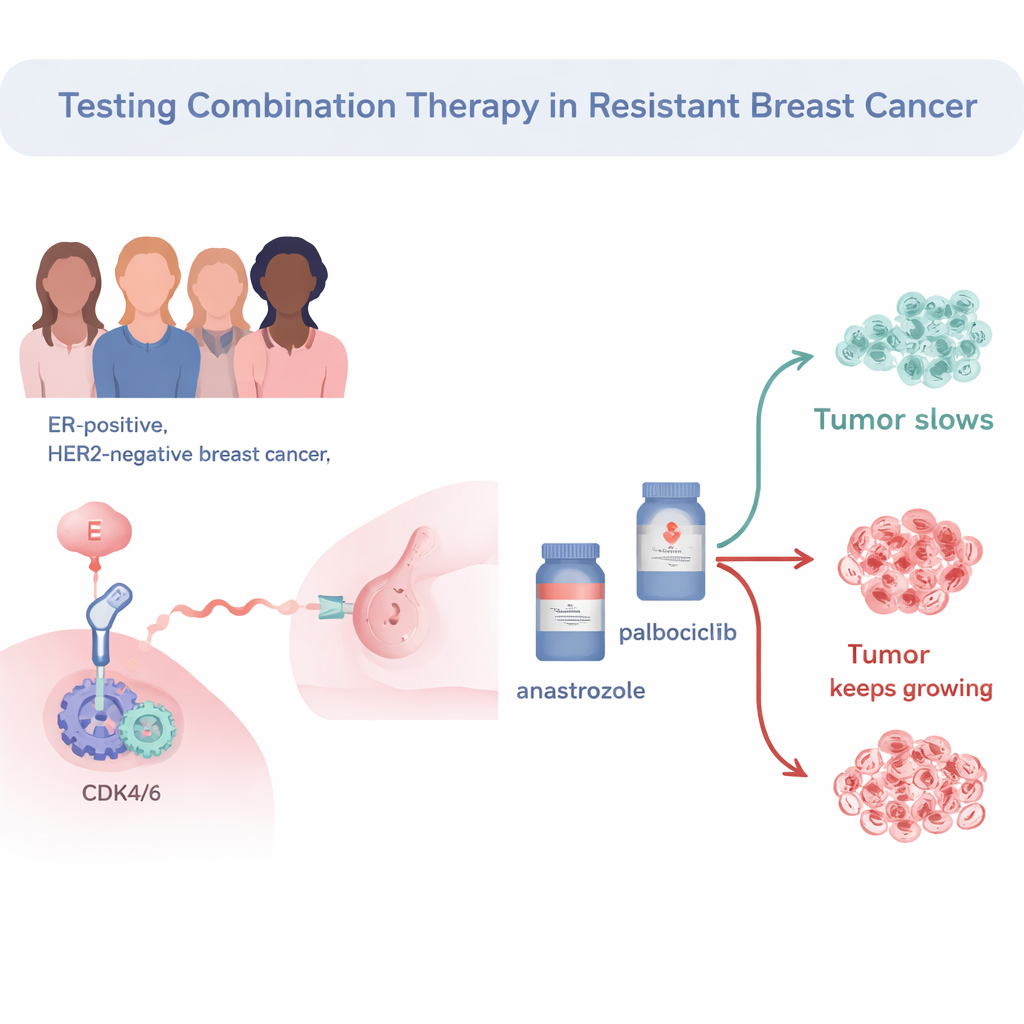
Wer sprach auf die Medikamentenkombination an?
Unter den 33 Patientinnen, deren Tumoren vollständig ausgewertet werden konnten, erreichten 57,6 % nach nur zwei Wochen der Kombinationsbehandlung den vollständigen Zellzyklus‑Stillstand. Bei Anwendung einer weniger strengen Schwelle — indem Tumoren als „sensitiv“ klassifiziert wurden, wenn Ki67 unter 10 % fiel — wurden etwa zwei Drittel der Tumoren als ansprechbar beurteilt. Patientinnen, deren Tumoren auch weiterhin hohe Ki67‑Werte zeigten, hatten tendenziell aggressivere Tumoren: höheres Grading, größere Tumorgröße und höhere Ausgangswerte von Ki67. Diese Tumoren gehörten außerdem häufiger zu sogenannten „non‑luminalen“ molekularen Subtypen, die im Allgemeinen aggressiver verlaufen als die klassischen hormongetriebenen „luminal A“‑Tumoren.
Was macht manche Tumoren resistent gegen die Behandlung?
Das Team ging über einfache Ansprechraten hinaus und analysierte Tumorproben umfassend mittels DNA‑Sequenzierung, RNA‑Sequenzierung und Proteinanalyse. Resistente Tumoren ließen sich nicht durch eine einzige Mutation definieren; vielmehr zeigten sie ein Muster einer „überaktiven Verdrahtung“. Im Vergleich zu sensiblen Tumoren wiesen resistente Karzinome abgeschwächte Östrogenrezeptor‑Signale, aber stärkere Aktivität in Pfaden auf, die Zellteilung und Wachstum antreiben — etwa Zellzyklusgene, den mTOR‑Wachstumspfad sowie mehrere entzündliche und Interferon‑vermittelte Netzwerke. Zudem zeigten sie höhere Werte von immunologischen „Bremsen“, den sogenannten Immuncheckpoints, einschließlich Genen wie IDO1 und PD‑L1, die dem Tumor helfen können, der körpereigenen Abwehr zu entkommen.
Von Signalwegen zu möglichen neuen Therapien
Um zu prüfen, ob sich diese überaktiven Signalwege therapeutisch ausnutzen lassen, erzeugten die Forschenden Laborzellmodelle, die gegen CDK4/6‑Inhibitoren wie Palbociclib resistent geworden waren. Diese resistenten Zellen zeigten dasselbe Profil erhöhter Zellzyklus‑ und Interferon/entzündlicher Signalgebung, das auch in den Tumoren der Patientinnen beobachtet wurde. Bei Behandlung mit Wirkstoffen, die die JAK‑STAT‑Signalübertragung blockieren — einem wichtigen Weg downstream von Interferon — war ein Medikament, Pacritinib, besonders wirksam darin, das Wachstum resistenter Zellen und patientenabgeleiteter Tumor‑Organoide zu verlangsamen. Das legt nahe, dass die Kombination von CDK4/6‑Inhibitoren mit bestimmten JAK‑zielgerichteten Arzneien eine vielversprechende Strategie für Patientinnen sein könnte, deren Tumoren die derzeitigen Kombinationen überwunden haben.
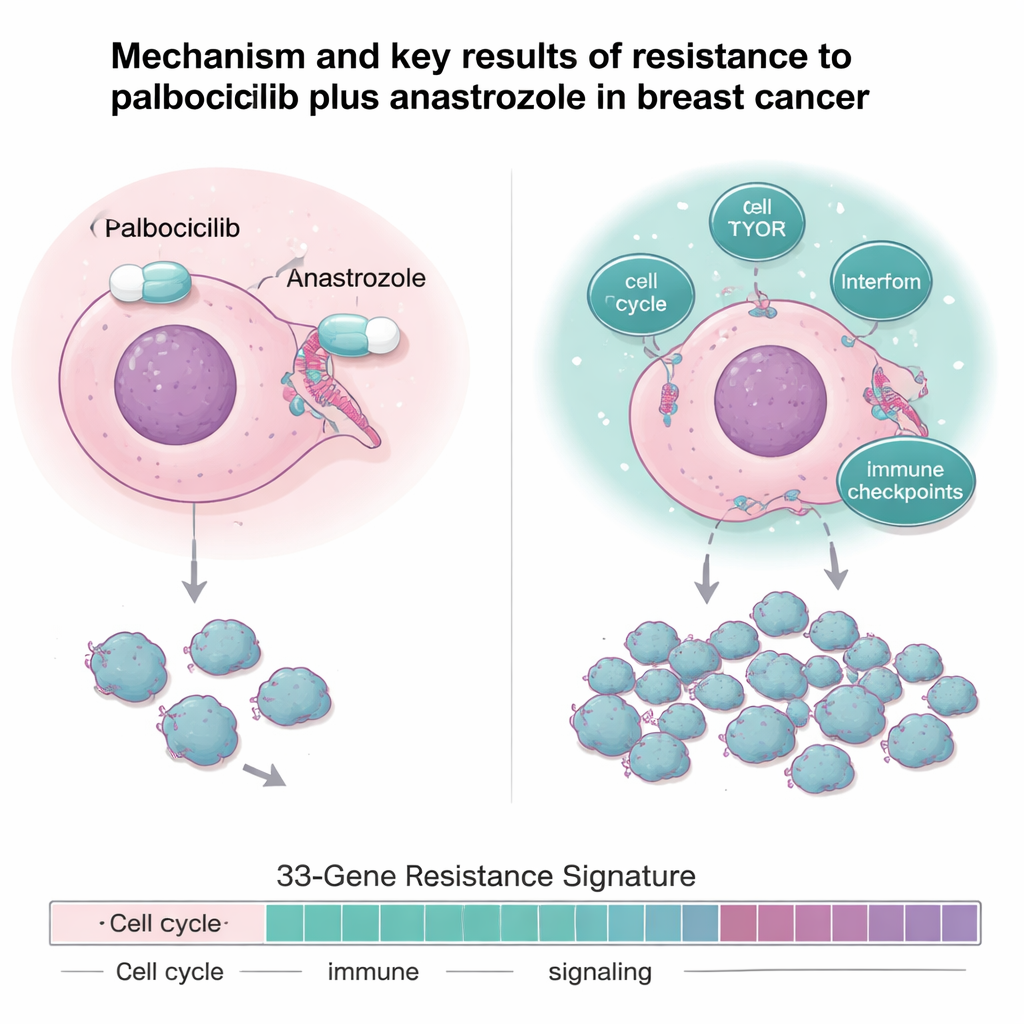
Ein Gen‑Fingerabdruck, der das Ergebnis vorhersagt
Durch den Vergleich sensibler und resistenter Tumoren aus zwei verwandten Studien erstellten die Forschenden eine 33‑Gene umfassende „Resistenzsignatur“, die Gene abbildet, die an Zellteilung, DNA‑Reparatur, Wachstums‑Signalgebung, Stoffwechsel sowie Immun‑/Entzündungsreaktionen beteiligt sind. Dieser Gen‑Fingerabdruck war sehr präzise darin, sensitive von resistenten Tumoren in der Studie zu unterscheiden. Wichtig ist, dass dieselbe 33‑Gen‑Signatur in einer unabhängigen Gruppe von 151 Patientinnen mit metastasiertem Brustkrebs, die außerhalb der Studie routinemäßig mit CDK4/6‑Inhibitoren plus Hormontherapie behandelt wurden, angewendet wurde: Bei denen, deren Tumoren hohe Werte für die Resistenzsignatur aufwiesen, waren das progressionsfreie Intervall und das Gesamtüberleben kürzer. Mit anderen Worten: Dieses vor der Behandlung gemessene Genmuster konnte Patientinnen kennzeichnen, die wahrscheinlich weniger lange von Standardregimen auf CDK4/6‑Basis profitieren würden.
Was das für die künftige Versorgung bedeutet
Für Menschen mit endokrin‑resistentem, östrogenrezeptorpositivem Brustkrebs liefert diese Studie sowohl Zuversicht als auch einen Fahrplan. Sie zeigt, dass das Hinzufügen von Palbociclib zu Anastrozol in mehr als der Hälfte der resistenten Fälle das Tumorwachstum noch zum Erliegen bringen kann. Gleichzeitig offenbart sie, dass einige Tumoren auf alternative Wachstums‑ und immunbezogene Pfade angewiesen sind, was sie schwerer kontrollierbar macht. Die neu definierte 33‑Gen‑Signatur und die Entdeckung, dass JAK‑zielgerichtete Wirkstoffe wie Pacritinib resistente Zellen bremsen können, deuten auf eine stärker personalisierte Behandlung hin: Patientinnen zu identifizieren, die wahrscheinlich nicht auf Standardkombinationen ansprechen, und sie früher in Studien mit neuen Wirkstoffkombinationen zu lenken, die direkt die Backup‑Überlebenswege des Tumors angreifen.
Zitation: Kong, T., Mabry, A., Highkin, M. et al. Biomarkers of response to neoadjuvant palbociclib plus anastrozole in endocrine-resistant estrogen receptor-positive/HER2-negative breast cancer: a phase 2 trial. Nat Commun 17, 949 (2026). https://doi.org/10.1038/s41467-026-68570-6
Schlüsselwörter: ER‑positiver Brustkrebs, CDK4/6‑Inhibitoren, endokrine Resistenz, Tumorbiomarker, Palbociclib Anastrozol