Clear Sky Science · de
Multimodale Analyse entwirrt die genetischen und mikrobiellen Zusammenhänge zwischen entzündlichen Darmerkrankungen und anderen immunvermittelten Erkrankungen in einem harmonisierten Bevölkerungsrahmen
Warum manche Immunerkrankungen gemeinsam auftreten
Viele Menschen mit entzündlicher Darmerkrankung (IBD) – langanhaltende Entzündung des Darms – entwickeln auch andere immunvermittelte Erkrankungen wie Arthritis, Psoriasis oder multiple Sklerose. Ärztinnen und Ärzte beobachten diese Überlappungen regelmäßig, doch bisher war unklar, wie sehr sie durch gemeinsame Gene, durch unsere alltägliche Umwelt oder durch die Mikroben im Darm verursacht werden. Diese Studie verwendet landesweite Daten aus Dänemark, umfangreiche genetische Datensätze und Darmmikrobiomprofile, um zu klären, warum bestimmte Immunerkrankungen dazu neigen, zusammen aufzutreten, und warum Crohn-Krankheit und Colitis ulcerosa, die beiden Hauptformen der IBD, sich nicht immer gleich verhalten.
Krankheitsmuster in Familien verfolgen
Die Forschenden begannen damit, einen riesigen Stammbaum der modernen dänischen Bevölkerung anhand von Meldedaten zu erstellen, die Eltern, Kinder und Geschwister verknüpfen. Im Fokus standen mehr als zweieinhalb Millionen Vollgeschwister, die zwischen 1910 und 2010 geboren wurden; sie untersuchten, wie häufig Crohn-Krankheit oder Colitis ulcerosa zusammen mit 23 anderen immunvermittelten entzündlichen Erkrankungen auftraten, darunter rheumatoide Arthritis, Psoriasis, Typ‑1‑Diabetes, multiple Sklerose und Lupus. Sie stellten fest, dass sich sowohl Crohn-Krankheit als auch Colitis ulcerosa stark familiär häufen, dabei aber unterschiedliche „Begleiter“ haben. So waren beide Darmerkrankungen innerhalb von Familien deutlich mit Psoriasis, psoriatischer Arthritis, rheumatoider Arthritis und ankylosierender Spondylitis verknüpft, während Colitis ulcerosa – nicht aber Crohn-Krankheit – auffällige familiäre Verbindungen zu Erkrankungen wie Sarkoidose und Lupus zeigte.
Einblick in gemeinsame Gene
Familienmuster können gemeinsame Gene, gemeinsame Umwelt oder beides widerspiegeln. Um diese Einflüsse zu trennen, griff das Team auf Genom-weite Assoziationsstudien zurück, die Hunderttausende genetische Marker im Genom großer Patientengruppen untersuchen. Sie quantifizierten, wie viel des genetischen Risikos für Crohn-Krankheit und Colitis ulcerosa mit anderen Immunerkrankungen geteilt wird. Wie erwartet teilen die beiden Darmerkrankungen ein starkes genetisches Fundament. Darüber hinaus jedoch divergierten ihre genetischen Verbindungen. Crohn-Krankheit zeigte eine positive genetische Überlappung mit Asthma, Psoriasis, psoriatischer Arthritis und rheumatoider Arthritis, während Colitis ulcerosa mehr genetisches Risiko mit Typ‑1‑Diabetes und primärer biliärer Cholangitis, einer Lebererkrankung, gemeinsam hatte. Auffällig war, dass beide IBD-Typen negative genetische Korrelationen mit multipler Sklerose zeigten, und Colitis ulcerosa zusätzlich mit Lupus, was darauf hindeutet, dass einige genetische Varianten, die das Risiko für Darmentzündungen erhöhen, gegen bestimmte Gehirn- oder systemische Immunerkrankungen schützen könnten.
Dem mikrobiellen „Akzent“ des Darms zuhören
Gene sind nur ein Teil der Geschichte. Die Autorinnen und Autoren sammelten zudem Stuhl-Mikrobiomdaten von Tausenden Menschen weltweit und verarbeiteten alle 16S‑rRNA-Sequenzdaten in harmonisierter Weise neu, damit Bakterienstämme zwischen Studien vergleichbar sind. Für sieben Immunerkrankungen erstellten sie „Mikrobiota‑Krankheitsprofile“ – statistische Zusammenfassungen, wie Hunderte bakterieller Varianten bei Patienten im Vergleich zu gesunden Kontrollen differieren. Der Vergleich dieser Profile zeigte, dass Crohn-Krankheit und Colitis ulcerosa im Großen und Ganzen ähnliche mikrobielle Störungen teilen und beide stark mit rheumatoider Arthritis und Zöliakie überlappen. Dennoch wies Colitis ulcerosa auch Mikrobiomähnlichkeiten mit multipler Sklerose und Morbus Basedow auf, selbst wenn die genetische Überlappung mit diesen Erkrankungen schwach oder negativ war. Diese Diskrepanz zwischen Genen und Mikroben deutet auf eine starke Rolle von Umwelt und Lebensstil hin – einschließlich Medikamenten, Ernährung und Antibiotikabelastung – bei der Herausbildung gemeinsamer mikrobieller Signaturen über scheinbar weit entfernte Immunerkrankungen hinweg.
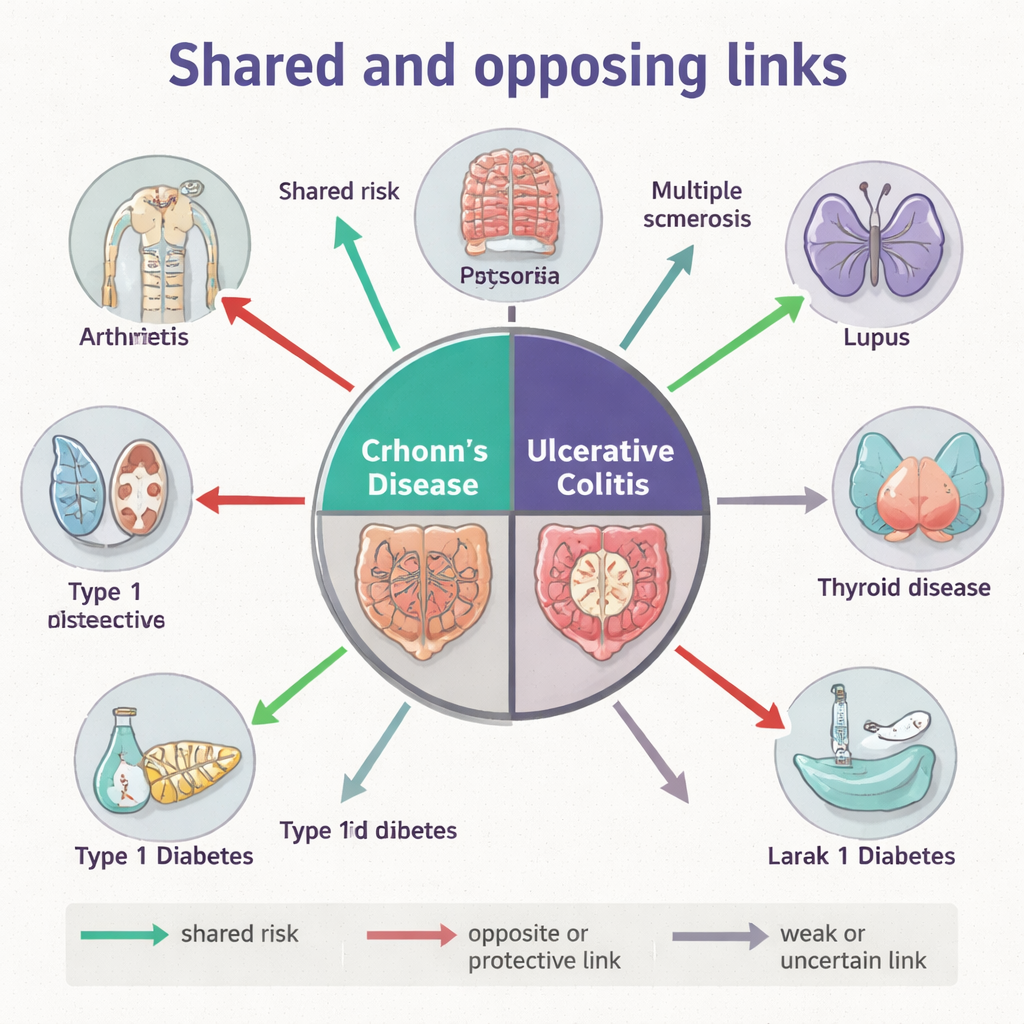
Was das für Patienten und Ärztinnen bedeutet
Zusammengefasst zeigen die familiären, genetischen und mikrobiellen Ebenen, dass Crohn-Krankheit und Colitis ulcerosa keine austauschbaren Bezeichnungen sind, sondern unterschiedliche Mitglieder der Immunerkrankungsfamilie. Einige Erkrankungen, wie Psoriasis und bestimmte Formen von Arthritis, zeigen konsistente Verbindungen über alle drei Ebenen und deuten auf tief geteilte biologische Mechanismen hin. Andere, wie multiple Sklerose und Lupus, zeigen nahezu ein „Zug‑und‑Schieb“-Verhältnis, bei dem genetische Effekte und mikrobielle Muster in entgegengesetzte Richtungen weisen. Diese Nuancen helfen zu erklären, warum Menschen mit IBD sehr unterschiedliche Kombinationen anderer Immunprobleme erleben können und warum dasselbe Medikament in einer Erkrankung hilfreich, in einer anderen jedoch nachteilig sein kann.
Blick nach vorn: in Richtung individualisierter Versorgung
Für Laien lautet die zentrale Botschaft, dass Immunerkrankungen nicht isoliert entstehen. Die Studie zeigt, dass die Kombination von Erkrankungen, die eine Person entwickelt, von einem wechselnden Mix aus vererbten Genen, familiärem Hintergrund und dem mikroskopischen Leben im Darm abhängt. Sie plädiert dafür, Crohn-Krankheit und Colitis ulcerosa als verwandte, aber unterschiedliche Entitäten zu erforschen und zu behandeln, mit besonderem Augenmerk auf das breitere Immunprofil und die Familiengeschichte jeder Patientin bzw. jedes Patienten. Künftig könnten die Kombination aus genetischen Risikoscores und Mikrobiom-Signaturen Ärztinnen und Ärzten helfen, besser vorherzusagen, welche zusätzlichen Immunerkrankungen bei einer Person mit IBD auftreten könnten, und Präventions‑ und Behandlungsstrategien zu entwickeln, die wirklich personalisiert statt Einheitsgröße sind.
Zitation: Vestergaard, M.V., Alfaro-Núñez, A., Sazonovs, A. et al. Multimodal analysis disentangles the genetic and microbial associations between inflammatory bowel disease and other immune-mediated diseases across a harmonized population framework. Nat Commun 17, 1849 (2026). https://doi.org/10.1038/s41467-026-68564-4
Schlüsselwörter: entzündliche Darmerkrankung, autoimmunes Komorbidität, Darmmikrobiom, genetische Korrelation, Crohn-Krankheit und Colitis ulcerosa