Clear Sky Science · de
Die Zellwand aufbrechen für eine effiziente DNA‑Einführung in Kieselalgen
Algen als winzige grüne Fabriken
Kieselalgen — mikroskopisch kleine Algen, die in den Ozeanen treiben — produzieren still und leise etwa ein Fünftel des organischen Kohlenstoffs der Erde, nähren marine Nahrungsnetze und binden Kohlendioxid. Wissenschaftler möchten diese robusten, schnell wachsenden Organismen in winzige grüne Fabriken verwandeln, die Treibstoffe, Nahrungsmittel und Spezialchemikalien herstellen. Ein großes Hindernis stand dem jedoch im Weg: Es ist überraschend schwierig, zuverlässig neue DNA in Kieselalgenzellen einzubringen. Diese Studie geht dieses praktische Problem direkt an und beschreibt neue Wege, genetische Anweisungen und Genom‑Editierwerkzeuge an der robusten Außenwand der Kieselalge vorbei zu schleusen.
Die Schale von Meeresmikroben aufweichen
Die Arbeit konzentriert sich auf das Modellorganismus Phaeodactylum tricornutum, ein Laborliebling, dessen Genom gut kartiert ist und für das bereits Grundwerkzeuge existieren. Die Autoren vermuteten, dass die Zellwand, die erste physische Barriere, die jede DNA überwinden muss, ein wichtiger Engpass ist. Durch Behandlung der Zellen mit dem Enzym Alcalase entfernten sie diese Wand teilweise oder vollständig und erzeugten fragile „Spheroplasten“ und „Protoplasten“, die sich deutlich leichter durchdringen lassen. Anschließend angewandte Elektroporation — kurze elektrische Pulse, die vorübergehende Poren öffnen — erhöhte die Zahl erfolgreicher Transformanten dramatisch, etwa um zwei Größenordnungen im Vergleich zu früheren Methoden. Sogar winzige DNA‑Mengen, bereits ab einem Nanogramm, reichten aus, um gentechnisch veränderte Zellen zu gewinnen. 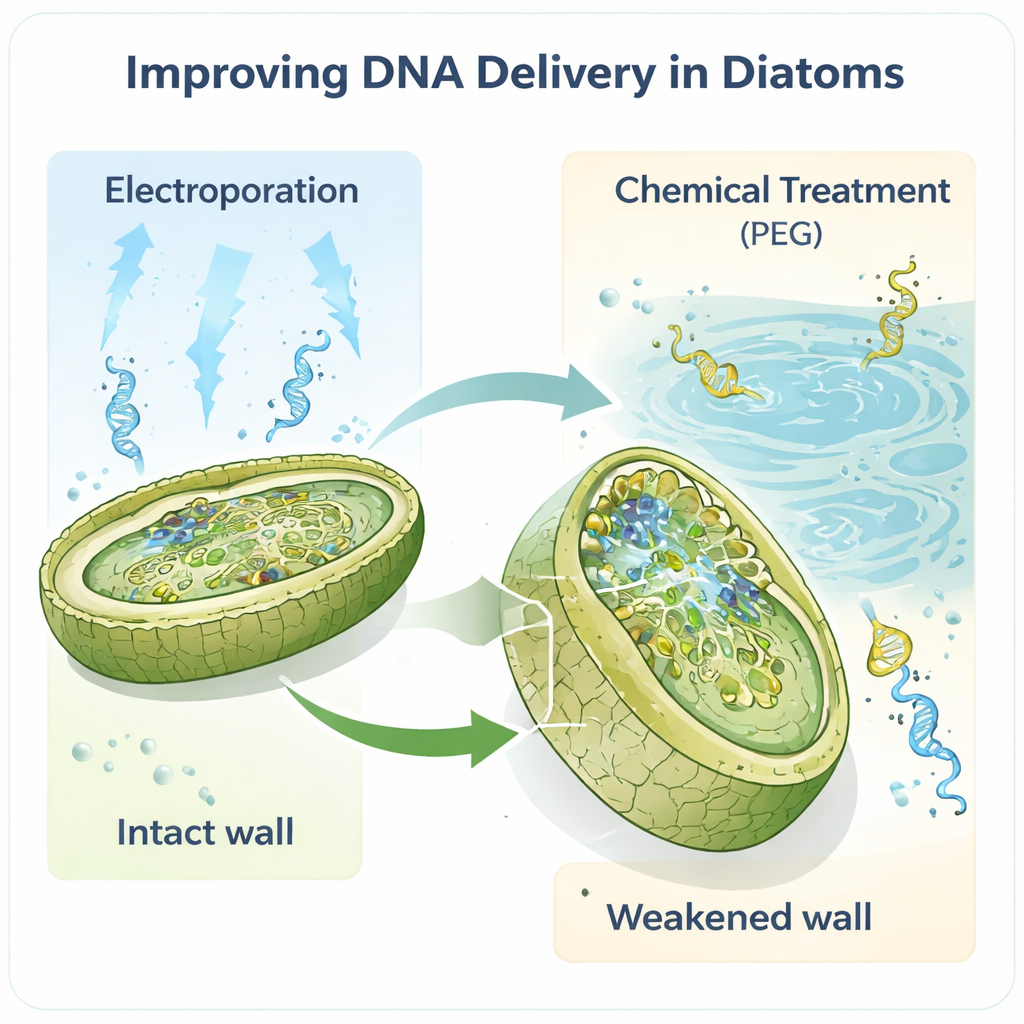
Schnelle DNA‑Einführung ohne Umweg über Bakterien
Traditionelle Methoden zur Modifikation von Kieselalgen verlassen sich oft auf bakterielle „Kuriere“, die große, ringförmige DNA‑Moleküle, sogenannte Episome, in die Algen schleusen. Zwar wirksam, ist dieser Ansatz langsam, technisch anspruchsvoll und kann empfindliche DNA‑Konstrukte destabilisieren. Die neuen Protokolle zeigen, dass sowohl Elektroporation als auch eine verfeinerte chemische Methode mit Polyethylenglykol (PEG) Episome direkt in Kieselalgen bringen können, ohne den bakteriellen Schritt. Bemerkenswert ist, dass Episome mit einer Länge von bis zu 55,6 Tausend Basenpaaren geliefert und intakt wiedergewonnen wurden. Dieselben Strategien funktionierten auch in einer zweiten Art, Thalassiosira pseudonana, die eine stärker mineralisierte Wand besitzt, was darauf hindeutet, dass dieses Toolkit allgemein nützlich ist und kein arteigener Trick.
Die Zelle baut ihre eigenen genetischen Kreise
Bei der Untersuchung, wie sich durch Elektroporation eingebrachte DNA in den Zellen verhält, stießen die Forscher auf ein überraschendes Talent: Kieselalgen können DNA‑Fragmente eigenständig zusammennähen. Lineare Stücke von Episomen traten in die Zelle ein und wurden entweder durch ungenaue „nicht‑homologe“ Verknüpfung oder durch präzisere, überlappungsgeführte „homologie‑gerichtete“ Reparatur zu Kreisen vervollständigt. Die Autoren bezeichneten diesen Vorgang als „diatom in vivo assembly“ bzw. DIVA. Durch das Design überlappender Fragmente brachten sie die Zellen dazu, zwei, drei oder vier Teile mit hohen Erfolgsraten zu vollständigen Episomen zusammenzusetzen, wobei gelegentlich kleine synthetische Kassetten eingebaut wurden, die Fluoreszenzmarker oder neue Funktionen hinzufügen. Diese Fähigkeit verwandelt den Diatomenkern in eine winzige DNA‑Werkstatt und könnte arbeitsintensive Assemblierungsschritte ersetzen, die sonst in Hefen oder E. coli durchgeführt werden.
Genome nur mit Protein‑Komplexen editieren
Neben dem Einbringen von Episomen zeigten die Forscher, dass sie fertige CRISPR–Cas9 Protein‑RNA‑Komplexe direkt mit ihrer optimierten Elektroporationsmethode in Kieselalgenzellen liefern können. Durch Zielsetzung des Gens PtAPT, das die Empfindlichkeit gegenüber einem toxischen Adenin‑Analoga steuert, erzeugten sie Tausende resistenter Mutanten, ohne zusätzliche DNA in das Genom einzuführen. Viele dieser Mutanten trugen kleine Einfügungen oder Deletionen an der Zielstelle; einige fingen sogar Fragmente von „Träger‑DNA“ ein, die zur Pufferung des elektrischen Schocks beigegeben worden war. Das Team lieferte dann CRISPR‑Komplexe und Episome in einem einzigen Schritt gemeinsam und stellte fest, dass etwa eine von zehn Kolonien sowohl eine genomische Editierung als auch ein selektierbares Episom trug — ein effizienter Weg, ansonsten unsichtbare Genveränderungen zu verfolgen. 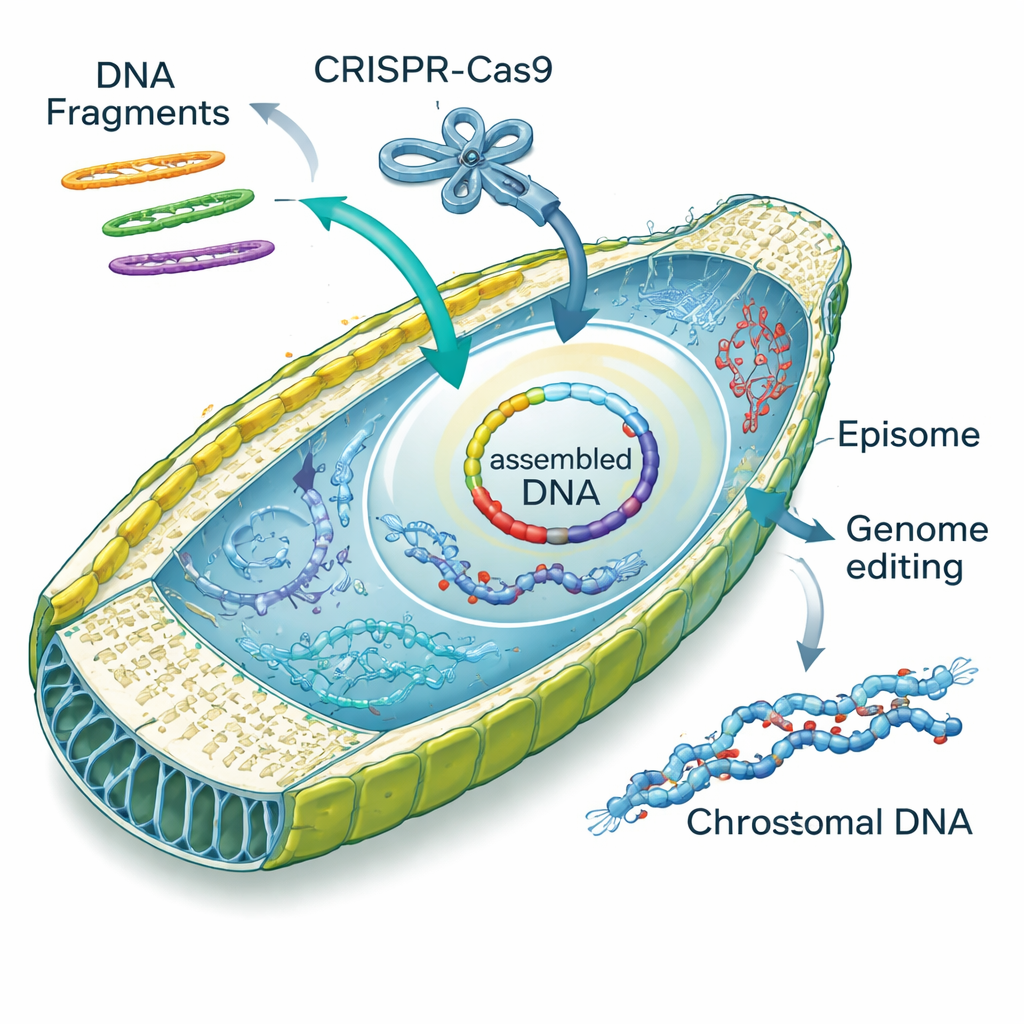
Auf dem Weg zu Designer‑Kieselalgen für eine nachhaltige Zukunft
Für Nicht‑Spezialisten ist die Kernbotschaft, dass Kieselalgen deutlich näher daran rücken, praktikable, programmierbare Organismen zu werden. Durch das behutsame Aufbrechen oder Aufweichen der Zellwand verwandelten die Autoren einen wählerischen, ertragsarmen Prozess in eine robuste Pipeline, die kleine DNA‑Mengen verwendet, mit großen genetischen Konstrukten arbeitet und der Zelle sogar erlaubt, ihre eigene DNA zu montieren und zu editieren. Diese Fortschritte verkürzen den Weg von einer am Computer entworfenen Sequenz zu einem lebenden, getesteten Stamm. Langfristig könnten solche Werkzeuge die Entwicklung von Kieselalgen mit vollständig synthetischen Chromosomen beschleunigen und diese Meeresmikroben für sauberere Treibstoffe, klimafreundliche Chemie und neue biologische Entdeckungen nutzbar machen.
Zitation: Walker, E.J.L., Pampuch, M., Deng, L. et al. Breaking the cell wall for efficient DNA delivery to diatoms. Nat Commun 17, 1848 (2026). https://doi.org/10.1038/s41467-026-68562-6
Schlüsselwörter: Kieselalgen‑Biotechnologie, genetische Transformation, CRISPR‑Genomeditierung, synthesische Biologie, Mikroalgen‑Engineering