Clear Sky Science · de
Strukturen der nukleotidgebundenen menschlichen Telomerase in mehreren Schritten ihres Zyklus zur Addition telomerischer DNA‑Wiederholungen
Warum die Enden unserer Chromosomen wichtig sind
Jedes Mal, wenn sich eine Zelle teilt, werden die schützenden Kappen an den Enden unserer Chromosomen — die Telomere — etwas kürzer. Werden sie zu kurz, hören Zellen auf sich zu teilen oder funktionieren nicht mehr richtig, was zu Alterung und Krankheiten beiträgt. Eine molekulare Maschine namens Telomerase kann diese Kappen wieder aufbauen und ist in den meisten Krebsarten ungewöhnlich aktiv. Diese Studie zeigt in beispielloser Detailgenauigkeit, wie die menschliche Telomerase Telomere Schritt für Schritt greift und verlängert, und liefert Hinweise darauf, wie man dieses Enzym eines Tages bei altersbedingten Störungen und Krebs feinjustieren könnte.
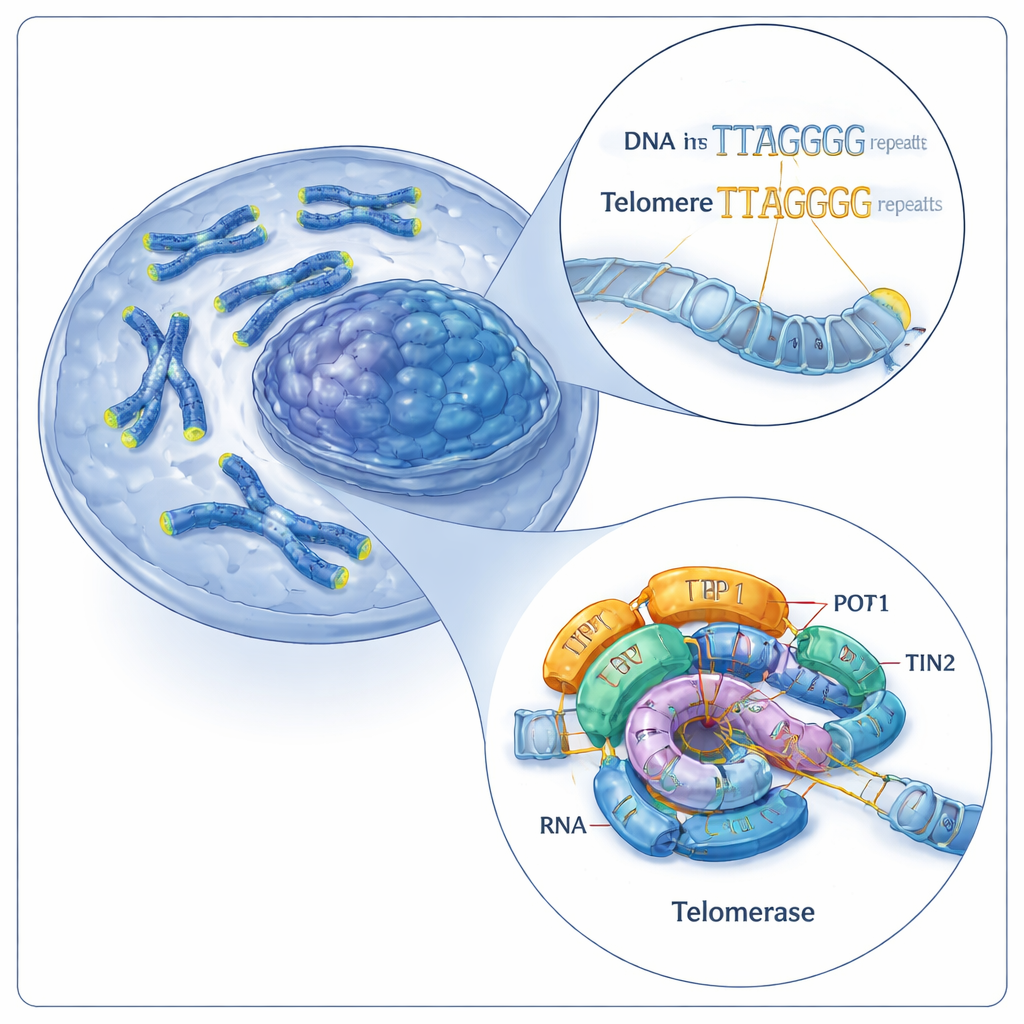
Die Reparaturmannschaft für die Chromosomenkappen der Zelle
Telomere bestehen aus kurzen, sich wiederholenden DNA‑Sequenzen (beim Menschen ein sechsstelliger Muster: TTAGGG). Telomerase verlängert Telomere, indem sie am Chromosomenende weitere dieser Wiederholungen anfügt. Dabei arbeitet sie mit zwei Hauptkomponenten: einem Protein, der Telomerase‑Reversen‑Transkriptase (TERT), und einem eingebetteten RNA‑Molekül (hTR), das als Vorlage dient. Zusammen bilden diese Komponenten einen katalytischen Kern, der zusätzlich von Begleitproteinen unterstützt wird, die als Shelterin bekannt sind, darunter ein Trio namens TPP1–POT1–TIN2. Frühere Arbeiten hatten die menschliche Telomerase nur in einem Arbeitszustand sichtbar gemacht, sodass eine zentrale Frage offenblieb: Wie fügt diese Maschine wiederholt neue Wiederholungen hinzu, ohne von der DNA abzufallen?
Telomerase im Moment des Handelns einfrieren
Die Forschenden rekonstruierten die menschliche Telomerase in menschlichen Zellen und setzten sie anschließend mit sorgfältig gestalteten Stücken telomerischer DNA und nicht‑reaktiven Nukleotid‑Analoga zusammen — Molekülen, die wie DNA‑Bausteine aussehen, aber nicht vollständig eingebaut werden können. Mithilfe hochauflösender Kryo‑Elektronenmikroskopie hielten sie Schnappschüsse der Telomerase in drei Schlüsselphasen ihres Zyklus zur Wiederholungsaddition fest: am Anfang (Initiation), in der Mitte der Kopie (Elongation) und kurz vor dem Abschluss einer Wiederholung (Prä‑Termination). Jeder Schnappschuss zeigte den katalytischen Kern der Telomerase, der ein kurzes DNA–RNA‑Hybrid umschließt, wobei ein ankommendes Nukleotid in der aktiven Stelle bereitliegt, um an den wachsenden DNA‑Strang angefügt zu werden.
Ein winziger Reißverschluss, der einen großen Prozess steuert
In allen drei Stadien zeigte sich ein überraschendes Muster: Das DNA–RNA‑Hybrid innerhalb der Telomerase bleibt im Wesentlichen gleich lang — nur vier Basenpaare — und dehnt sich nur vorübergehend auf fünf aus, wenn ein neues Nukleotid eintritt. Eine spezifische Aminosäure in TERT, die man als „Reißverschluss‑Kopf“ bezeichnet, markiert konstant das Ende dieses kurzen Hybrids und verhindert, dass es länger wird. Wenn neue DNA‑Bausteine hinzugefügt werden, löst sich ein Basenpaar am äußersten Ende, sodass das Hybrid nie über dieses enge Fenster von vier bis fünf Paaren hinauswächst. Dieses kompakte Design erleichtert vermutlich das Auftrennen und Verschieben der Stränge, sodass das Enzym weiterwandern und die nächste Wiederholung beginnen kann, ohne die DNA vollständig loszulassen. Feine Unterschiede darin, welche DNA‑ und RNA‑Basen dieses kurze Hybrid besetzen, erklären, warum manche telomerischen Endsequenzen stärker an die Telomerase binden als andere.
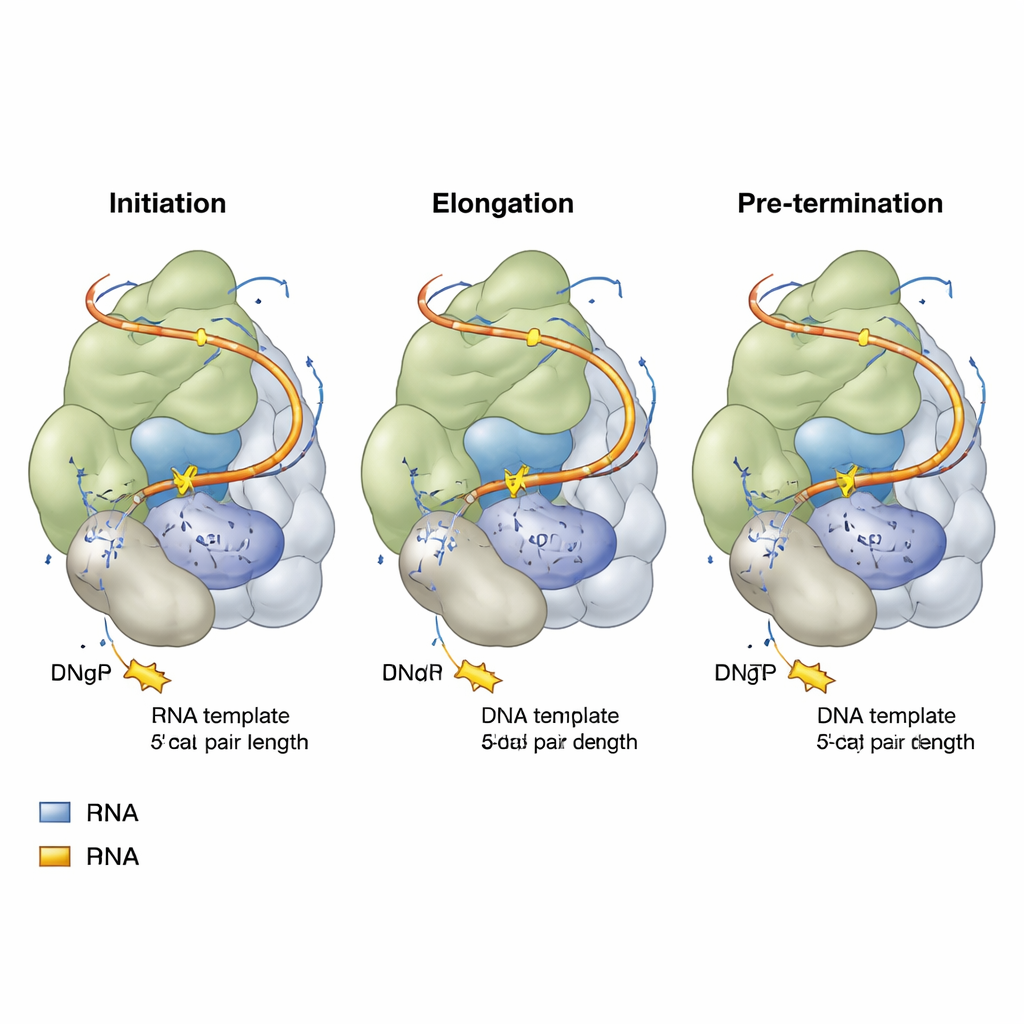
Flexible RNA‑Verbindungen und bewegliche Teile
Die RNA‑Vorlage innerhalb der Telomerase schwimmt nicht frei; sie ist beidseitig durch flexible Abschnitte befestigt, sogenannte 5′‑ und 3′‑Template‑Linker. Wenn die Telomerase von der Initiation zur Prä‑Termination fortschreitet, wird der vorgelagerte (5′) Linker wie ein Gummiseil gespannt und erreicht schließlich einen voll ausgestreckten Zustand, der hilft, das Ende einer Wiederholung anzuzeigen. Gleichzeitig wölbt sich der nachgelagerte (3′) Linker nach außen und nähert sich einer anderen RNA‑Struktur (der P6.1‑Haarschleife) und angrenzenden Proteinbereichen. Werden diese Linker zu kurz oder zu lang, oder wird P6.1 verändert, sinkt die Fähigkeit der Telomerase, Wiederholung an Wiederholung anzufügen, stark ab. Wichtig sind zudem bestimmte Proteinregionen — die TEN‑Domäne und eine telomerase‑spezifische Einfügung, die als TRAP‑Keil bezeichnet wird — die als verstellbare Führungen fungieren und sowohl mit der DNA als auch mit diesen RNA‑Linkern in Kontakt stehen. Mutationen, die das Volumen des TRAP‑Keils verringern, können das Enzym tatsächlich prozessiver machen, was darauf hindeutet, dass dieser Keil normalerweise als kontrollierte Barriere wirkt, die die Bewegung der Vorlage zeitlich steuert.
Neue Einblicke in ein therapeutisches Ziel
Durch die Kombination struktureller Schnappschüsse mit funktionellen Tests gezielter Mutationen schlägt die Studie ein detailliertes mechanisches Modell dafür vor, wie die menschliche Telomerase wiederholt Telomere verlängert. Das Enzym hält ein sehr kurzes DNA–RNA‑Hybrid, verwendet eine reißverschlussähnliche Aminosäure, um diese Länge durchzusetzen, und stützt sich auf flexible RNA‑Linker und bewegliche Protein‑Elemente, um die Vorlage voranzuschieben und die DNA während mehrerer Kopierrunden verankert zu halten. Für Nicht‑Fachleute lautet die Kernbotschaft: Telomerase arbeitet nicht als starre Kopiermaschine, sondern als fein abgestimmtes, federbelastetes Gerät, dessen Geometrie und bewegliche Teile bestimmen, wie lange und wie effizient sie Telomere erhalten kann. Das Verständnis dieses Zusammenspiels öffnet Wege zu Wirkstoffen, die die Telomerase in Tumoren dämpfen oder ihre Funktion bei vorzeitiger Alterung stabilisieren könnten.
Zitation: Balch, S., Franco-Echevarría, E., Ghanim, G.E. et al. Structures of nucleotide-bound human telomerase at several steps of its telomeric DNA repeat addition cycle. Nat Commun 17, 1847 (2026). https://doi.org/10.1038/s41467-026-68560-8
Schlüsselwörter: Telomerase, Telomere, cryo‑EM, Genomstabilität, Krebsbiologie