Clear Sky Science · de
DNA-Methylierung und lncRNA steuern asynchrone DNA-Replikation in bestimmten imprintierten Gendomänen
Warum der Zeitplan, in dem die Zelle ihre DNA kopiert, wichtig ist
Jedes Mal, wenn sich eine Zelle teilt, muss sie ihre gesamte DNA kopieren, doch nicht alle Regionen werden zum gleichen Zeitpunkt dupliziert. Manche Abschnitte werden früh, andere spät kopiert und folgen einem präzisen „Stundenplan“ des Genoms. In dieser Arbeit untersuchen die Autoren, warum in einigen wenigen speziellen Genclustern, die sich daran erinnern, von welchem Elternteil sie stammen, die mütterlichen und väterlichen Kopien zu unterschiedlichen Zeiten repliziert werden. Das Verständnis dieses ungewöhnlichen Zeitpunkts gibt Aufschluss darüber, wie chemische Markierungen auf der DNA und lange nicht-kodierende RNAs (lncRNAs) das Genom organisieren und Entwicklung sowie Krankheit beeinflussen können.
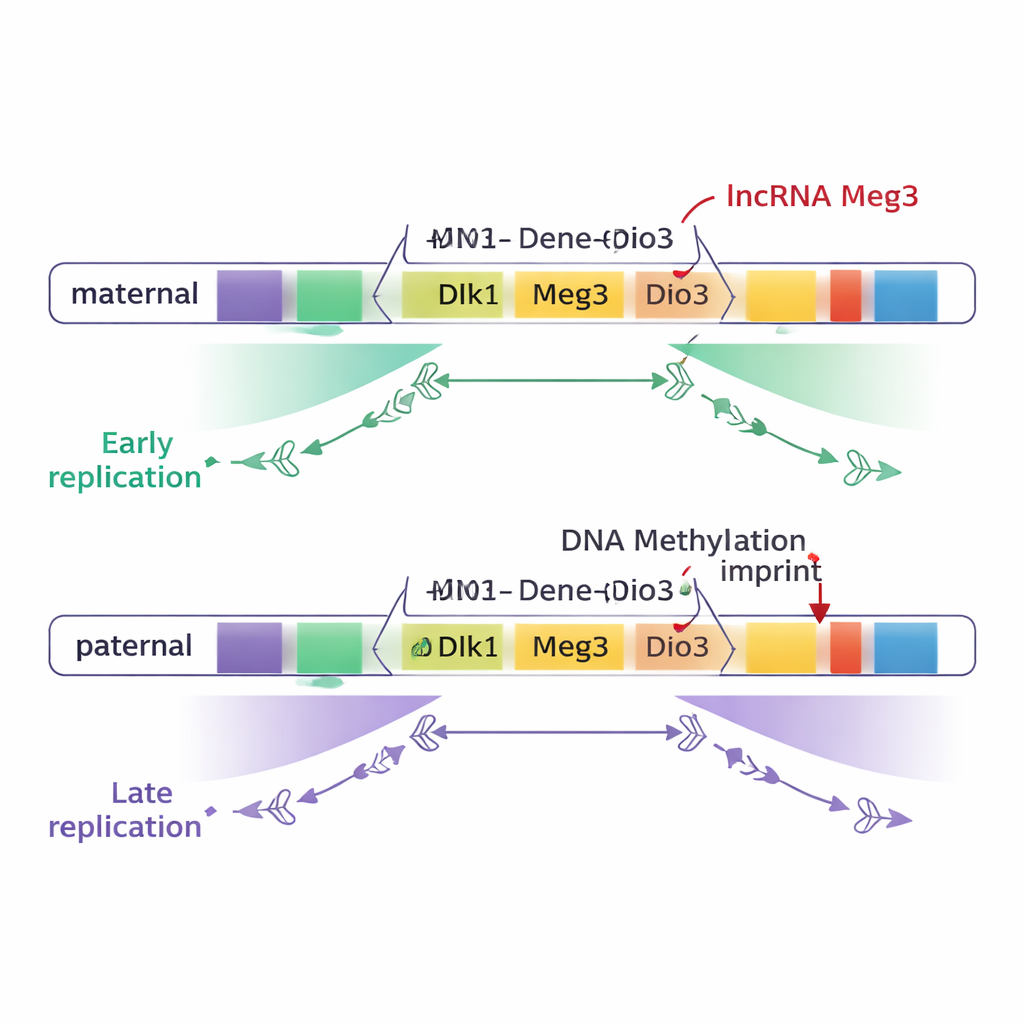
Elterliche Erinnerungen, in die DNA geschrieben
Bei Säugetieren verhalten sich einige wenige „imprintete“ Gendomänen unterschiedlich, je nachdem, ob sie von der Mutter oder vom Vater vererbt wurden. Dieser Elternherkunftseffekt wird durch DNA-Methylierung—kleine chemische Markierungen, die an spezifische Regionen, so genannte differentielle methylierte Regionen (DMRs), angeheftet werden—und durch Änderungen in der Chromosomenfaltung gesteuert. Die Autoren untersuchten Maus-embryonale Stammzellen, die frühen Embryonalzellen ähneln. Sie verglichen Zellen mit ausschließlich maternalen Genomen, ausschließlich paternalem Genom und normalen Hybriden, die je eines von beiden tragen. Indem sie verfolgten, zu welchem Zeitpunkt DNA-Abschnitte im Zellzyklus kopiert wurden, kartierten sie die Replikationszeitpunkte im gesamten Genom und fokussierten sich auf bekannte imprintete Regionen.
Zwei imprintete Regionen brechen die Regeln
Der größte Teil des Genoms, einschließlich der meisten imprinteten Domänen, wurde auf mütterlichen und väterlichen Chromosomen zur gleichen Zeit repliziert. Auffällig waren jedoch zwei große imprintete Regionen: die Dlk1–Dio3-Domäne auf Chromosom 12 und die Snrpn-Region auf Chromosom 7. In diesen Bereichen wurde ein breiter DNA-Abschnitt—am Dlk1–Dio3 etwa drei Viertel einer Million Basenpaare—auf dem einen elterlichen Chromosom früh und auf dem anderen spät repliziert. Entscheidend war, dass dieser Unterschied der Elternherkunft folgte, nicht dem Stammhintergrund: die mütterliche Kopie wichtiger Gene wie Dlk1 und des lncRNA-Gens Meg3 replizierte konsequent früh, während die väterlichen Kopien spät replizierten.
DNA-Methylierung stellt den Schaltmechanismus
Um zu testen, was diesen Zeitunterschied verursacht, erzeugten die Forscher Stammzellen, in denen das normale Methylierungsmuster an DMRs entweder entfernt oder auf beide elterlichen Chromosomen übertragen wurde. Wenn beide elterlichen Kopien der Dlk1–Dio3-DMRs methyliert waren, replizierte die gesamte Region spät auf beiden Chromosomen. Wenn die Methylierung weitgehend von beiden Kopien entfernt wurde, replizierte dieselbe Region früh auf beiden. Ähnliche Experimente an Snrpn führten ebenfalls zum Verlust der zeitlichen Unterschiede. Diese Ergebnisse zeigen, dass elternspezifische DNA-Methylierung wesentlich ist, um den Früh-gegen-Spät-Replikationskontrast zwischen mütterlichen und väterlichen Chromosomen zu erzeugen, zumindest in diesen beiden Domänen.
Eine lange RNA feintunt frühe Replikation
Die DNA-Methylierung allein erklärte jedoch nicht das gesamte Bild. In der Dlk1–Dio3-Region wird außerdem eine lange nicht-kodierende RNA namens Meg3 als Teil eines großen RNA-„Polycistrons“ produziert. Auf dem mütterlichen Chromosom erlauben unmethylierte DMRs die Expression von Meg3; auf dem väterlichen Chromosom hält Methylierung sie stumm. Durch gezielte Deletionen, die Meg3 ausschalteten, während die DNA-Methylierung intakt blieb, zeigten die Autoren, dass der Verlust von Meg3-RNA bewirkte, dass bestimmte Teile der mütterlichen Domäne von früher zu später Replikation wechselten. Anders gesagt: Meg3-RNA fördert die frühe Kopie benachbarter Abschnitte auf dem mütterlichen Chromosom und fügt der DNA-Methylierung eine zweite Kontrollebene hinzu.
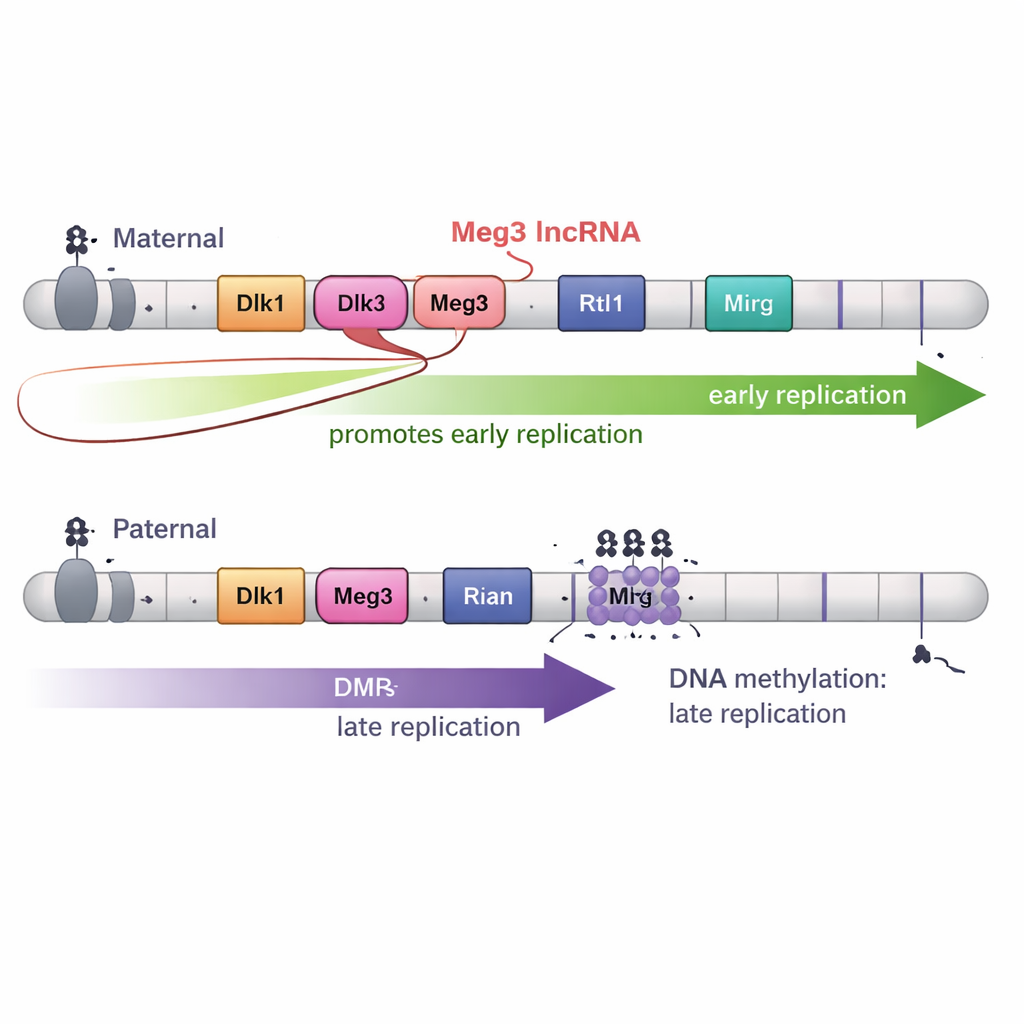
3D-Faltung und Entwicklung fügen weitere Wendungen hinzu
Da Genomfaltung oft mit Replikationszeitpunkten verknüpft ist, kartierte das Team auch die 3D-Chromosomenarchitektur in hoher Auflösung. Überraschenderweise stimmten in der Dlk1–Dio3-Region die Grenzen der 3D-Domänen nicht mit den Grenzen von Früh- und Spätreplikation überein. Selbst wenn Methylierungsmuster verändert wurden und sich die Replikationszeitpunkte änderten, verschoben sich die grundlegenden Faltungseinheiten—topologisch assoziierende Domänen—auf unterschiedliche Weise. Schließlich, als die Stammzellen zu neuronalen Vorläuferzellen differenziert wurden, verschwanden die markanten Zeitunterschiede zwischen mütterlichen und väterlichen Kopien größtenteils, obwohl Imprinting-Marken und viele Aspekte der 3D-Struktur erhalten blieben. Das deutet darauf hin, dass entwicklungsspezifische Signale das besondere Früh-gegen-Spät-Muster in Stammzellen außer Kraft setzen können.
Was das in einfachen Worten bedeutet
Die Studie zeigt, dass in einigen wenigen spezialisierten Genvierteln, die sich an ihre elterliche Herkunft erinnern, der Zeitplan der DNA-Kopie durch eine Kombination aus chemischen Markierungen auf der DNA und langen nicht-kodierenden RNAs gesteuert wird. DNA-Methylierung an imprintkontrollierenden Regionen legt eine grundsätzliche Früh‑oder‑Spät‑Zeit für jedes elterliche Chromosom fest, und die Meg3-lncRNA schiebt nahe liegende mütterliche DNA zusätzlich in Richtung früherer Replikation. Diese Effekte wirken überwiegend unabhängig von der 3D-Faltung des Chromosoms. Während der Entwicklung, wenn sich Zellen spezialisieren, verblasst dieses ungewöhnliche Timing und zeigt, dass es ein Merkmal des pluripotenten Stammzellzustands ist. Insgesamt erklärt die Arbeit, wie elterliche epigenetische „Erinnerungen“ und nicht-kodierende RNAs lokal den üblichen Replikationszeitplan des Genoms außer Kraft setzen können.
Zitation: Imaizumi, Y., Charon, F., Surcis, C. et al. DNA methylation and lncRNA control asynchronous DNA replication at specific imprinted gene domains. Nat Commun 17, 1844 (2026). https://doi.org/10.1038/s41467-026-68558-2
Schlüsselwörter: genomische Prägung, DNA-Methylierung, Replikationszeitpunkt, lange nicht-kodierende RNA, embryonale Stammzellen