Clear Sky Science · de
Mikrobielle Aktivierung des GLP-2R mildert Entzündungen im Gastrointestinaltrakt
Warum darmfreundliches Protein wichtig ist
Während die Welt nach nachhaltigen Wegen sucht, eine wachsende Bevölkerung zu ernähren, blicken Wissenschaftler über Felder und Farmen hinaus auf riesige Stahltanks, in denen Mikroben als Nahrungsquelle gezüchtet werden. Diese Studie untersucht, ob ein solches mikrobenbasiertes Protein mehr tun kann als nur zu nähren. Die Forscher fragten: Kann ein aus harmlosen Bakterien hergestelltes Protein sowohl den Nährstoffbedarf decken als auch den Darm aktiv vor Entzündungen schützen — ein Kernproblem bei Erkrankungen wie entzündlichen Darmerkrankungen und durch Chemotherapie ausgelösten Darmschäden?
Ein neuer Proteintyp aus Mikroben
Im Mittelpunkt dieser Arbeit steht ein Protein aus dem Bodenbakterium Methylococcus capsulatus Bath (McB). Anstatt als lebende Bakterien verzehrt zu werden, wird McB zu einem mikrobiellen Lysat verarbeitet — im Grunde ein pulverisiertes Gemisch aus aufgebrochenen Bakterienzellen — das kommerziell unter dem Namen FeedKind® hergestellt wird. Mäuse erhielten Diäten, bei denen dieses Lysat den größten Teil des Proteins lieferte, entweder in einer einfachen oder in einer eher menschenähnlichen „komplexen“ Ernährung. Das Team verfolgte dann, wie diese Nahrung die Zusammensetzung der Darmmikrobiota, die Immunzellen im Darm und die Widerstandsfähigkeit des Darms gegenüber verschiedenen Verletzungsarten veränderte.
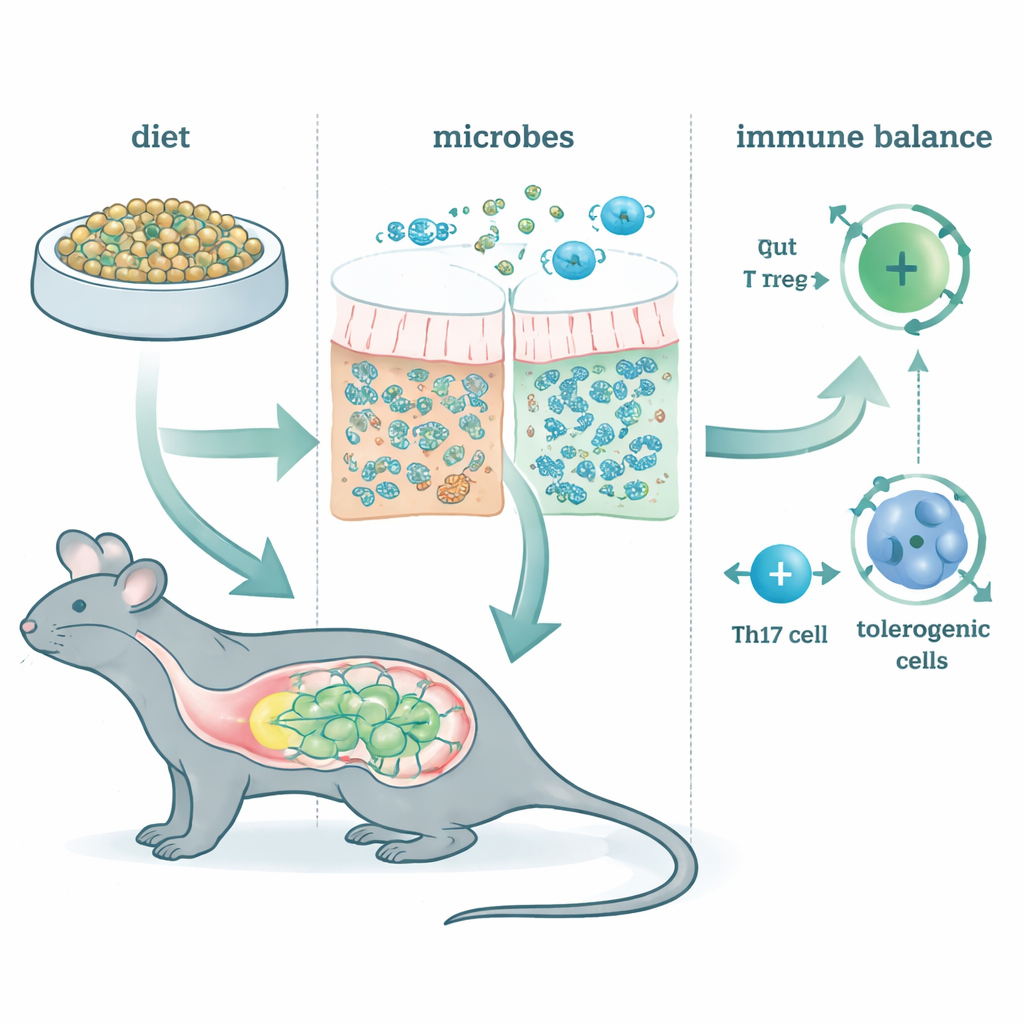
Umgestaltung der mikrobiellen Nachbarschaft
Die Gabe von McB veränderte die Darmmikrobiota schnell und nachhaltig, unabhängig von der zugrunde liegenden Diät. Nur ein winziger Bruchteil von McB selbst tauchte jemals im Kot auf, was bedeutet, dass das Material im Darm nahezu vollständig verwertet wurde. Stattdessen gediehen einige wenige Bakterienarten aus Familien wie Lachnospiraceae und Bacteroidaceae. Genetische Analysen zeigten, dass diese Gemeinschaften für Fermentationswege angereichert waren, die kurzkettige Fettsäuren produzieren — kleine Moleküle, die bereits dafür bekannt sind, Darmzellen zu nähren und das Immunsystem zu beeinflussen. Anders gesagt wirkte McB weniger wie ein konventionelles Protein und mehr wie ein gezielter Brennstoff, der das Tätigkeitsprofil der ansässigen Mikroben umgestaltet.
Das Immunsystem zur Toleranz anleiten
Die Autoren untersuchten anschließend wichtige T‑Zelltypen, die mitentscheiden, ob der Darm ruhig oder aggressiv auf Eindringendes reagiert. Eine Gruppe, peripher induzierte regulatorische T‑Zellen (pTregs), hilft, Überreaktionen auf Nahrung und harmlose Mikroben zu verhindern. Eine andere Gruppe, Th17‑Zellen, kann je nach „Stimmung“ entweder schädliche Entzündungen antreiben oder eine gesunde Barriere unterstützen. Die McB‑Fütterung erhöhte pTregs kräftig entlang des gesamten Darms, selbst wenn die meisten Darmmikroben durch Antibiotika ausgeschaltet wurden. Dagegen hingen McB‑Effekte auf Th17‑Zellen von der Anwesenheit und normalen Funktion der Darmbakterien ab. Bei mikrobiell intakten Mäusen verschob McB Th17‑Zellen in einen beruhigenderen, IL‑10‑produzierenden und weniger entzündlichen Zustand. Wurde die Fermentation blockiert, verschwand diese tolerogene Verschiebung, was unterstreicht, dass McB teilweise wirkt, indem es die Kommunikation zwischen Mikroben und Immunsystem umlenkt.
Den Darm bei Verletzung schützen
Um zu prüfen, ob diese Veränderungen in echten Schutz umschlagen, setzten die Forscher Mäuse zwei starken Darmschädigungen aus. Die eine war das Chemotherapeutikum 5‑Fluorouracil, das weitreichende Schäden und die Verkürzung der fingerartigen Zotten, die Nährstoffe aufnehmen, verursacht. Die andere war eine chemische Substanz (DSS), die Kolitis auslöst — ein Modell für Entzündungen des Dickdarms. Mäuse mit McB‑Diät verloren weniger Gewicht, behielten längere Zotten und Kolonlänge, zeigten weniger blutende Läsionen und hatten in beiden Modellen niedrigere mikroskopische Schadenswerte. Diese Vorteile blieben bestehen, selbst wenn CD4‑T‑Zellen experimentell entfernt wurden, was darauf hindeutet, dass McB‑vermittelte Darm‑Schutzwirkungen nicht ausschließlich auf adaptive Immunzellen zurückgehen, sondern auch direkte Effekte auf die Darmschleimhaut einschließen.
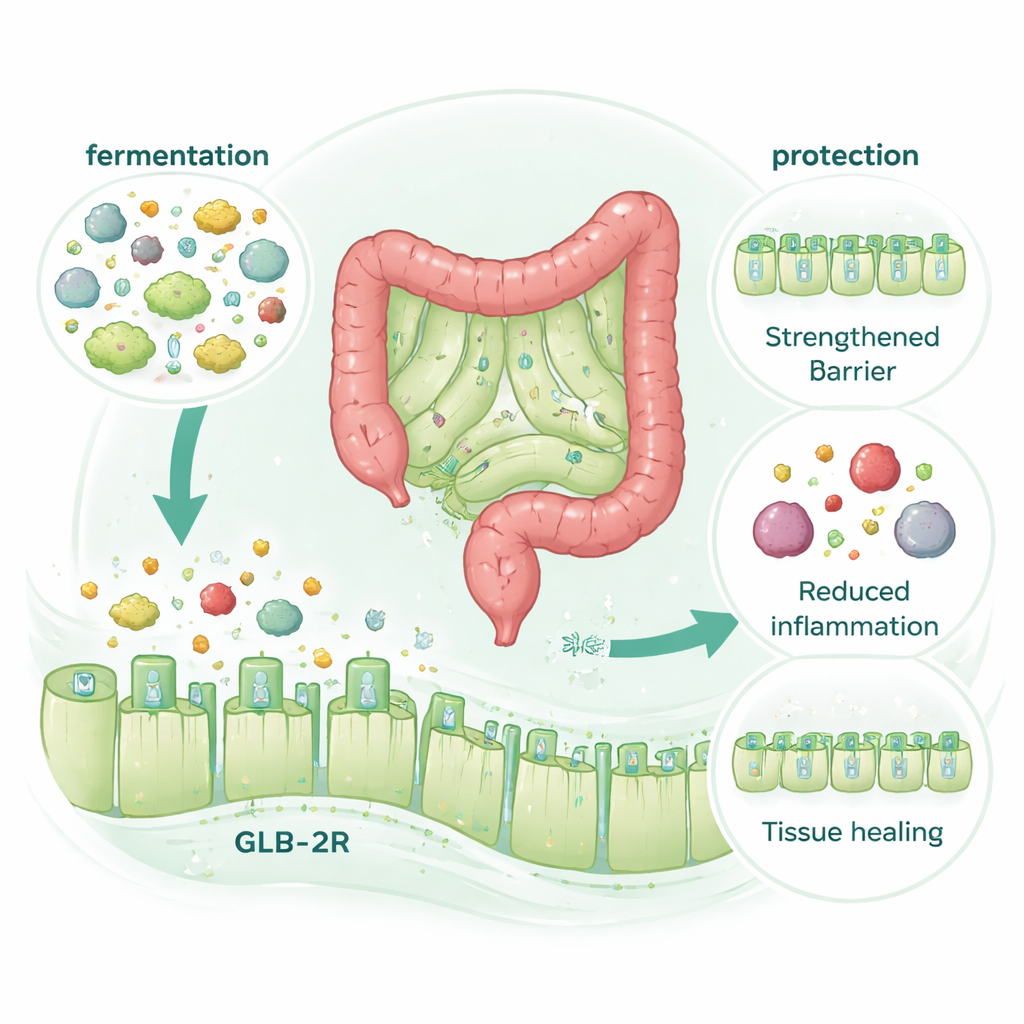
Ein Hormonrezeptor, aber kein zusätzliches Hormon
Eine überraschende Entdeckung war, dass der schützende Effekt von McB unbedingt den Darmrezeptor für ein reparationsförderndes Hormon namens GLP‑2 (der GLP‑2‑Rezeptor, oder GLP‑2R) erforderte, nicht aber den verwandten GLP‑1‑Rezeptor. Fehlt Mäusen der GLP‑2R, schützte McB sie nicht mehr vor Schäden durch Chemotherapie oder Kolitis. Dennoch erhöhte McB selbst nicht die GLP‑2‑Spiegel im Blut, selbst wenn Verdauung und Hormonabbau sorgfältig kontrolliert wurden. Stattdessen verschwanden die Vorteile, wenn die mikrobielle Fermentation im Dickdarm chemisch blockiert wurde, obwohl sich die Gesamtzusammensetzung der Mikrobiota kaum veränderte. Das deutet auf einen Mechanismus hin, bei dem die mikrobielle Aufspaltung von McB kleine Verbindungen erzeugt, die wie GLP‑2‑„Mimetika“ wirken und dessen Rezeptor aktivieren, um die Barriere zu stärken und die Reparatur zu fördern — ohne vermehrte Ausschüttung des Hormons.
Was das für zukünftige Lebensmittel bedeuten könnte
Für eine allgemeine Leserschaft lautet die Kernbotschaft: Manche künftigen Proteinquellen könnten nicht nur klimafreundlich gestaltet werden, sondern auch aktiv die Darmgesundheit unterstützen. In Mäusen bewirkte ein kommerziell skalierbares McB‑Lysat sowohl eine Umprogrammierung des Immunsystems in Richtung Toleranz als auch eine verbesserte Widerstandsfähigkeit des Darms gegen schwere Verletzungen — durch zwei teilweise unabhängige Wege: eine direkte Stärkung regulatorischer T‑Zellen und eine fermentationsgetriebene Aktivierung des GLP‑2‑Rezeptors, die die Gewebereparatur fördert. Während Studien am Menschen noch ausstehen, legt die Arbeit nahe, dass mikrobenabgeleitete Proteine eine neue Klasse von „intelligenten“ Lebensmitteln bilden könnten — die uns nähren, mit unseren eigenen Mikroben zusammenarbeiten und die natürlichen Abwehrkräfte des Darms gegen Entzündung dezent unterstützen.
Zitation: Yang-Jensen, S.K., Choi, B.SY., Nägele, N.S. et al. Microbial activation of the GLP-2R mitigates gastrointestinal inflammation. Nat Commun 17, 1839 (2026). https://doi.org/10.1038/s41467-026-68551-9
Schlüsselwörter: Darmentzündung, mikrobielles Protein, Mikrobiom, GLP-2-Rezeptor, regulatorische T‑Zellen