Clear Sky Science · de
Etherlipide beeinflussen das Schicksal von Krebszellen durch Modulation der Eisenaufnahme
Wie ein wenig bekanntes Fett die Schwachstelle von Krebs offenlegen könnte
Krebs wird oft als „Krankheit der Gene“ bezeichnet, doch diese Studie zeigt, dass die Fette, aus denen die Außenhülle einer Zelle besteht, genauso wichtig sein können. Die Forschenden enthüllen, wie eine spezielle Fettklasse, die Etherlipide genannt wird, gefährlichen Krebszellen hilft, Eisen aus ihrer Umgebung aufzunehmen – was sowohl ihre Fähigkeit zur Ausbreitung fördert als auch ihre Anfälligkeit für eine neu erkannte Form des Zelltods erhöht. Dieses versteckte Zusammenspiel zwischen Zellmembran, Eisen und Tumorverhalten zu verstehen, könnte Wege zu Therapien öffnen, die gezielt die aggressivsten Krebszellen eliminieren.
Ein anderer Blick auf Krebszellen
Die meisten Krebsstudien konzentrieren sich auf DNA‑Mutationen und die von ihnen kodierten Proteine. Diese Arbeit richtet den Fokus auf die Zellmembran – die dünne, ölige Hülle um jede Zelle. In dieser Hülle gibt es viele Arten von Lipiden (Fetten), jeweils mit eigenen Formen und physikalischen Eigenschaften. Die Autorinnen und Autoren konzentrieren sich auf Etherlipide, die in vielen Säugetierzellen etwa ein Fünftel der Phospholipide ausmachen, aber relativ wenig untersucht wurden. Sie zeigen, dass hoch metastasierende, stammzellähnliche Krebszellen ihre Membranen mit Etherlipiden anreichern, wodurch diese Membranen eine niedrige Spannung und hohe Fluidität erhalten. Diese physikalischen Eigenschaften verändern wiederum, wie Zellen Eisen aufnehmen – ein Metall, das sowohl Tumorwachstum antreiben als auch einen zerstörerischen Prozess namens Ferroptose auslösen kann, eine eisenabhängige Form des Zelltods.
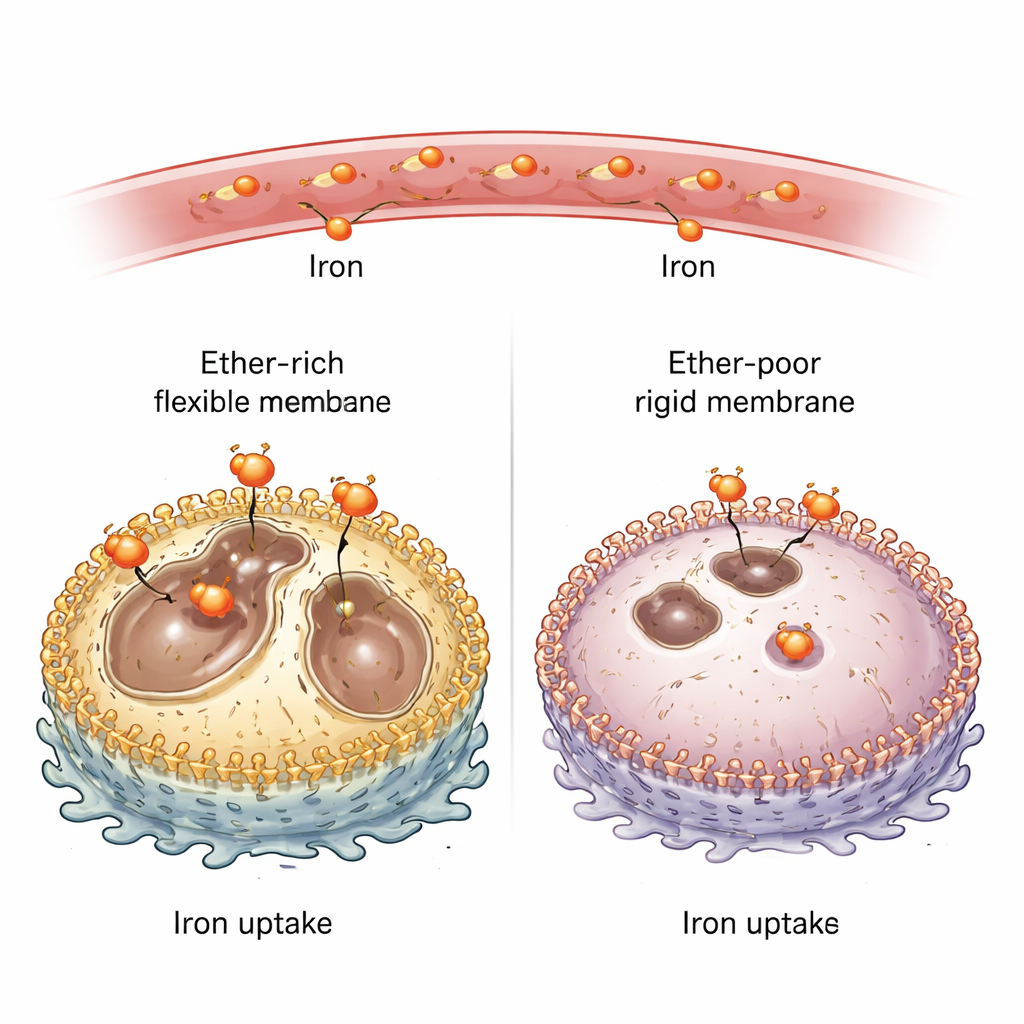
Die Verbindung von Membranfetten und Eisenaufnahme
Um Etherlipide zu untersuchen, schaltete das Team in mehreren Maus‑ und menschlichen Krebszelllinien Schlüsselenzyme aus, die für deren Herstellung nötig sind. Ohne diese Enzyme fielen die Etherlipide in der Plasmamembran von etwa einem Viertel aller Lipide auf nur noch wenige Prozent ab. Überraschenderweise wiesen diese etherarmen Zellen deutlich weniger „redox‑aktives“ Eisen auf – die chemisch reaktive Form, die an Oxidationsreaktionen beteiligt ist – sowohl in Kultur als auch in in Mäusen implantierten Tumoren. Als die Forschenden von außen zusätzliches Eisen zuführten, stiegen die Eisenwerte der Zellen wieder an und sie wurden erneut empfindlich gegenüber Ferroptose‑auslösenden Wirkstoffen. Das zeigte, dass Etherlipide mehr tun, als nur als brennbarer Brennstoff für Oxidation zu dienen; sie steuern aktiv, wie viel Eisen in die Zelle gelangt.
Ein spezialisiertes Eisentor: Der CD44‑Weg
Die Forschenden fragten dann, wie die Membranzusammensetzung die Eisenaufnahme verändert. Zellen nehmen Eisen typischerweise über ein bekanntes Protein auf, den Transferrinrezeptor, aber aggressive, stammzellähnliche Krebszellen nutzen zusätzlich einen anderen Weg: ein Oberflächenprotein namens CD44, das Eisen aufnimmt, das an ein Zuckermolekül namens Hyaluronan gebunden ist. Durch Verfolgung fluoreszenter Sonden zeigte das Team, dass das Entfernen von Etherlipiden die Aufnahme über den Transferrinrezeptor kaum beeinflusste, wohl aber die CD44‑vermittelte Endozytose stark verlangsamte – eine alternative, clathrinunabhängige Route, Material in die Zelle zu bringen. Die Wiederherstellung von Etherlipiden oder ihre Zugabe in Form von Liposomen belebte diesen CD44‑Weg wieder. Die Störung von CD44 selbst oder der Abbau von Hyaluronan senkten das zelluläre Eisen, was bestätigte, dass dieser etherabhängige Weg ein wichtiges Eisentor in diesen Krebszellen darstellt.
Wie weichere Membranen das Zellverhalten verändern
Warum sind Etherlipide für CD44 so wichtig, nicht aber für den klassischen Eisenrezeptor? Die Antwort liegt in der Physik. Mit präzisen Werkzeugen, die winzige Fäden aus der Zelloberfläche ziehen, zeigten die Autorinnen und Autoren, dass etherreiche Membranen eine geringere Spannung haben und sich leichter verformen lassen. Wenn Etherlipide entfernt wurden, stieg die Membranspannung und die Lipide packten dichter, wodurch die Membran steifer wurde. Diese Veränderungen behinderten stark die Formen der Endozytose, die von flexiblen, flöschenähnlichen Membranabschnitten abhängen – genau die Art, die CD44 nutzt – während die clathrinbasierte Aufnahme weitgehend intakt blieb. Etherlipide halfen außerdem, „Lipid‑Rafts“ zu stabilisieren, winzige geordnete Inseln in der Membran, in denen CD44 sich sammelt, bevor es nach innen gezogen wird. Kurz gesagt, Etherlipide stimmen die physikalische Landschaft der Membran so ab, dass die CD44‑gesteuerte Eisenaufnahme begünstigt wird.
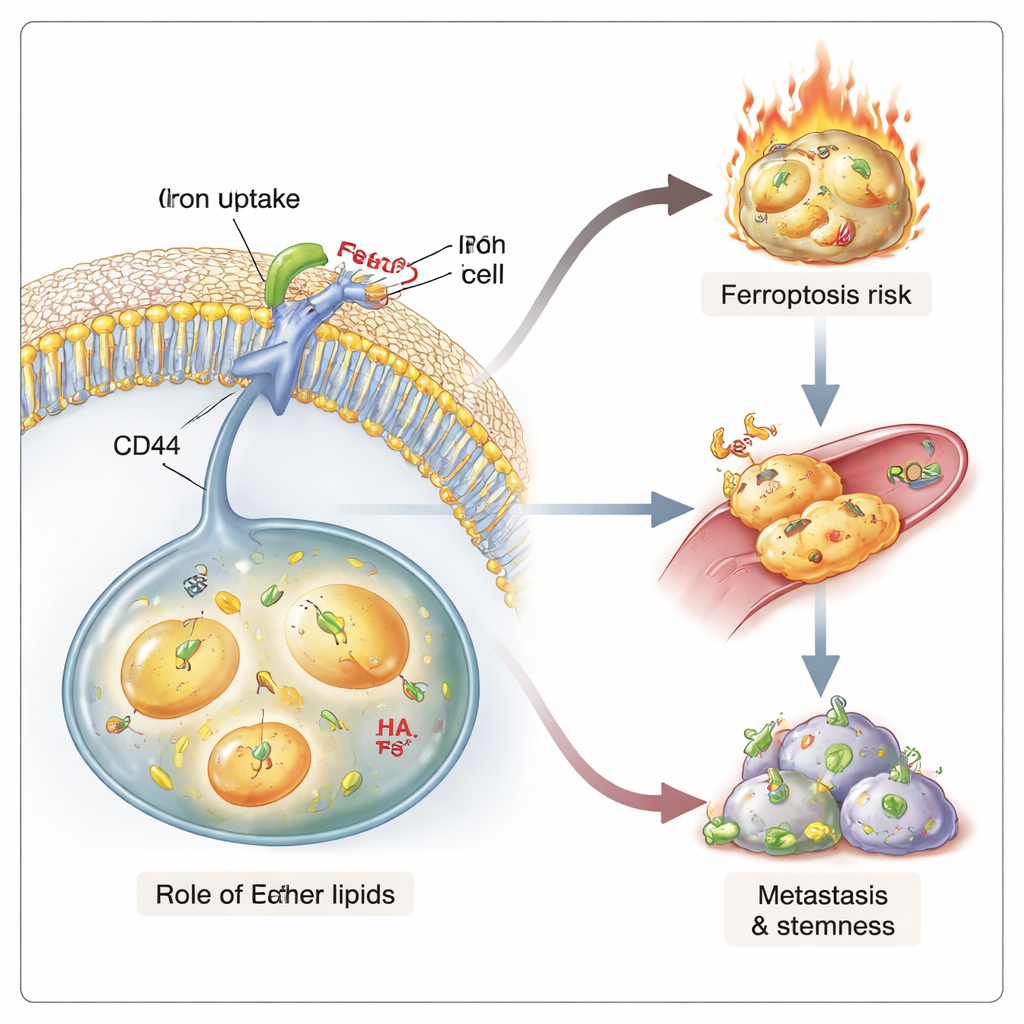
Sowohl Ausbreitung als auch Selbstzerstörung antreiben
Hohe Eisenwerte und niedrige Membranspannung stehen in Verbindung mit Eigenschaften, die Krebs tödlich machen: der Fähigkeit, neue Tumoren zu bilden, und der Überlebensfähigkeit gegenüber Therapien. In dreidimensionalen Mikrovessel‑Modellen quetschten sich etherreiche Krebszellen leichter aus gefäßähnlichen Strukturen – ein frühes Stadium der Metastasierung. In Mäusen bildeten etherdefiziente Krebszellen weniger Metastasen, obwohl ihre Primärtumoren in ähnlichem Tempo wuchsen. Diese Zellen zeigten zudem reduzierte „Stammigkeit“, gemessen an ihrer verminderten Fähigkeit, in Kultur Mammosphären zu bilden und Tumoren in limiting‑dilution‑Implantaten zu initiieren. Gleichzeitig waren etherreiche Zellen mit ihrer höheren Eisenbelastung und leichter oxidierbaren Lipiden empfindlicher gegenüber Ferroptose, wenn sie mit spezifischen Wirkstoffen oder Immunhinweisen konfrontiert wurden. So erzeugen Etherlipide einen zweischneidigen Zustand: Sie unterstützen aggressives, stammzellähnliches Verhalten, machen diese Zellen aber gleichzeitig durch eisengetriebene Lipid‑Schäden besonders angreifbar.
Warum das für zukünftige Krebstherapien wichtig ist
Für Nicht‑Spezialisten ist die Kernbotschaft, dass nicht alle Krebszellen gleich gefährlich sind und ihre Außenmembranen mitbestimmen, wie bedrohlich und wie verwundbar sie sind. Etherlipide formen die Zelloberfläche so um, dass Eisen durch eine spezialisierte Tür hineinfließen kann, wodurch metastasierende, stammzellähnliche Zellen angetrieben werden, gleichzeitig aber mit den Bausteinen für ihre eigene Zerstörung beladen werden. Therapien, die die Produktion von Etherlipiden verändern, die CD44‑basierte Eisenaufnahme stören oder gezielt Ferroptose auslösen, könnten diese schwer behandelbaren Zellpopulationen selektiv angreifen und gleichzeitig normales Gewebe schonen. Indem diese Studie zeigt, wie eine wenig bekannte Fettklasse Membranphysik, Metallstoffwechsel und Zellschicksal verbindet, öffnet sie einen neuen Weg zu intelligenteren, präziseren Krebsinterventionen.
Zitation: Mansell, R.P., Müller, S., Yang, JS. et al. Ether lipids influence cancer cell fate by modulating iron uptake. Nat Commun 17, 1835 (2026). https://doi.org/10.1038/s41467-026-68547-5
Schlüsselwörter: Etherlipide, Krebsstammzellen, Eisenaufnahme, Ferroptose, Metastasierung