Clear Sky Science · de
Adipozytärer Sclerostin loop3-LRP4-Interaktion, die Sclerostin zur Beeinträchtigung des gesamten Fett- und Glukosestoffwechsels benötigt
Warum Knochen für den Blutzucker wichtig sind
Die meisten Menschen betrachten Knochen als lebloses Gerüst, doch Knochenzellen setzen still Hormone frei, die mit dem Rest des Körpers kommunizieren. Diese Studie zeigt, wie ein solches Knochenprotein, Sclerostin genannt, eine Verbindung zwischen zwei sehr häufigen Problemen älterer Frauen herstellt: brüchigen Knochen (Osteoporose) und Typ-2-Diabetes. Indem die Forschenden einen spezifischen „Handschlag“ zwischen Sclerostin und Fettzellen offenlegen, skizzieren sie einen Weg, Knochen zu stärken und gleichzeitig Blutzucker und Cholesterin zu verbessern, ohne das Herz zusätzlich zu belasten.
Ein fehlgeleitetes Knochensignal
Sclerostin ist ein Protein, das vorwiegend von Knochenzellen gebildet wird. Es bremst normalerweise die Knochenbildung und schützt, einigermaßen überraschend, auch Blutgefäße. Das Team konzentrierte sich auf ein kleines Segment dieses Proteins, genannt loop3, und untersuchte, ob es eine Rolle bei gestörtem Fett- und Zuckerstoffwechsel spielt. Sie fanden heraus, dass Frauen mit postmenopausaler Osteoporose, die zudem Typ-2-Diabetes hatten, sowie Personen mit frisch diagnostiziertem Diabetes höhere Sclerostinwerte im Blut aufwiesen als vergleichbare Personen ohne Diabetes. Bei Mäusen, die zur Nachahmung metabolischen Stresses mit fettreicher Kost gefüttert wurden, stiegen die Sclerostinwerte zusammen mit Gewichtszunahme, höheren Blutfettwerten und schlechterer Blutzuckerregulation. Diese Muster deuteten darauf hin, dass überschüssiges Sclerostin mehr als ein bloßer Beobachter der Stoffwechselerkrankung sein könnte.
Einen winzigen Loop mit großer Wirkung zerlegen
Um zu verstehen, was loop3 bewirkt, erzeugten die Forschenden Mäuse, bei denen Sclerostin verändert oder das loop3-Segment entfernt wurde. Mäuse, die normales Sclerostin im Übermaß produzierten, sammelten mehr Fett in ihren weißen Fettdepots an, hatten größere Fettzellen, höhere zirkulierende Fettsäurespiegel sowie schlechtere Glukosetoleranz und Insulinantwort als normale Mäuse. Als loop3 genetisch gelöscht oder subtil mutiert wurde, verbesserten sich diese Probleme: Fettpolster waren kleiner, Fettzellen schrumpften, Blutfette sanken und die Zuckerregulation besserte sich. Bemerkenswerterweise traten ähnliche Vorteile auf, wenn Mäuse mit einem speziell entworfenen, DNA-ähnlichen Wirkstoff (einem Aptamer) behandelt wurden, der an loop3 bindet und dessen Funktion blockiert, ohne die Menge an Sclerostin im Blut zu verändern.
Wie Fettzellen das Knochensignal „hören“
Die Gruppe richtete dann den Blick auf Fettzellen, um zu sehen, wie loop3 seine schädliche Botschaft übermittelt. Sie konzentrierten sich auf ein Rezeptorprotein an der Fettzelloberfläche namens LRP4, das zuvor dafür bekannt war, Sclerostin bei der Wirkung auf Knochen zu unterstützen. In Zellkulturversuchen zeigten sie, dass loop3 physikalisch an einen spezifischen Abschnitt von LRP4 auf Fettzellen bindet. Dieser Kontakt löste Veränderungen aus, die die Fähigkeit der Zellen erhöhten, Fette aufzubauen und abzubauen und mehr Glukose aus dem Blut aufzunehmen, was zu übergroßen, überaktiven Fettzellen führte. Wenn die Wissenschaftler entscheidende Bausteine in LRP4 so veränderten, dass loop3 nicht mehr andocken konnte, oder wenn sie ein kleines blockierendes Peptid hinzufügten, das die Andockstelle von LRP4 nachahmte, wurde die Wirkung von Sclerostin auf Fettansammlung und Zuckeraufnahme stark reduziert. Sowohl in Zellen als auch in Mäusen stellte die Blockade dieser loop3–LRP4-Interaktion eine normalere Fettzellgröße wieder her und verbesserte die Glukosetoleranz.
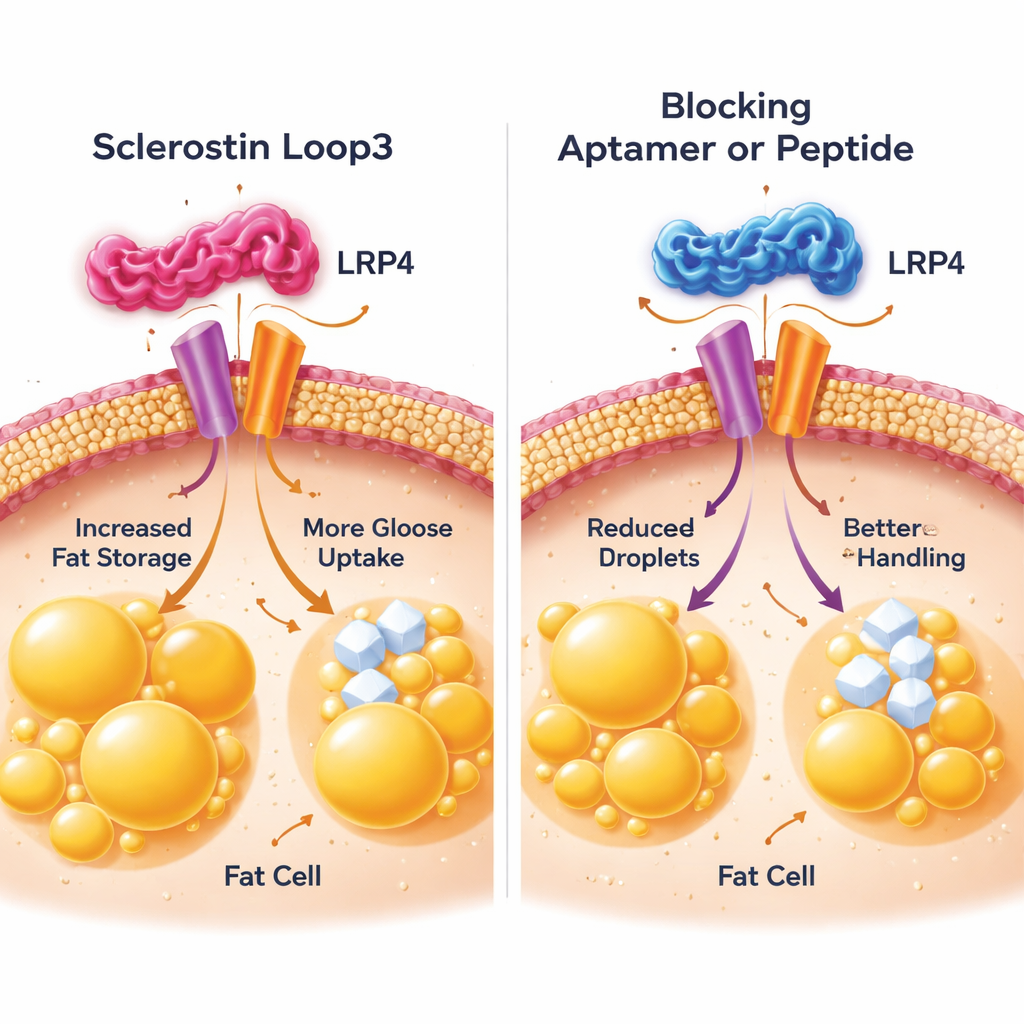
Stärkere Knochen, gesünderer Stoffwechsel
Eine wichtige Sorge bei bestehenden Sclerostin-blockierenden Medikamenten gegen Osteoporose ist, dass sie zwar Knochen aufbauen und den Stoffwechsel verbessern, Regulierungsbehörden aber vor einem erhöhten Risiko schwerer Herzprobleme gewarnt haben. Frühere Arbeiten dieser Gruppe zeigten, dass loop3 für Sclerostins Bremswirkung auf die Knochenbildung entscheidend ist, nicht jedoch für seine herzschützenden Effekte. Hier zeigen sie weiter, dass die gezielte Behandlung von loop3 – sei es durch genetische Modifikationen oder durch loop3-fokussierte Wirkstoffe – den gesamten Fett- und Zuckerstoffwechsel in mehreren Mäusemodellen verbessert und gleichzeitig Knochenmasse und -stärke erhöht. Im Gegensatz zu aktuellen Medikamenten löste diese Strategie keinen kompensatorischen Anstieg eines anderen knochenbezogenen Inhibitors, DKK1, aus, der die langfristigen Vorteile abschwächen kann.
Was das für Patienten bedeuten könnte
Einfach gesagt argumentiert die Studie, dass ein sehr kleines Stück eines Knochenhormons sowohl schlechte Knochengesundheit als auch metabolische Erkrankung vorantreibt, indem es direkt mit Fettzellen kommuniziert. Durch die Unterbrechung des Gesprächs zwischen dem loop3-Segment von Sclerostin und dem LRP4-Rezeptor auf Fettzellen könnte es möglich werden, Therapien zu entwickeln, die Knochen stärken und Blutfette sowie Blutzucker normalisieren, während die herzschützenden Funktionen von Sclerostin erhalten bleiben. Für postmenopausale Frauen, die häufig sowohl an Osteoporose als auch an Typ-2-Diabetes leiden, könnten solche loop3-gerichteten Therapien eines Tages eine sicherere, länger anhaltende Möglichkeit bieten, zwei Erkrankungen gleichzeitig zu behandeln.
Zitation: Jiang, H., Tao, X., Yu, S. et al. Adipocytic sclerostin loop3-LRP4 interaction required by sclerostin to impair whole-body lipid and glucose metabolism. Nat Commun 17, 1812 (2026). https://doi.org/10.1038/s41467-026-68526-w
Schlüsselwörter: sclerostin, loop3, LRP4, Osteoporose, Typ-2-Diabetes