Clear Sky Science · de
Palmitinsäure‑ausgelöste Palmitoylierung von B7H3 fördert die Immunflucht
Warum diese Forschung für Krebspatienten wichtig ist
Die meisten Menschen wissen, dass neue Immuntherapien das Immunsystem dabei unterstützen können, Krebs anzugreifen, doch viele Patientinnen und Patienten mit häufigem kolorektalem (Darm‑)Krebs profitieren kaum davon. Diese Studie deckt einen verborgenen biochemischen Mechanismus auf, den Darmtumoren nutzen, um sich vor Immunangriffen zu schützen, und weist auf einen neuen Wirkstofftyp — ein kleines Peptid — hin, der die Wirksamkeit von Immuntherapien für diese Patientengruppe verbessern könnte.
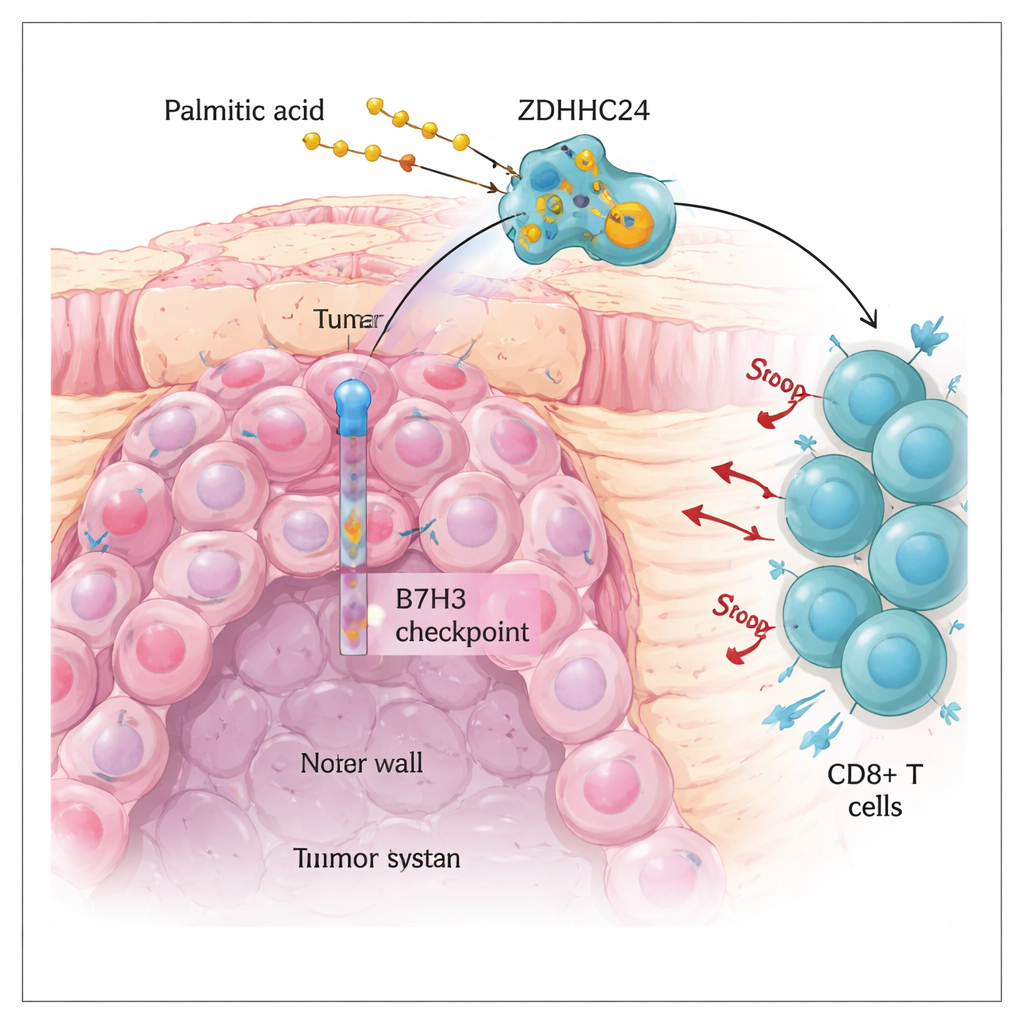
Ein Hindernis der aktuellen Darmkrebs‑Immuntherapie
Kolorektaler Krebs gehört zu den häufigsten Krebserkrankungen weltweit. Immuntherapeutika, die immunologische „Bremsen“ lösen, wie PD‑1‑ und PD‑L1‑Inhibitoren, haben die Behandlung für eine Minderheit von Patientinnen und Patienten mit stark mutierten Tumoren (sogenannte MSI‑H‑Tumoren) revolutioniert. Leider sprechen die meisten kolorektalen Karzinome, die mikrosatellitenstabil (MSS) sind, schlecht auf diese Therapien an. Die Autoren konzentrierten sich auf ein anderes Bremsmolekül namens B7H3, das auf der Tumorzelloberfläche sitzt und die Aktivität von Killerzellen, insbesondere CD8+‑T‑Zellen, dämpft. Sie fanden heraus, dass das B7H3‑Protein in MSS‑Tumoren stark erhöht ist und mit schlechterem Überleben korreliert, obwohl das zugrunde liegende B7H3‑Gen nicht stärker aktiv ist. Diese Diskrepanz warf eine wichtige Frage auf: Was hält das B7H3‑Protein auf Tumorzellen so reichlich vorhanden?
Wie ein verbreitetes Fett Tumoren beim Verstecken hilft
Das Team vermutete, dass der Tumorstoffwechsel B7H3 stabilisieren könnte. Durch den Vergleich der Genaktivität und kleiner Molekülprofile von MSS‑ und MSI‑H‑Kolonkarzinomen entdeckten sie, dass sich viele fettbezogene Stoffwechselwege unterscheiden, wobei eine Fettsäure besonders auffiel: Palmitinsäure. Als sie Darmkrebszellen im Labor verschiedenen Fettabbauprodukten aussetzten, erhöhte nur Palmitinsäure klar die B7H3‑Proteinmenge. Weitere Experimente zeigten den Grund: Palmitinsäure geht in eine chemische Modifikation namens Palmitoylierung ein, bei der eine Fettsäurekette an spezifische Stellen von Proteinen angehängt wird. Diese Modifikation, vermittelt durch ein Enzym namens ZDHHC24 an einer einzelnen Cystein‑Position innerhalb von B7H3, machte B7H3 stabiler und auf der Tumorzelloberfläche häufiger vorhanden.
Den Entsorgungsweg der Immunbremse blockieren
Zellen beseitigen normalerweise unerwünschte oder beschädigte Proteine über Systeme, die wie Recycling und Müllabfuhr funktionieren. Die Forschenden zeigten, dass B7H3 hauptsächlich über einen zellulären „Selbst‑Fress“‑Weg namens Autophagie abgebaut wird, der ein Rezeptorprotein namens SQSTM1/p62 verwendet, um Fracht für die Zerstörung zu markieren. Wenn B7H3 palmitoyliert war, band es schlecht an diesen Rezeptor und entging so der autophagischen Degradation, was zu anhaltend hohen Mengen der immunhemmenden Komponente führte. Wenn die Palmitoylierungsstelle so mutiert wurde, dass sie den Fettanhang nicht mehr tragen konnte, oder wenn das Enzym ZDHHC24 gelöscht wurde, wurde B7H3 effizienter in die zellulären „Mülltüten“ geleitet und abgebaut. In Mäusen wuchsen Tumoren ohne palmitoyliertes B7H3 langsamer, veränderten nicht ihre intrinsische Wachstumsrate in immundefizienten Tieren und zeigten deutlich mehr CD8+‑T‑Zellen sowie stärkere tumorabtötende Aktivität. Das demonstrierte, dass die Modifikation hauptsächlich dadurch wirkt, dass sie die Immunantwort lahmlegt, nicht dadurch, dass sie die Teilungsrate der Krebszellen verändert.
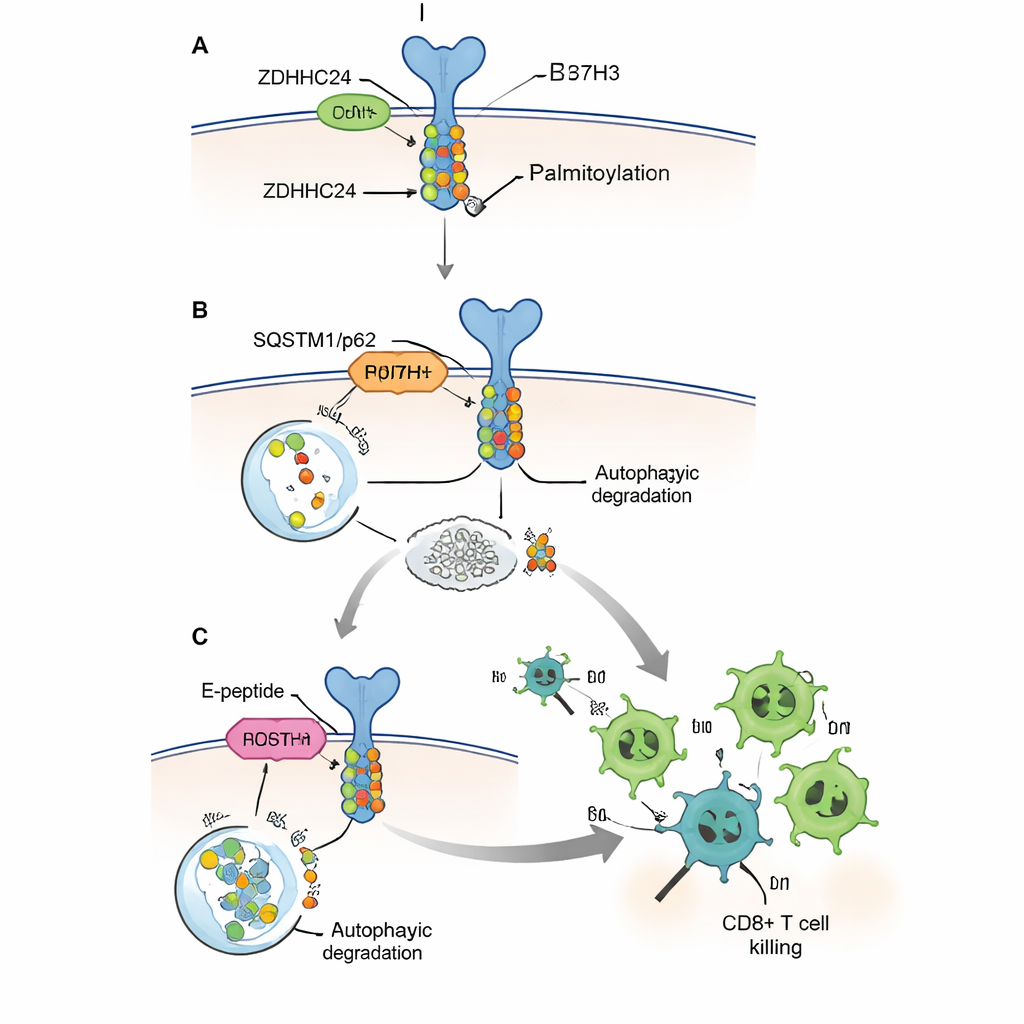
Den Schild abschwächen und T‑Zellen stärken
Da das vollständige Entfernen von ZDHHC24 oder B7H3 genetisch keine praktikable Therapie beim Menschen darstellt, entwarfen die Autoren ein kurzes, zellgängiges Peptid, das sie E‑Peptid nennen. Es ahmt einen kleinen Abschnitt des B7H3‑Proteins nach, der normalerweise an ZDHHC24 bindet, und wirkt als Köder, der das Enzym daran hindert, echte B7H3‑Moleküle zu modifizieren. In kultivierten Zellen reduzierte das E‑Peptid die Palmitoylierung und den Proteinspiegel von B7H3, stellte dessen Erkennung durch die Autophagie‑Maschinerie wieder her und ermöglichte menschlichen CD8+‑T‑Zellen, Tumorzellen effizienter zu töten. In mehreren Mausmodellen, einschließlich eines humanisierten Mausmodells mit menschlichen Immunzellen und menschlichen Darmtumoren, führten Injektionen des E‑Peptids zu Tumorschrumpfung, zu einer erhöhten Zahl von CD8+‑T‑Zellen in den Tumoren und zu einer gesteigerten Produktion wichtiger Killer‑Moleküle wie Granzyme B und Interferon‑gamma.
Ein neuer Partner für bestehende Immuntherapien
Schließlich prüften die Forschenden, ob diese Strategie mit dem standardmäßigen PD‑1‑Blocker zusammenwirken kann. In Mausmodellen des kolorektalen Krebses zeigten sowohl das E‑Peptid allein als auch ein Anti‑PD‑1‑Antikörper allein eine gewisse Tumorkontrolle. Kombiniert ergaben beide Behandlungen jedoch eine deutlich stärkere und länger anhaltende Tumorsuppression, in einigen Fällen verschwanden die Tumoren sogar, und die mittlere Überlebenszeit verdoppelte sich gegenüber den Kontrollen. Das legt nahe, dass das Ausschalten des B7H3‑Schilds durch Entfernen seines Fett‑„Ankers“ bestehende Checkpoint‑Medikamente, die den PD‑1‑Weg angreifen, ergänzen kann.
Was das für zukünftige Krebsbehandlungen bedeutet
Kurz gefasst zeigt diese Studie, dass eine verbreitete Nahrungsfettsäure, Palmitinsäure, von Darmtumoren missbraucht werden kann, um ein immunblockierendes Protein (B7H3) chemisch zu verstärken und dem Krebs beim Verstecken zu helfen. Durch das Blockieren dieser einzelnen chemischen Bindung konnten die Autoren die „Rüstung“ entfernen, die zelleigenen Entsorgungssysteme B7H3 abbauen lassen und CD8+‑T‑Zellen wieder Zugang geben, um anzugreifen. Während das E‑Peptid selbst ein experimentelles Werkzeug im Frühstadium ist, identifiziert die Arbeit die Palmitoylierung von B7H3 — und ihr Enzym ZDHHC24 — als vielversprechende Arzneimittelziele. Wenn ähnliche Wirkstoffe in Menschen sicher und wirksam wären, könnten sie eines Tages mehr kolorektale Karzinome von „kalten“ Tumoren, die auf Immuntherapie nicht ansprechen, in „heiße“ Tumoren verwandeln, die das Immunsystem erkennen und zerstören kann.
Zitation: Rao, Z., Huang, C., Wu, Q. et al. Palmitic acid-triggered B7H3 palmitoylation promotes immune escape. Nat Commun 17, 1810 (2026). https://doi.org/10.1038/s41467-026-68525-x
Schlüsselwörter: Immuntherapie bei Darmkrebs, B7H3 Checkpoint, Palmitinsäure‑Stoffwechsel, Proteinpalmitoylierung, CD8‑T‑Zell‑Tumorimmunität