Clear Sky Science · de
Zebrafisch-Makrophagen wandeln physikalische Wunds Signale in schnelle Gefäßdurchlässigkeit um
Wie ein winziger Fisch uns etwas über Wundschwellung lehrt
Wenn Sie sich das Knie aufschürfen, wird die Stelle rasch rot, geschwollen und durch Flüssigkeit durchtränkt. Diese schnelle Veränderung der umliegenden Blutgefäße ist entscheidend, um Infektionen zu bekämpfen und die Reparatur in Gang zu setzen, doch wie der Körper innerhalb von Sekunden Schäden erkennt und reagiert, war in Echtzeit schwer zu beobachten. Mithilfe durchschaubarer Zebrafisch-Larven und fortschrittlicher Live-Bildgebung zeigt diese Studie, wie spezialisierte Immunzellen, die Blutgefäße umschließen, den physikalischen Schock einer Wunde in nahezu sofortiges Gefäßleck umwandeln und liefert neue Einsichten in Entzündung, Heilung und sogar menschliche Lungenschädigung.
Beobachtung, wie sich Verletzung im Körper ausbreitet
Die Forscher arbeiteten mit jungen Zebrafischen, deren transparente Körper es erlauben, Zellen und Blutgefäße unter dem Mikroskop zu verfolgen. Sie schnitten die Spitze der Schwanzflosse ab und füllten den Kreislauf mit einem leuchtenden Farbstoff, der in gesunden Gefäßen bleibt. Wenn die verletzten Fische wieder in normales Süßwasser gelegt wurden, erzeugte der plötzliche Wassereintritt in die Gewebe einen „osmatischen Schock“ rund um die Wunde. Innerhalb von Minuten weiteten sich nahe Gefäße und begannen, den fluoreszenten Farbstoff ins umliegende Gewebe entweichen zu lassen, was der Schwellung und dem Ausfließen ähnelt, wie es bei menschlichen Wunden vorkommt. Durch das Wechseln der Fische zwischen normalem und speziell ausbalancierten Salz- oder Zuckerlösungen zeigte das Team, dass diese schnelle Gefäßdurchlässigkeit stark von osmotischen Veränderungen abhängt und nicht allein durch einfaches Geweberiss ausgelöst wird.
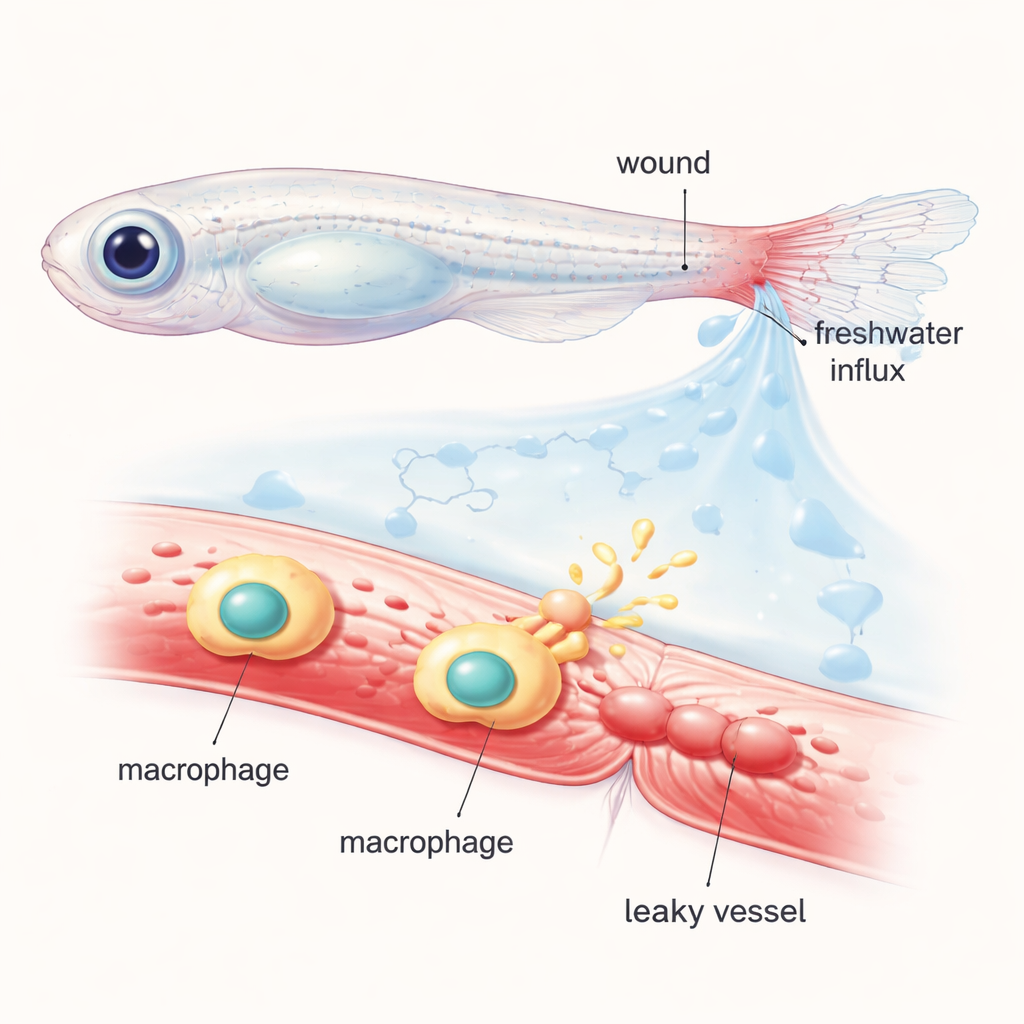
Verfolgung der chemischen Botenstoffe hinter dem Leck
Um herauszufinden, welche Moleküle den physikalischen Schock in ein Leck-Signal umwandeln, untersuchten die Wissenschaftler eine Familie von Fettsäureverbindungen, die Eicosanoide genannt werden und aus Arachidonsäure entstehen. Diese Lipide sind für ihre Rollen bei Entzündungen und der Durchblutung bekannt. Mithilfe genetischer Mutanten und Arzneimittel schalteten sie gezielt einzelne Enzyme im Eicosanoid-Weg aus. Die Blockade eines Schlüsselenzyms namens Alox5a (5-Lipoxygenase) oder seines Partners Lta4h reduzierte deutlich die Menge an Farbstoff, die nach osmatischem Schock aus den Blutgefäßen entwich, ohne jedoch den Wundverschluss selbst zu verhindern. Im Gegensatz dazu hatten Eingriffe in andere verwandte Enzyme wenig Effekt. Das deutete auf einen spezifischen Zweig des Lipidwegs als Haupttreiber der schnellen Leckantwort hin, der fast wie ein chemisches Ventil funktioniert, das auf Knopfdruck geöffnet oder geschlossen werden kann.
Die überraschende Rolle der gefäßumschließenden Immunzellen
Im Blut zirkulieren verschiedene Typen von Immunzellen; bei Zebrafisch-Larven sind Neutrophile und Makrophagen die Hauptakteure. Das Team nutzte einen eleganten genetischen Trick, um vor der Verletzung selektiv entweder Neutrophile oder Makrophagen zu vernichten. Das Entfernen der Neutrophilen veränderte die Gefäßleckage kaum. Wurden jedoch Makrophagen eliminiert, sank die Leckreaktion um etwa die Hälfte — ein Effekt, der dem der Blockade des Alox5a–Lta4h-Lipidwegs entspricht. Wichtig ist, dass diese Eingriffe den schnellen Wundverschluss nicht verhinderten, was zeigt, dass die Rekrutierung von Leukozyten und das Gefäßleck gewissermaßen unabhängig gesteuert werden können. Das enthüllte perivaskuläre Makrophagen — Makrophagen, die eng an der Außenseite von Gefäßen liegen — als Schlüsselübersetzer zwischen physischer Verletzung und vaskulärem Verhalten.
Von der Kernverformung zum chemischen Signal
Wie erkennen diese perivaskulären Makrophagen eine Wunde, die etwas entfernt liegen kann? Die Antwort liegt in der Art, wie sich ihre Zellkerne auf mechanischen Stress hin verhalten. Wenn sich der osmatische Schock von der Wunde durch das angrenzende Gewebe ausbreitet, führt der Wassereintritt zu subtiler Zellschwellung und Kernverformung. Die Forscher markierten ein mechanosensitives Enzym namens cPla2 mit einem fluoreszierenden Marker und exprimierten es spezifisch in Makrophagen. Nach der Verletzung im normalen Süßwasser wanderte cPla2 rasch an die innere Oberfläche der Kernmembran in Makrophagen und lief als Welle durchs Gewebe mit einer Geschwindigkeit von etwa 50 Mikrometern pro Sekunde — ein Tempo, das der Ausbreitung gelöster Salze entspricht. Diese Translokation hing von hypotonen Bedingungen ab und war in isotonischen Lösungen deutlich schwächer. Makrophagen in Gefäßnähe zeigten besonders ausgeprägte, reversible Pulse von nuklearem cPla2-Binden, was wiederum Arachidonsäure freisetzt, die in die leak-auslösenden Lipide umgewandelt wird.
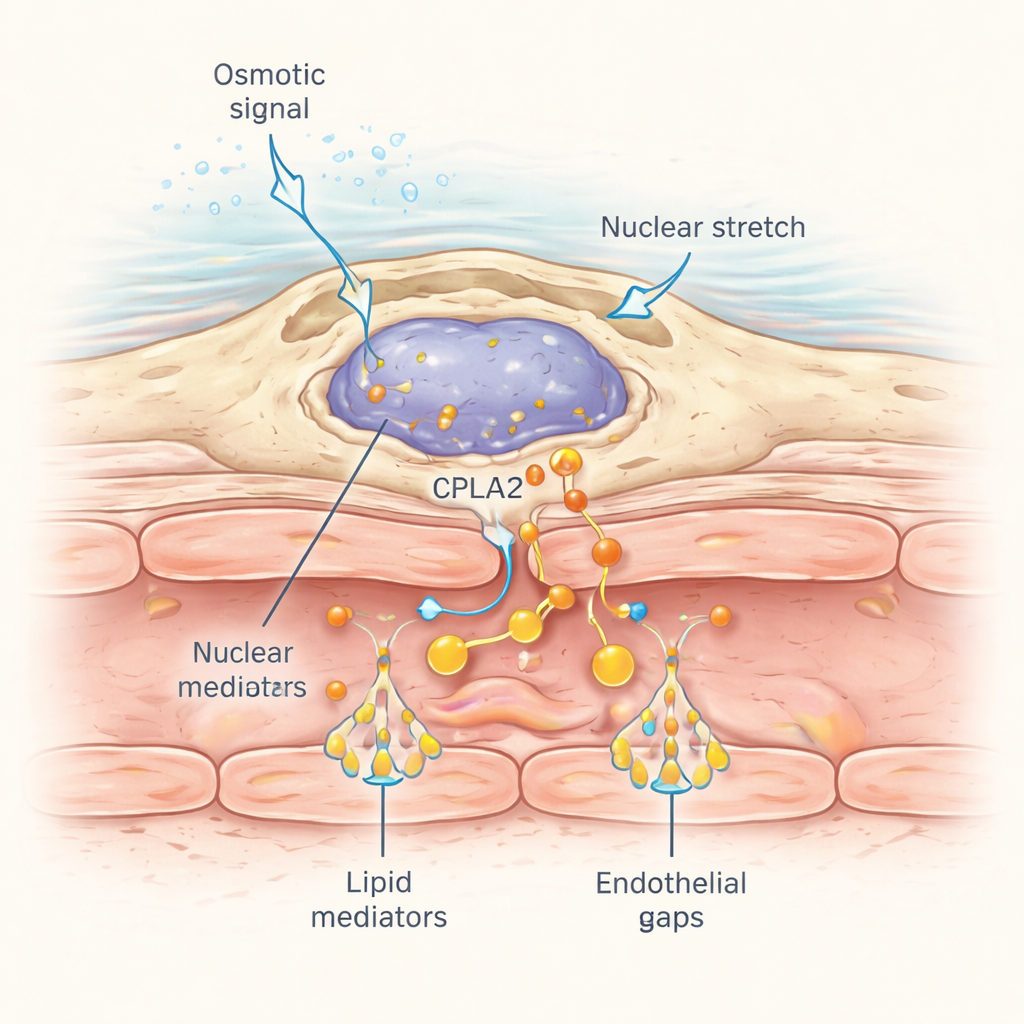
Warum das über Fische hinaus wichtig ist
Kurz gesagt zeigt diese Studie, dass bestimmte Makrophagen als physische Wächter fungieren: Sie spüren die Dehnung von Gewebe- und Kernmembranen durch osmotische Veränderungen an einer Wunde, schalten cPla2 an ihrer Kernoberfläche ein und produzieren rasch lipidische Botenstoffe, die den umliegenden Blutgefäßen signalisieren, „die Tore zu öffnen“, damit Flüssigkeit und Immunfaktoren einströmen können. Obwohl Zebrafische im Süßwasser leben und besonderen osmotischen Herausforderungen ausgesetzt sind, dürften ähnliche mechanosensitive Wege in menschlichem Gewebe aktiv sein, das wechselnden Druck- und Strömungsbedingungen ausgesetzt ist — etwa die Lungen bei mechanischer Beatmung. Das Verständnis, wie Kernverformung und Lipidsignale die Gefäßpermeabilität in Echtzeit steuern, könnte schließlich Behandlungen informieren, die Entzündungen feinjustieren — entweder indem schädliches Austreten bei Erkrankungen wie akutem Lungenversagen gedämpft wird oder indem hilfreiche Reaktionen gefördert werden, um die Gewebereparatur zu beschleunigen.
Zitation: Gelashvili, Z., Shen, Z., Ma, Y. et al. Zebrafish macrophages convert physical wound signals into rapid vascular permeabilization. Nat Commun 17, 1807 (2026). https://doi.org/10.1038/s41467-026-68520-2
Schlüsselwörter: Wundheilung, Blutgefäße, Makrophagen, Entzündung, Zebrafisch