Clear Sky Science · de
Ultradünne Flüssigzellen für mikrosekunden-aufgelöste Kryo-EM
Proteine bei der Arbeit in Echtzeit beobachten
Viele der Maschinen, die unsere Zellen am Leben erhalten, bestehen aus Proteinen, und häufig kennen wir ihr Aussehen, wenn sie in einer eingefrorenen Stellung vorliegen. Was wir jedoch wirklich sehen wollen, ist, wie sie sich bewegen, während sie ihre Aufgaben erfüllen. Diese Studie stellt eine neue Methode vor, um solche Bewegungen auf unglaublich kurzen Zeitskalen — Millionstel einer Sekunde — zu beobachten, ohne die scharfen Details zu opfern, die moderne Kryo‑Elektronenmikroskopie (Kryo‑EM) liefert.
Ein neues Fenster in die mikroskopische Welt
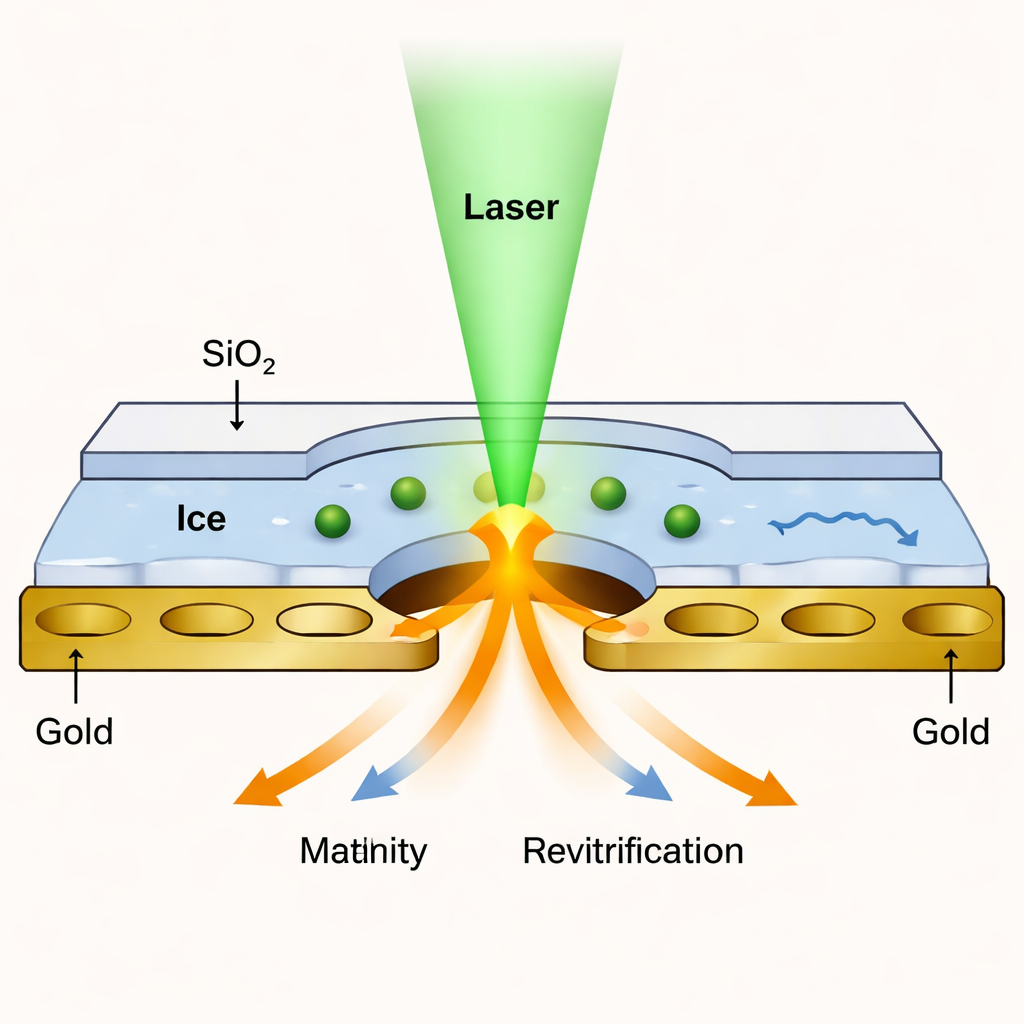
Kryo‑EM hat die Strukturbiologie revolutioniert, indem es eingefrorene Proteine in annähernd atomarer Auflösung abbildet. Traditionelle Methoden zeigen jedoch nur Stillbilder. Um Bewegung einzufangen, haben Forscher die „mikrosekunden-aufgelöste Kryo‑EM“ entwickelt: Ein Laser schmilzt kurz ein gefrorenes Präparat, sodass Proteine sich bewegen können, und das Präparat wird dann schnell wieder eingefroren, um die neuen Positionen einzufangen. Das Problem war bisher, dass die winzige Flüssigkeitsschicht, die durch den Laser entsteht, nach einigen Dutzend Mikrosekunden zu zerfallen droht, was die Beobachtungszeit begrenzt. Die neue Arbeit löst diesen Engpass, indem sie die Probe in einer ultradünnen Flüssigzelle einschließt und so lange stabil hält, dass auch langsamere, komplexere Bewegungen beobachtet werden können.
Bau einer ultradünnen Flüssigzelle
Das Team entwickelte eine Art nanoskopisches Sandwich: Die Proteinlösung wird auf einem Standard-Lochgitter aus Gold eingefroren und dann auf beiden Seiten mit Siliziumdioxid-Schichten von nur etwa 1,4 Nanometern Dicke — nur wenige Atomlagen — beschichtet. Diese glasartigen Schichten fungieren als transparente Deckel, die verhindern, dass die Flüssigkeit verdampft, wenn der Laser das Eis schmilzt. Kurze Laserpulse erwärmen die versiegelte Probe auf eine kontrollierte Temperatur und erlauben ein Wiedereinfrieren innerhalb von Mikrosekunden. Da die Membranen so dünn sind, lassen sie dennoch genügend Elektronen durch, damit das Mikroskop Bilder mit nahezu derselben Auflösung wie bei konventioneller Kryo‑EM erzeugen kann — im Test an Apoferritin erzielten die Autoren Auflösungen von etwa 1,7–1,8 Å.
Scharfere Ansichten und gleichmäßigere Winkelverteilungen
Eine verborgene Herausforderung in der Kryo‑EM ist, dass Proteine dazu neigen, an der Luft‑Wasser‑Grenzfläche in der dünnen Eisschicht zu haften, wodurch sie ähnliche Orientierungen einnehmen und eine vollständige 3D-Rekonstruktion erschweren. Die Siliziumdioxid-Beschichtungen in diesen Flüssigzellen ändern die Oberfläche von Wasser‑Luft zu Wasser‑Feststoff und machen sie verträglicher für Wasser. Infolgedessen bleiben Proteine seltener in einer einzigen Pose hängen. Bei Tests an einer großen zellulären Maschine, dem 50S-Ribosomuntereinheit, stellten die Autoren fest, dass die Winkelverteilung der Partikel nahezu perfekt gleichmäßig wurde, wodurch das langjährige Problem der „bevorzugten Orientierung“ im Wesentlichen beseitigt wurde, während die hohe Auflösung in den Endrekonstruktionen erhalten blieb.
Die zeitliche Steuerung der Bewegung eines molekularen Hebels
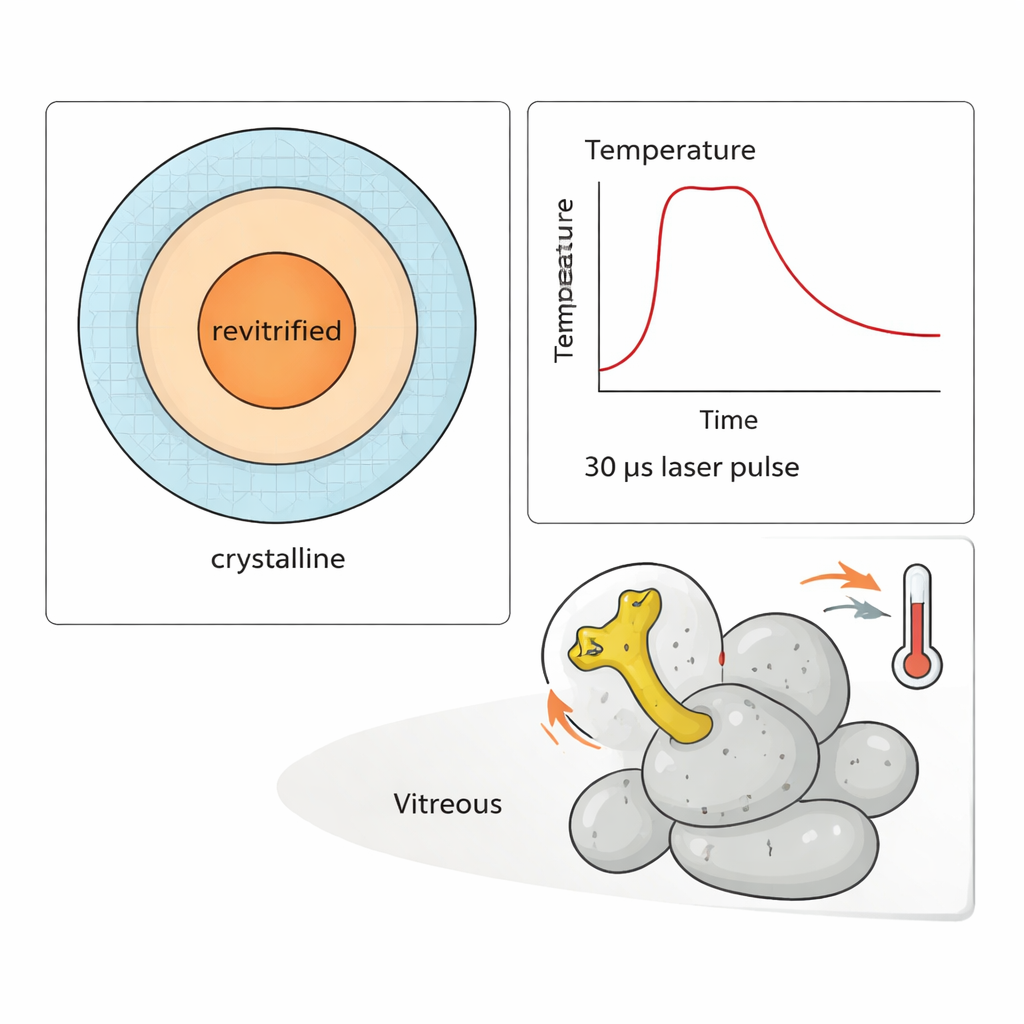
Um die Leistungsfähigkeit ihrer Methode zu demonstrieren, führten die Forscher ein „Temperatursprung“-Experiment an der 50S-Untereinheit durch. Ein flexibler Arm dieses Partikels, bekannt als L1‑Schnauze, schwingt während der Proteinsynthese wie ein Hebel. Durch Abgabe von Pulsen aus 30‑Mikrosekunden-Lasern konnten sie die Probe für bis zu etwa 300 Mikrosekunden auf unterschiedliche Temperaturen erwärmen und dann erneut einfrieren. Simulationen und Messungen, welche Bereiche als Glas wieder erstarrten, erlaubten eine Abschätzung der Temperatur für jedes beobachtete Partikel. Die Analyse Tausender Bilder zeigte, dass die Amplitude der L1‑Schnauzenbewegung mit der Temperatur deutlich zunimmt — jedoch erst nach Hunderten von Mikrosekunden. Zu frühen Zeiten spiegelt die Verteilung der Konformationen noch den ursprünglichen, raumtemperaturähnlichen Zustand vor dem Einfrieren wider.
Warum das für die zukünftige Biologie wichtig ist
Für Nicht‑Fachleute ist die Kernbotschaft, dass dieses Design ultradünner Flüssigzellen die Beobachtungsdauer von Proteinbewegungen drastisch verlängert, ohne die strukturellen Details zu verwischen. Es verschiebt die mikrosekunden-aufgelöste Kryo‑EM von der Erfassung nur der schnellsten Ereignisse hin zu Untersuchungen langsamerer, biologisch relevanter Umlagerungen — etwa der verzögerten Reaktion der L1‑Schnauze auf einen Wärmestoß. Mit weiteren Verbesserungen könnte dieser Ansatz die Lücke bis in den Millisekundenbereich und darüber hinaus überbrücken; er bietet zudem neue Wege zur Probenvorbereitung, zur Reduktion von Bildartefakten und zum Auslösen von Reaktionen direkt auf dem Gitter. Praktisch bedeutet das: Wissenschaftler kommen dem Ziel immer näher, „molekulare Filme“ zu erstellen, die die Gestalt von Proteinen mit ihrer tatsächlichen Funktion in lebenden Zellen verknüpfen.
Zitation: Curtis, W.A., Wenz, J., Krüger, C.R. et al. Ultrathin liquid cells for microsecond time-resolved cryo-EM. Nat Commun 17, 1799 (2026). https://doi.org/10.1038/s41467-026-68515-z
Schlüsselwörter: zeitaufgelöste Kryo-EM, Proteindynamik, Flüssigzellen-Elektronenmikroskopie, Ribosom L1-Schnauze, ultradünne Siliziumdioxid-Membranen