Clear Sky Science · de
Bionisches Janus-Hydrogel fördert die Regeneration infizierter Achillessehnen durch mechano-immunes räumlich-zeitliches Steuern
Warum das für verletzte Sehnen wichtig ist
Rissbildungen der Achillessehne sind sowohl bei Sportlern als auch bei älteren Menschen häufig. Wenn die Verletzung von Bakterien besiedelt wird, verläuft die Heilung oft schlecht: Die Sehne kann an Festigkeit verlieren, an umliegendes Gewebe verkleben oder sogar erneut einreißen. Diese Studie stellt einen neuen „intelligenten" Hydrogelverband vor, der von der natürlichen Sehnenscheide inspiriert ist und während einer Operation auf eine infizierte Sehne aufgetragen werden kann. Er verfolgt drei Ziele gleichzeitig: mechanischen Schutz der Sehne, Abtötung medikamentenresistenter Bakterien und eine sanfte Steuerung des Immunsystems weg von schädlicher Entzündung hin zu echter Regeneration.
Ein zweigleisiger Verband, von der Natur inspiriert
Gesunde Sehnen liegen in einer gleitfähigen Hülle, die ihnen ein reibungsloses Gleiten ermöglicht und gleichzeitig festen Halt bietet. Chirurgen tun sich schwer, dies nach einer Reparatur nachzubilden: Materialien, die gut an der Sehne haften, neigen oft auch dazu, am umliegenden Gewebe zu kleben und schmerzhafte Verwachsungen zu verursachen. Die Forschenden übertrugen dieses natürliche Prinzip von „Haftung plus Schmierung" auf ein Janus(zweigeteiltes)-Hydrogel namens HAPP@H-EXO. Die eine Seite greift die Sehnenoberfläche stark mit reversiblen chemischen Bindungen und Wasserstoffbrücken, was solide mechanische Unterstützung bietet. Die gegenüberliegende Seite ist lotusblattähnlich behandelt, wasserabweisend und reibungsarm, sodass angrenzende Gewebe nicht haften. So entsteht eine Schutzmanschette, die mit der Sehne mitbewegt, aber Verwachsungen zur Umgebung verhindert. 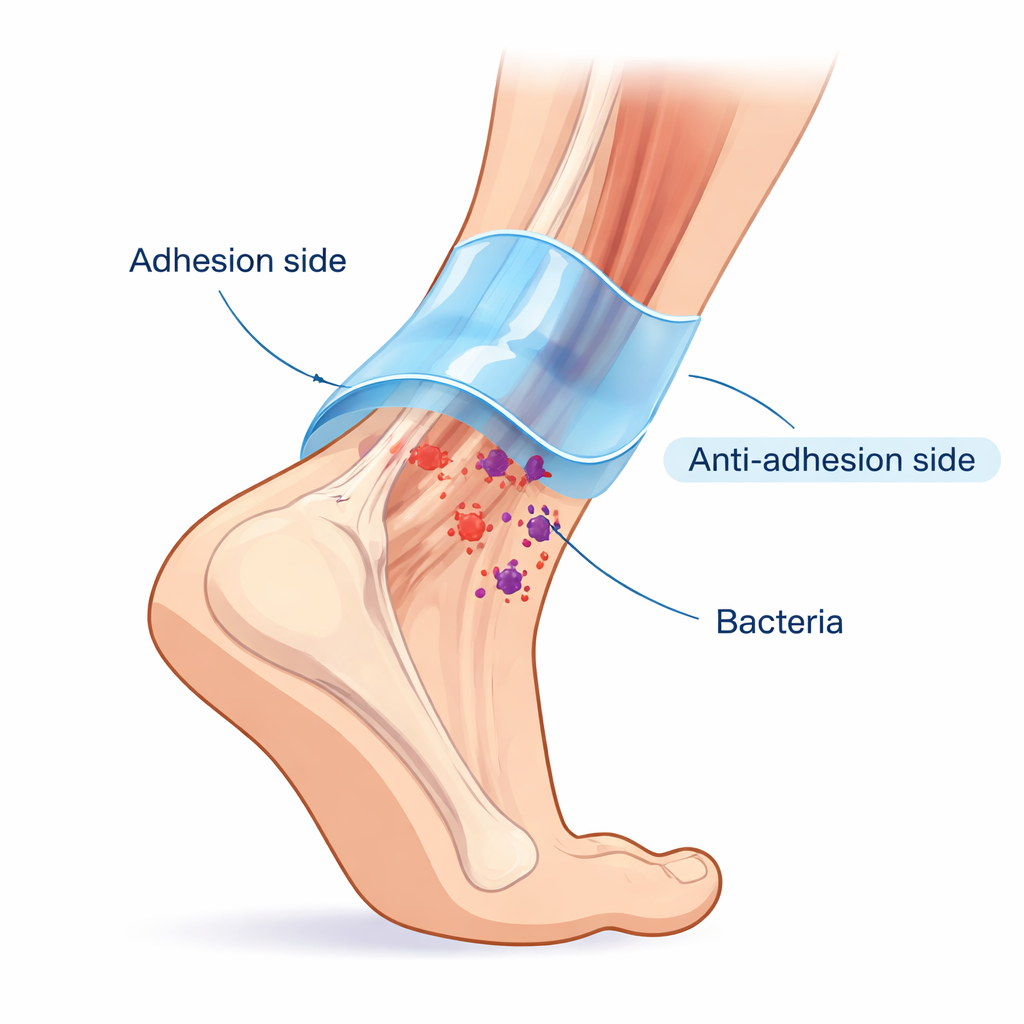
Entwickelt, um Last zu teilen und wiederholte Beanspruchung zu überstehen
Im Gegensatz zu vielen weichen Gelen ist dieses Material so ausgelegt, dass es in einer harten mechanischen Umgebung bestehen kann: Jeder Schritt belastet und entlastet die Achillessehne. Das Team kombinierte ein steifes, permanent vernetztes Netzwerk mit einem zweiten, dynamischen Netzwerk, das sich unter Belastung umordnen kann. Tests zeigten, dass das Hydrogel sich dehnt und zusammendrückt, ohne zu reißen, über mindestens 100 Kraftzyklen seine Festigkeit behält und wenig Energie dissipiert — es federt also zurück, statt sich langsam zu verformen. Computersimulationen deuteten darauf hin, dass sich, wenn das Gel um eine genähte Sehne gelegt wird, die hohen Spannungen an den Stichpunkten zu den Sehnenrändern verteilt und so die Chance eines neuen Einreißens an der Reparaturstelle reduziert. In Tierversuchen führte dies zu reparierten Sehnen, deren Festigkeit und Steifigkeit denen normalen Gewebes nahekamen.
Bakterien einfangen und Resistenz verhindern
Bakterielle Infektionen sind ein Hauptgrund für das Scheitern von Sehnenreparaturen, besonders bei multiresistenten Stämmen wie MRSA. Anstatt sich auf traditionelle Antibiotika zu stützen, fängt das Hydrogel Bakterien physikalisch ein und tötet sie ab. Eine Komponente, eine Phenylboronsäuregruppe, erkennt zuckerreiche Strukturen an bakteriellen Zellwänden und bildet reversible Bindungen mit ihnen, wodurch Bakterien aus dem umliegenden Flüssigkeitsfilm herausgezogen werden. Eine weitere Komponente, ein positiv geladenes Polymer, destabilisiert dann bakterielle Membranen, sodass sie aufbrechen. In Labortests tötete das Gel MRSA, häufige Staphylokokken und E. coli schnell ab, baute robuste Biofilme auf, und behielt seine antibakterielle Wirksamkeit über Tage und mehrere Einsatzzyklen, ohne dass Bakterien Resistenzen gegen das Einfang- oder Tötungsprinzip entwickelten. 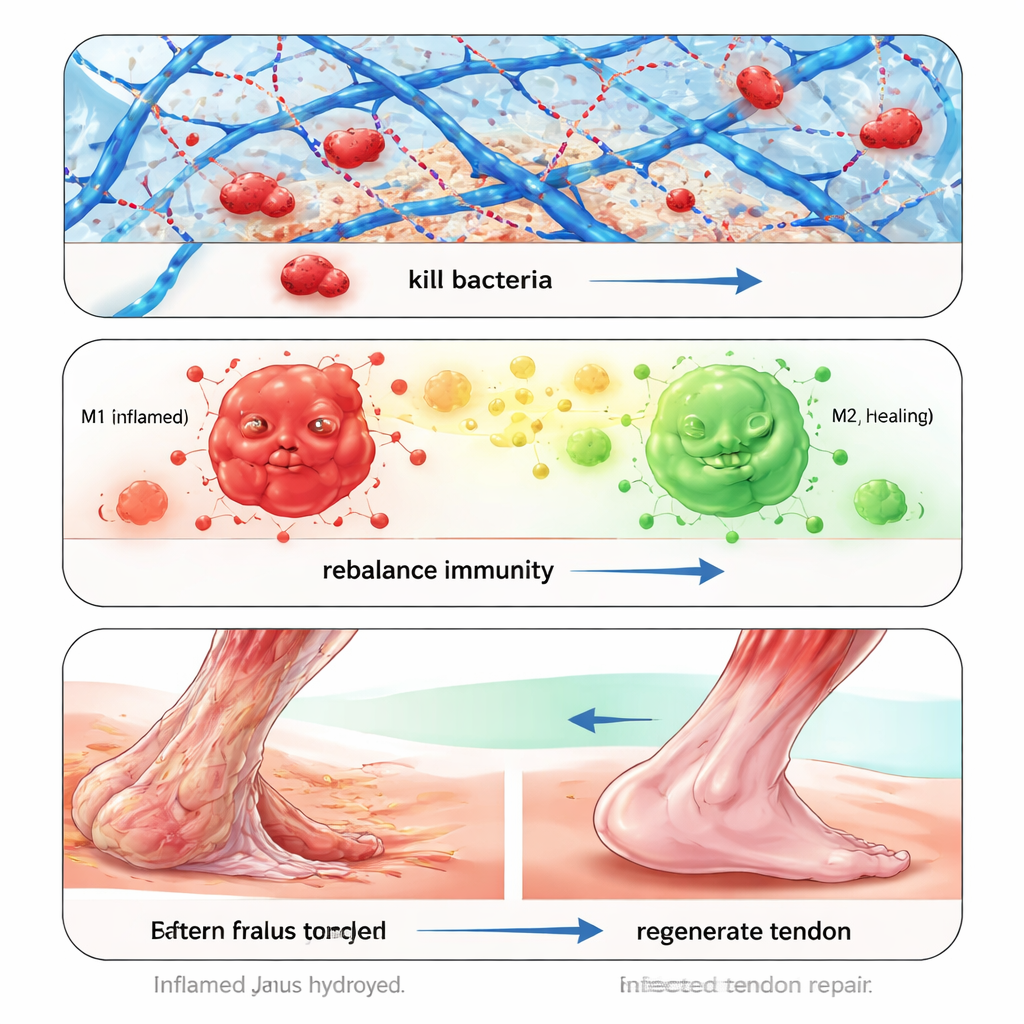
Das Immunsystem lenken und Gewebe neu aufbauen
Selbst wenn Bakterien entfernt sind, bleiben infizierte Sehnen oft in einem Zustand von oxidativem Stress und chronischer Entzündung, was die normale Reparatur blockiert. Um dem entgegenzuwirken, luden die Forschenden das Hydrogel mit winzigen Membranpaketen — Exosomen —, die von Sehnenstammzellen stammen, die unter niedrigem Sauerstoff gezüchtet wurden. Diese „hypoxischen" Exosomen sind reich an antiinflammatorischen und pro-regenerativen Signalen. Die Chemie des Gels sorgt dafür, dass Exosomen in der sauren, entzündeten Frühphase schneller freigesetzt werden und langsamer, wenn sich die Bedingungen normalisieren. In Zellversuchen reduzierten exosombeladene Gele schädliche reaktive Sauerstoffspezies, stellten die Mitochondrienfunktion wieder her, förderten die Bildung von Blutgefäßen und verschoben Immunzellen von einem entzündungsfördernden Zustand (M1) hin zu einem heilungsfördernden Zustand (M2). Genanalysen deuteten auf eine Dämpfung des NF-κB-Signalwegs hin, eines zentralen Treibers der Entzündung.
Von der infizierten Ruptur zur funktionellen Erholung
In Ratten- und Kaninchenmodellen mit absichtlich mit MRSA infizierten Achillessehnen führte das Auftragen des Janus-Hydrogels bei der Operation dazu, dass innerhalb einer Woche im Operationsbereich nahezu keine lebenden Bakterien mehr nachweisbar waren. In den folgenden Wochen zeigten behandelte Sehnen weniger oxidativen Schaden, weniger Entzündungsmarker und mehr pro-heilende Signale als unbehandelte Kontrollen. Die Mikroskopie zeigte besser ausgerichtete, dichtere Kollagenfasern, mehr Blutgefäße und die Expression wichtiger Proteine, die auf Sehnenreife hinweisen. Wichtig war, dass die äußere, nicht haftende Seite des Gels verhinderte, dass die Sehne an umliegendem Gewebe anhaftete — bestätigt durch Bildgebung und makroskopische Untersuchung. Tiere, die mit der exosombeladenen Version behandelt wurden, gewannen normalere Gangmuster und höhere lasttragende Kapazität der Sehne zurück, was auf eine nicht nur strukturelle, sondern auch funktionelle Wiederherstellung hinweist.
Was das für Patienten bedeuten könnte
Diese Arbeit demonstriert ein einzelnes, biomimetisches Material, das mechanische Unterstützung, Infektionskontrolle und immunologische Balance integriert angeht. Durch die Kombination eines zweigeteilten physikalischen Designs mit bakterienfangender Chemie und zeitgesteuerter Freisetzung regenerativer Exosomen half das Janus-Hydrogel infizierten Achillessehnen bei Tieren, stärker zu heilen, mit weniger Narben und besserer Beweglichkeit. Obwohl klinische Studien am Menschen noch nötig sind, deutet der Ansatz auf eine Zukunft, in der komplexe Weichteilverletzungen — insbesondere solche, die durch medikamentenresistente Infektionen kompliziert sind — mit „intelligenten" chirurgischen Verbänden behandelt werden könnten, die den Heilungsprozess aktiv orchestrieren.
Zitation: Li, J., Wang, Z., Yang, W. et al. Bionic Janus hydrogel drives infected Achilles tendon regeneration via mechano-immune spatiotemporal steering. Nat Commun 17, 1805 (2026). https://doi.org/10.1038/s41467-026-68514-0
Schlüsselwörter: Achillessehnenreparatur, Hydrogelverband, medikamentenresistente Infektion, Geweberegeneration, Immunmodulation