Clear Sky Science · de
Mechanische Kräfte aus interzellulärer Peptid-Selbstaggregation treiben die Bildung von Sphäroiden
Mini-Gewebe im Labor aufbauen
Wissenschaftler arbeiten schnell daran, Miniaturversionen menschlicher Gewebe zu schaffen, die sich wie das Original verhalten. Solche lebenden Modelle können die Prüfung von Krebsmedikamenten sicherer machen und neue Behandlungen für Diabetes und andere Erkrankungen näher an die klinische Anwendung bringen. Diese Studie stellt eine clevere Methode vor, Zellen dazu zu bringen, realistischere dreidimensionale Verbände zu bilden, inklusive eigener primitiver „gefäßähnlicher“ Netzwerke, die die Nährstoffversorgung und Funktion verbessern.
Zellen ihre Umgebung spüren lassen
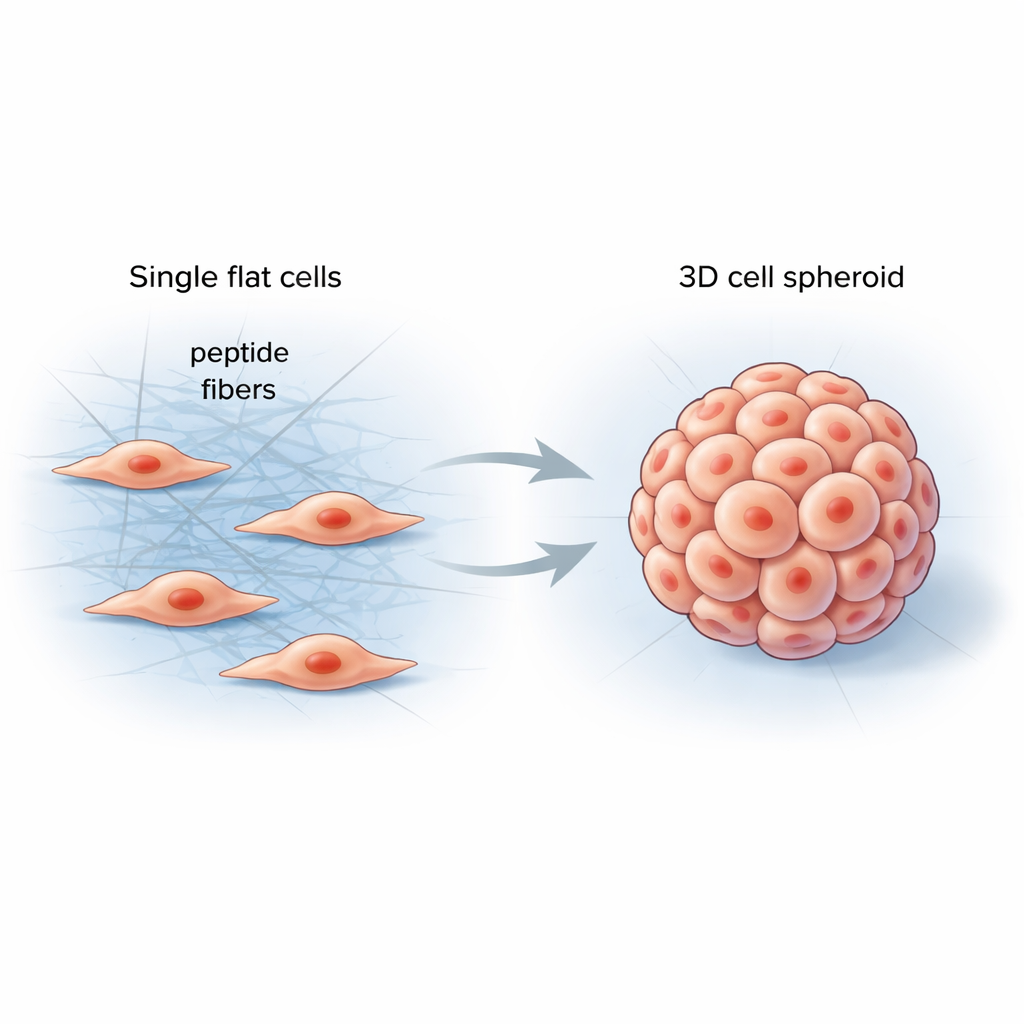
In unserem Körper leben Zellen in einer weichen, aber strukturierten Umgebung, der extrazellulären Matrix – einem Proteinnetz, das Gewebe stützt und Zellen kontinuierlich mechanische Signale sendet. Konventionelle Labormaterialien tun sich schwer, diese Komplexität nachzubilden, und erzeugen oft flache Zellschichten, die sich deutlich anders verhalten als echte Organe oder Tumoren. Die Forscher wollten ein einfaches, programmierbares Material entwerfen, das direkt zwischen Zellen entsteht, ihre Umgebung kontrolliert versteift und sie in natürlichere dreidimensionale Formen lenkt.
Intelligente Peptide, die sich zwischen Zellen zusammensetzen
Das Team entwickelte kurze Eiweißfragmente, sogenannte Peptide, die sich zu langen, dünnen Fasern verknüpfen können, wenn sie auf bestimmte Enzyme an Zelloberflächen treffen. Wurden diese Peptide zu Krebszellen gegeben, blieben sie zunächst inaktiv, wie eine klare Lösung. Sobald die zelleigenen Enzyme einen Teil des Moleküls entfernten, setzten die Peptide schnell selbstorganisierte Faserstrukturen frei, die sich um und zwischen benachbarten Zellen schlangen. Dieses neue Fasergeflecht veränderte die lokalen mechanischen Kräfte, wodurch die Zellen stärker aneinander zogen, ihr internes Gerüst umgestalteten und sich zu runden 3D-Sphäroiden statt zu flachen Schichten zusammenzogen.
Von Zellclustern zu gefäßähnlichen Netzwerken
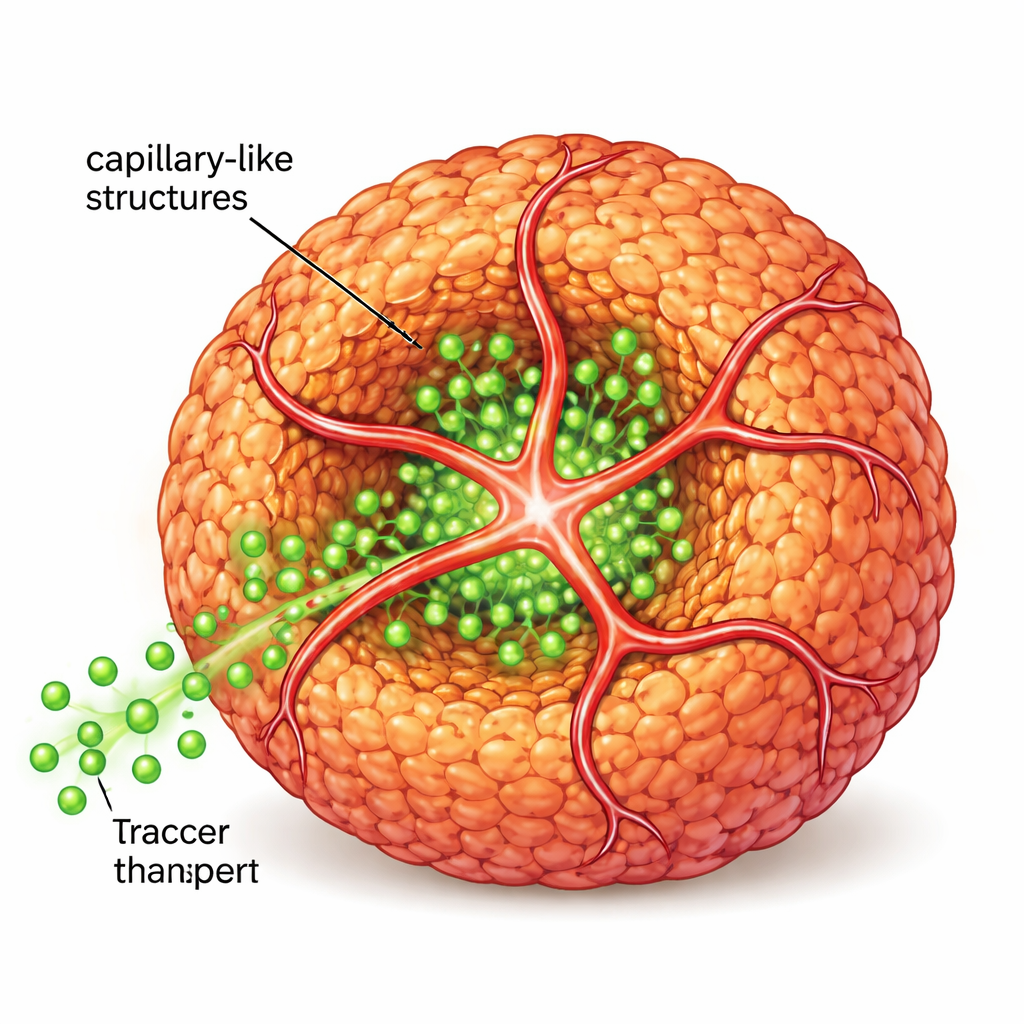
Um dem echten Gewebe näherzukommen, führten die Wissenschaftler anschließend menschliche Endothelzellen ein – jene Zellen, die normalerweise Blutgefäße auskleiden – zusammen mit einem zweiten Peptid, das ein kleines „Adressetikett“ trug, das diese Zellen anzieht. Gemeinsam bildeten das ursprüngliche und das modifizierte Peptid ein gemeinsames Nanofasergerüst. Endothelzellen nutzten dieses Gerüst, um in röhrenartige Ausläufer hervorzuwachsen, die sich um die Sphäroide legten und in sie eindrangen und kapillarähnliche Strukturen bildeten. Als das Team fluoreszierende zuckerähnliche Moleküle um diese Strukturen strömen ließ, zeigten sich eine deutlich tiefere Penetration in den Kern der Sphäroide im Vergleich zu Sphäroiden ohne diese inneren Röhren, was beweist, dass der Transport von Nährstoffen und Signalen wesentlich verbessert wurde.
Näher an echten Tumoren und funktionierenden Inseln
Die Genaktivitätsprofile zeigten, dass Tumorsphäroide mit kapillarähnlichen Strukturen den Proben von Patienten mit Glioblastom ähnlicher waren als traditionelle flache Kulturen oder nicht vaskularisierte Sphäroide. In Mäusen wuchsen Sphäroide mit diesen primitiven Gefäßnetzwerken zu größeren, stärker vaskularisierten Tumoren heran, was darauf hindeutet, dass das in vitro Modell zentrale Merkmale echten Tumorverhaltens einfängt. Die gleiche Strategie wurde auf Pankreas-Beta-Zellen angewendet, die typischerweise in stark vaskularisierten Langerhans-Inseln leben und Insulin als Reaktion auf Glukose ausschütten. Als Beta-Zell-Sphäroide mithilfe des Peptidsystems und Endothelzellen mit kapillarähnlichen Strukturen ausgestattet wurden, zeigten sie deutlich stärkere und fein abgestimmtere Insulinfreisetzung, was auf ein leistungsfähiges Werkzeug für Diabetesforschung und regenerative Medizin hinweist.
Warum das für künftige Therapien wichtig ist
Indem einfache Peptide sich zwischen lebenden Zellen selbst zusammensetzen lassen, bietet diese Arbeit ein allgemeines Rezept zum Aufbau miniaturisierter, vaskularisierter Gewebe, die sich so anfühlen und funktionieren wie Gewebe im Körper. Die resultierenden Sphäroide spiegeln Patienten-Tumoren und funktionierende Inseln besser wider und sind damit wertvoll für Medikamententests, das Studium von Krankheitsmechanismen und die Entwicklung neuer zellbasierter Therapien. Für Nicht-Spezialisten lautet die zentrale Erkenntnis: Wenn man im Labor gezüchteten Zellen das „richtige Gefühl“ und winzige gefäßähnliche Netzwerke gibt, verbessert das dramatisch, wie getreu sie menschliches Gewebe nachbilden – und kann so den Weg von der Grundlagenforschung zu wirksamen Behandlungen beschleunigen.
Zitation: Lu, H., Li, Y., Yang, X. et al. Mechanical forces from intercellular peptide self-assembly drive spheroid formation. Nat Commun 17, 1801 (2026). https://doi.org/10.1038/s41467-026-68513-1
Schlüsselwörter: Gewebeengineering, Krebsmodelle, Angiogenese, Organoide, Peptid-Selbstaggregation