Clear Sky Science · de
Intermittierendes Fasten hemmt Tp53-getriebenes Gliom durch darmmikrobiotika-vermittelte Methionin‑m6A-Regulation
Warum dem Darm eine Pause zu gönnen tödliche Hirntumore verlangsamen könnte
Das Glioblastom ist eine der aggressivsten Hirnkrebsarten, und die aktuellen Behandlungen – Operation, Bestrahlung und Chemotherapie – verschaffen Patientinnen und Patienten häufig nur begrenzt mehr Zeit. Diese Studie stellt eine einfache, aber weitreichende Frage für den Alltag: Kann unsere Art zu essen, konkret intermittierendes Fasten, die Darmbakterien und die Blutchemie so verändern, dass bestimmte Hirntumore deutlich langsamer wachsen?
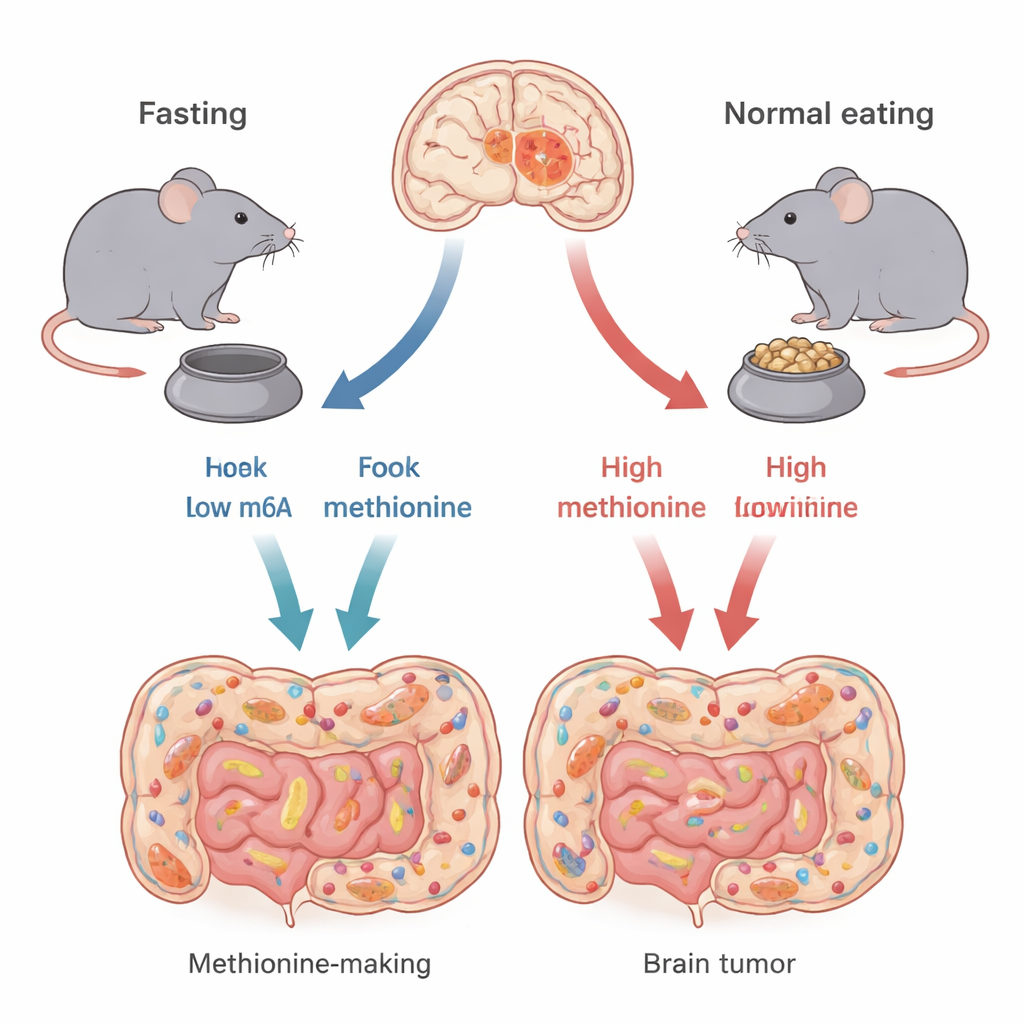
Verschiedene Ausprägungen desselben Hirnkrebses
Nicht alle Glioblastome sind gleich. Die Autorinnen und Autoren konzentrieren sich auf zwei wichtige genetische Typen, definiert durch Veränderungen in den Genen TP53 und CDKN2A. Diese Gene steuern, wie Zellen wachsen oder sterben. An Mausmodellen, die die jeweiligen menschlichen Subtypen gut nachbilden, zeigen die Forschenden, dass intermittierendes Fasten – 24 Stunden ohne Nahrung, gefolgt von 24 Stunden mit Nahrung – nicht allen Tumoren gleich zugutekommt. Mäuse mit TP53-Tumoren lebten länger und hatten kleinere Tumoren unter Fastenbedingungen, während Mäuse mit CDKN2A-Tumoren kaum Vorteile zeigten. Das deutet darauf hin, dass der Nutzen des Fastens stark vom genetischen Aufbau des Tumors abhängen kann.
Vom Essrhythmus über Darmbakterien zur Hirnchemie
Das Team untersuchte dann, wie Fasten seine selektive Wirkung ausübt. Da die Gesamtmenge der Nahrung zwischen den Gruppen gleich blieb, war der entscheidende Unterschied das Timing der Nahrungsaufnahme. Dieses Timing veränderte die Darmmikrobiota – die umfangreiche Gemeinschaft von Bakterien im Darm – deutlich. Bei den fastenden TP53-Mäusen nahmen bestimmte Bakteriengruppen ab, die Methionin besonders effizient produzieren, etwa spezifische Alistipes- und Prevotella-Stämme. Da Methionin ein essenzieller Baustein ist, den Tiere über die Nahrung oder Darmmikroben erhalten müssen, führte diese mikrobielle Verschiebung zu weniger Methionin, das vom Darm ins Blut und letztlich ins Gehirn gelangte.
Wie ein einzelner Nährstoff krebstreibende Signale abstimmt
Methionin ist nicht nur Nährstoff; es ist auch Rohstoff für S‑adenosylmethionin (SAM), den universellen „Methylspender“ der Zelle. SAM speist eine chemische Markierung von RNA namens m6A. Diese Markierungen beeinflussen, wie stark bestimmte Gene exprimiert werden. Im TP53-Tumormodell senkte Fasten Methionin‑ und SAM-Spiegel im Blut und in Hirntumorregionen. Mit mehreren Ebenen von Omics-Technologien – standardisierte RNA-Sequenzierung, Einzelzell-RNA-Profile und räumliche Karten von Genaktivität und Metaboliten – fanden die Forschenden bei Fasten weniger m6A-Markierungen auf wichtigen krebsassoziierten RNAs. Ein bedeutendes Ziel war TGFB2, ein Gen der TGF‑β-Signalwegkomponente, die bekannt dafür ist, Tumorwachstum und Invasion zu fördern. Unter Fasten waren das Enzym METTL3 (das m6A schreibt) und TGFB2 herunterreguliert, und die TGF‑β-Signalübertragung schwächte sich ab.
Ursache und Wirkung mit gezielten Interventionen nachweisen
Um über Korrelation hinauszukommen, führten die Wissenschaftlerinnen und Wissenschaftler „Rescue“-Experimente durch. Sie blockierten METTL3 mit einem Wirkstoff oder übertrugen Darmbakterien von fastenden Mäusen auf normal gefütterte Mäuse und beobachteten ein verlangsamtes Tumorwachstum auch ohne Fasten – ein Hinweis darauf, dass sowohl die Mikrobiota als auch die m6A-Maschinerie zentrale Rollen spielen. Umgekehrt wuchsen Tumoren von fastenden Mäusen mehr wie die von normal gefütterten Tieren, wenn zusätzlich Methionin verabreicht oder ein Wirkstoff eingesetzt wurde, der m6A-Markierungen erhöht; der Überlebensvorteil verschwand. Wichtig ist, dass eine Störung der Darmbakterien durch breit wirkende Antibiotika viele der fastenbedingten Veränderungen auslöschte, was unterstreicht, dass die Darmgemeinschaft ein zentrales Glied in dieser Kettenreaktion ist.
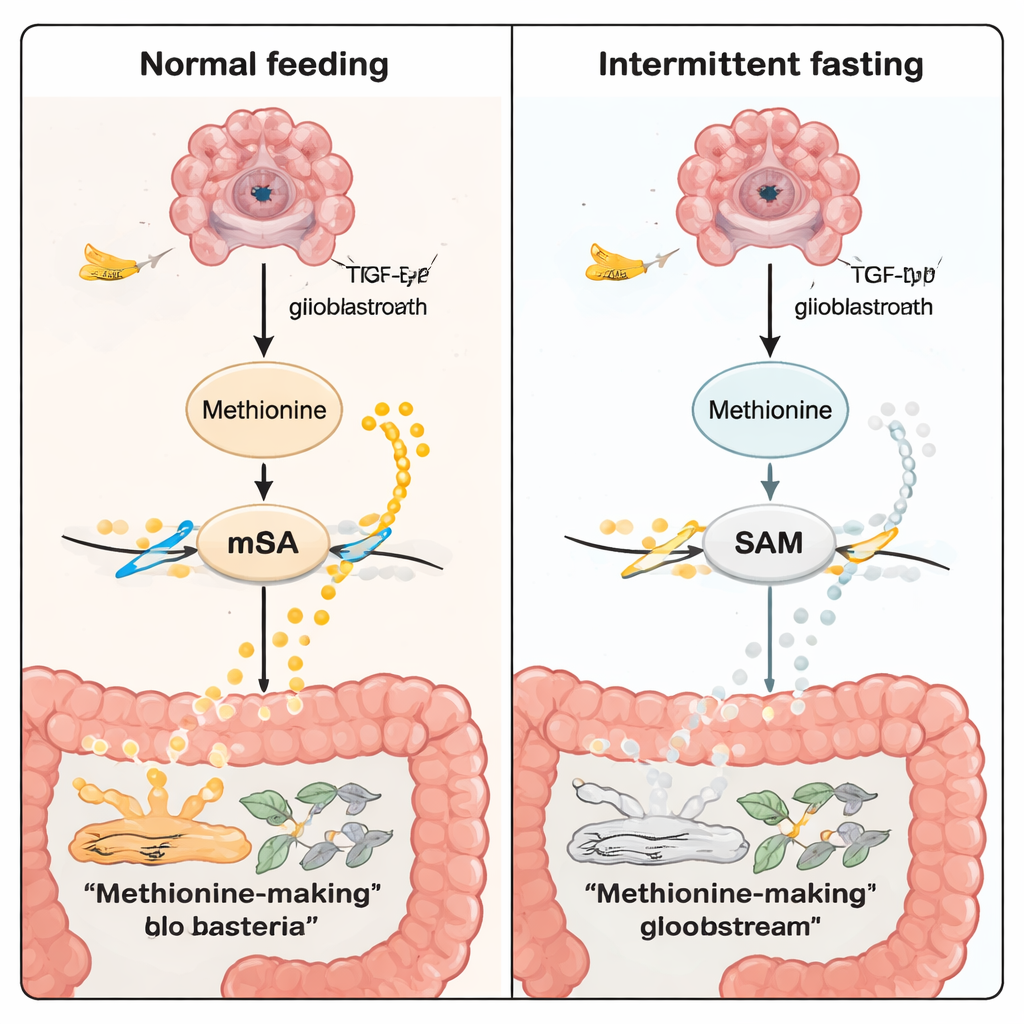
Was das für Menschen und künftige Therapien bedeutet
Für Laien lautet die Kernbotschaft: Nicht alle Krebserkrankungen – und nicht einmal alle Glioblastome – reagieren gleich auf eine Ernährungsstrategie wie intermittierendes Fasten. Bei TP53‑Typ-Gliomen scheint Fasten über den Darm mit dem Gehirn zu „kommunizieren“: Es verändert die Darmbakterien, was wiederum die Methioninproduktion senkt, die chemische Markierung der RNA reduziert und starke Wachstumssignale in Tumorzellen abschwächt. Obwohl diese Arbeit an Mäusen durchgeführt wurde und eine sorgfältige klinische Übersetzung erfordert, weist sie in die Richtung, dass einfache Lebensstilmuster, mikrobielle Therapien und Medikamente, die Methionin- oder m6A‑Wege ansprechen, künftig an die genetische Subtypisierung des Tumors angepasst werden könnten.
Zitation: Lin, Y., Li, S., Xu, X. et al. Intermittent fasting inhibits Tp53-driven glioma through gut microbiota-mediated methionine-m6A regulation. Nat Commun 17, 1804 (2026). https://doi.org/10.1038/s41467-026-68512-2
Schlüsselwörter: intermittierendes Fasten, Glioblastom, Darmmikrobiom, Methioninstoffwechsel, RNA-m6A-Modifikation