Clear Sky Science · de
Simultane Oxidation von Sulfid und Reduktion von Sulfat zur intrazellulären Redox-Homeostase unter stark sauren Bedingungen
Warum zur Reinigung giftiger Gase clevere Mikroben nötig sind
Viele Industrien setzen Schwefelwasserstoff frei, ein giftiges, nach faulen Eiern riechendes Gas, das Anlagen korrodieren, die Luft belasten und Menschen schädigen kann. Um es zu entfernen, greifen Ingenieure zunehmend auf Mikroben zurück, die Sulfid in sicherere Schwefelverbindungen umwandeln. Diese Studie enthüllt eine unerwartete mikrobiologische Strategie: Ein neu identifiziertes Mycobacterium betreibt gleichzeitig zwei normalerweise gegensätzliche chemische Wege, um Sulfid schnell zu entgiften und sich selbst vor inneren Schäden zu schützen — selbst unter extrem sauren Bedingungen.
Ein Tauziehen im Schwefelkreislauf
Im natürlichen Schwefelkreislauf wirken zwei entgegengesetzte Reaktionen. Einige Mikroben oxidieren Sulfid (die am stärksten reduzierte, toxische Form) zu weniger schädlichen Produkten wie elementarem Schwefel oder Sulfat und gewinnen dabei Energie. Andere gehen den umgekehrten Weg und reduzieren Sulfat zurück zu Sulfid, um essenzielle Zellbestandteile wie schwefelhaltige Aminosäuren aufzubauen. Weil diese Reaktionen einander rückgängig machen, nahm man lange an, dass eine einzelne Zelle sie nicht gleichzeitig ablaufen lässt; das wäre verschwenderisch, wie Heizen und Kühlen eines Hauses mit offenen Fenstern. 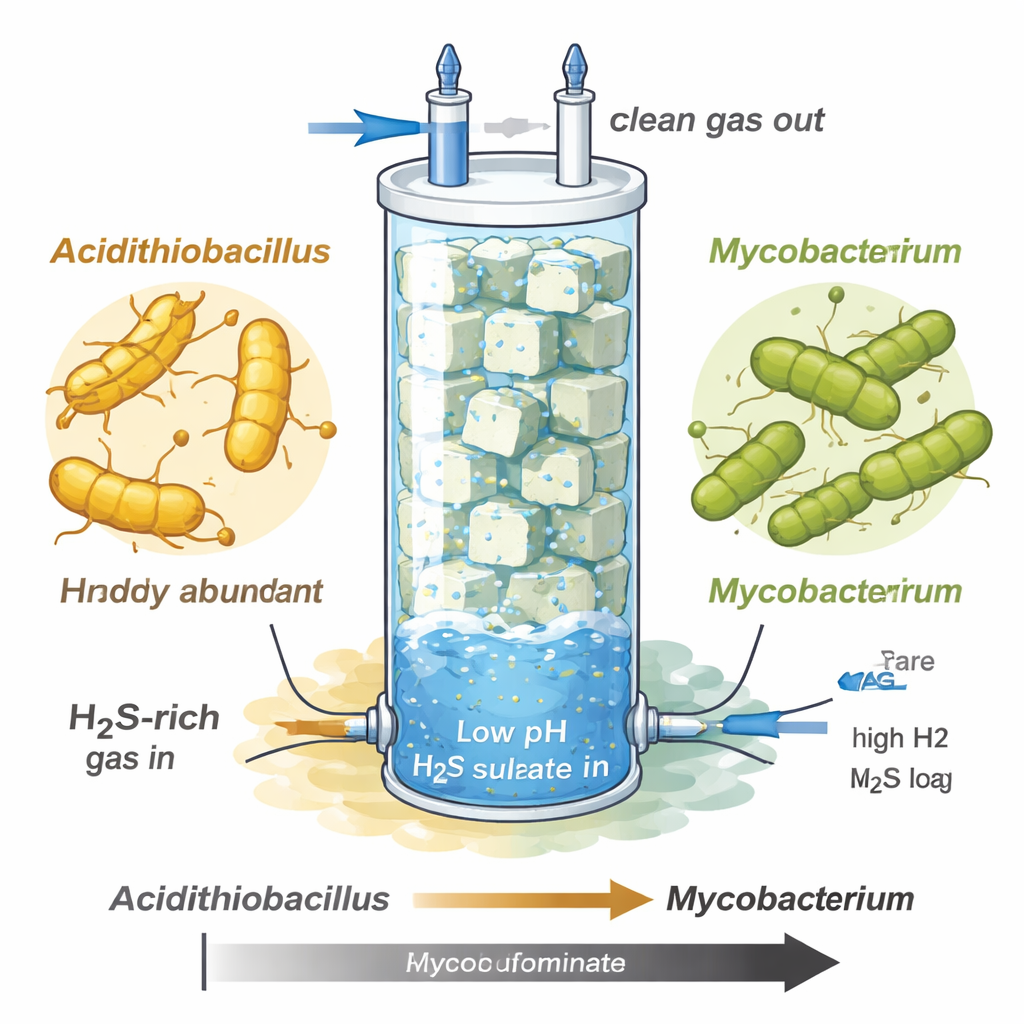
Einen Überlebenskünstler in einem Extremreaktor finden
Die Forscher untersuchten einen Biotrickling-Filter — eine hohe Glas-Säule, gefüllt mit Schaumstoffwürfeln —, der so ausgelegt ist, Schwefelwasserstoff aus Gasströmen ähnlich Rohbiogas oder Erdgas zu entfernen. Als sie die Sulfidbelastung erhöhten und das System sehr sauer hielten (pH etwa 1–1,5), veränderte sich die mikrobielle Gemeinschaft drastisch. Zunächst dominierte ein bekannter Sulfid-Oxidierer, Acidithiobacillus, und wandelte einen Großteil des Sulfids in Sulfat um, brach aber später unter der extremen Sulfidbelastung zusammen. An seine Stelle trat eine zuvor uncharakterisierte Mycobacterium-Art, bezeichnet als MAG-M116, die nahezu die gesamte Gemeinschaft übernahm, obwohl sie in der frühen, milderen Phase langsamer wuchs.
Ein Mikroorganismus, der die üblichen Regeln bricht
Genetische und Protein-Analysen zeigten, dass MAG-M116 einen ungewöhnlichen Stoffwechsel besitzt. Sie trägt das Schlüsselenzym Sulfid:Quinon-Oxidoreduktase, das Sulfid nur bis zu festem elementarem Schwefel oxidiert, das als winzige Partikel akkumuliert. Gleichzeitig verfügt das Mikroorganismus über einen kompletten Satz von Genen für die assimilative Sulfatreduktion, den Weg, der Sulfat in die Zelle aufnimmt und reduziert, um Aminosäuren wie Cystein und Methionin aufzubauen. Unter hohen Sulfidbedingungen waren beide Wege gleichzeitig aktiviert. Die Sulfidoxidation speiste Elektronen in die Energie-Maschinerie der Zelle, während die Sulfatreduktion einen Teil dieses Elektronenflusses aufnahm und so die beiden Richtungen des Schwefelkreislaufs in einer einzelnen Zelle verband.
Aus einem „verschwenderischen“ Zyklus ein Sicherheitsventil machen
Das gleichzeitige Betreiben beider Wege könnte theoretisch sinnlos erscheinen — Energie verbrennen ohne Nettogewinn. Das Team zeigt jedoch, dass es für MAG-M116 als Sicherheitsventil für überschüssige Elektronen dient. Die Oxidation großer Sulfidmengen setzt einen Elektronenschub in die respiratorische Kette der Zelle frei, der auslaufen und reaktive Sauerstoffspezies (ROS) erzeugen kann — schädliche Moleküle, die DNA, Proteine und Membranen angreifen. Durch die aktive Reduktion von Sulfat zu Aminosäuren lenkt die Zelle 10–14 % dieser Elektronen in konstruktive Arbeit um und verringert so die Ansammlung eines überreduzierten, auslaufgefährdeten Zustands. Experimente unter Bedingungen mit und ohne Sulfat zeigten, dass aktive Sulfatreduktion die ROS-Produktion um bis zu etwa 60 % senkte und die Anhäufung reduzierter Cofaktoren verhinderte, die sonst oxidative Schäden antreiben würden. 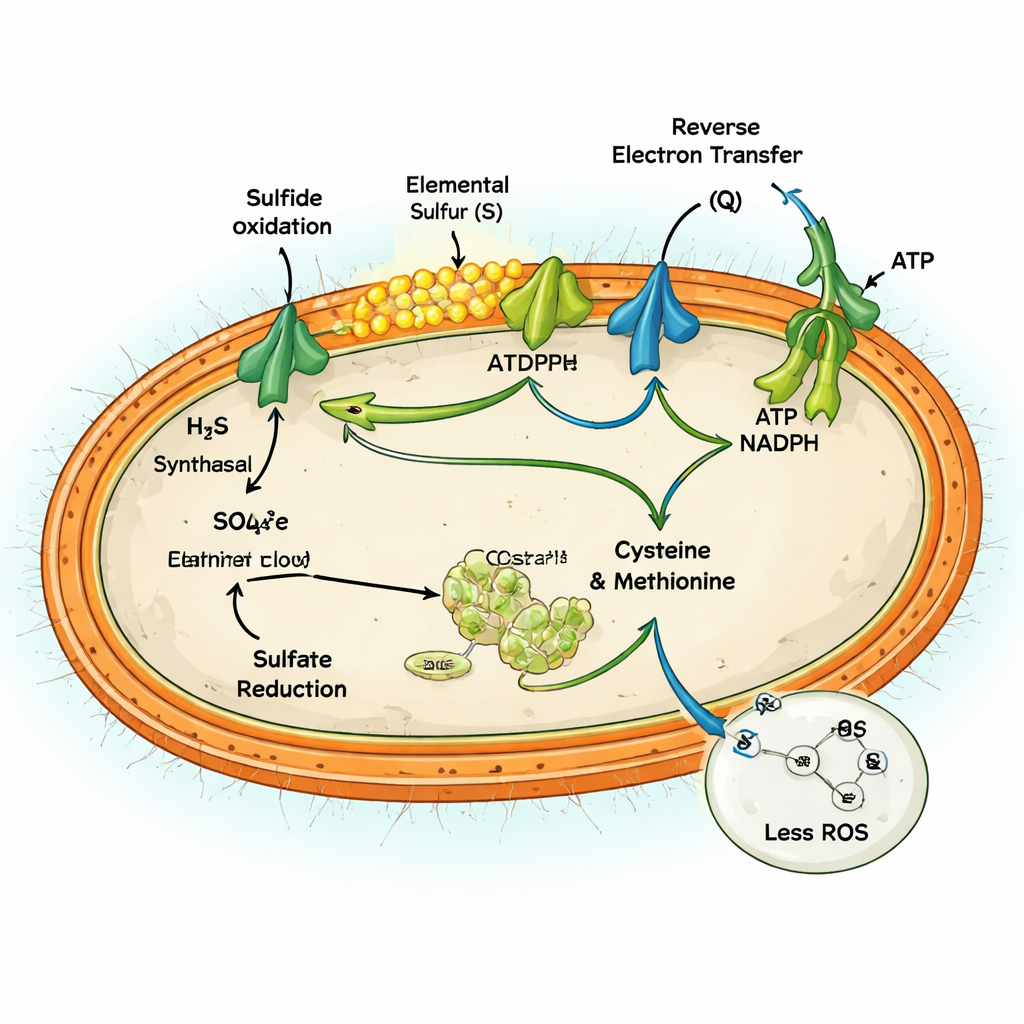
Vom giftigen Gas zu nützlichen Produkten
In den späteren Betriebsphasen des Reaktors, als MAG-M116 dominierte, wurde nahezu der gesamte zugeführte Schwefelwasserstoff in festen elementaren Schwefel umgewandelt und nicht in Sulfat. Gleichzeitig detektierten die Forscher steigende Konzentrationen von Cystein und Methionin in der Flüssigphase, was darauf hindeutet, dass das Mikroorganismus überschüssige schwefelreiche Aminosäuren in seine Umgebung freisetzte. Diese Kombination — stabiler elementarer Schwefel plus wertvolle organische Schwefelverbindungen — verwandelt einen einst gefährlichen Schadstoff in ein Gemisch rückgewinnbarer Produkte mit Anwendungen in Landwirtschaft, Werkstoffen und Energiesystemen.
Was das für Gesundheit und Technik bedeutet
Für Nichtfachleute lautet die Kernbotschaft: Dieses Mycobacterium hat ein doppeltes Problem gelöst — es kann hohe Konzentrationen eines giftigen Gases entfernen und gleichzeitig seine eigene innere Chemie im Gleichgewicht halten. Es tut dies, indem es „Schub–Zug“-Schwefelreaktionen simultan betreibt, die normalerweise getrennt bleiben, und den vermeintlich verschwendeten Zyklus als eingebautes Stoßdämpfer für überschüssige Elektronen und schädliche Sauerstoffradikale nutzt. Diese Entdeckung deutet nicht nur auf neue Wege zur Gestaltung robuster, niedrig-pH-Bioreaktoren für die Sulfid- und Sulfatentfernung hin, sondern legt auch nahe, dass verwandte Mikroben, einschließlich krankheitsverursachender Mycobacterium-Arten, ähnliche Tricks nutzen könnten, um oxidativen Angriffen im menschlichen Körper zu entgehen.
Zitation: Jia, T., Peng, Y., Niu, L. et al. Simultaneous sulfide oxidation and sulfate reduction for intracellular redox homeostasis under highly acidic conditions. Nat Commun 17, 1797 (2026). https://doi.org/10.1038/s41467-026-68508-y
Schlüsselwörter: Schwefelzyklus, Schwefelwasserstoff, Mycobacterium, Redox-Homeostase, Biodesulfurisierung