Clear Sky Science · de
Eine künstliche Zelle, die durch ADRB2 vermittelte Signalübertragung zur Regulierung der Glykogenolyse ermöglicht
Kleinen Bläschen das Sprechen beibringen
Stellen Sie sich eine mikroskopische Seifenblase vor, die ein hormonähnliches Signal von außen wahrnehmen und dann „entscheiden“ kann, gespeicherte Energie von innen zu verbrennen – ähnlich wie eine echte menschliche Zelle. Diese Studie baut genau eine solche künstliche Zelle und zeigt, wie menschengemachte Zellnachbildungen eine chemische Nachricht empfangen und in kontrollierte, energiebezogene Chemie umwandeln können. Solche Arbeiten rücken uns näher an smarte Wirkstoffträger, im Labor hergestellte Gewebe und einfache synthetische Lebensformen, die auf ihre Umgebung reagieren können.
Eine Zelle von außen nach innen aufbauen
Echte Zellen hören ständig mit Rezeptoren in ihrer äußeren Membran auf die Umgebung. Die Autoren wollten einen dieser natürlichen Signalwege nur mit gereinigten Komponenten und einfachen Fettbläschen, sogenannten Giant Vesicles, nachbauen. Im Fokus stand ein häufiger menschlicher Rezeptor, der β2‑Adrenerge Rezeptor (ADRB2), der in unserem Körper Herzfrequenz, Lungenfunktion und Energieverwendung mitsteuert. Treffen solche Rezeptoren auf einen Wirkstoff wie Isoproterenol (ISO), löst das normalerweise eine innere Kaskade aus, die das Botenmolekül cAMP erzeugt, das wiederum steuert, wie Zellen Glykogen, die gespeicherte Form von Glukose, abbauen. Diese gesamte Sequenz in einer künstlichen Zelle zu reproduzieren, war bislang nicht erreicht worden.
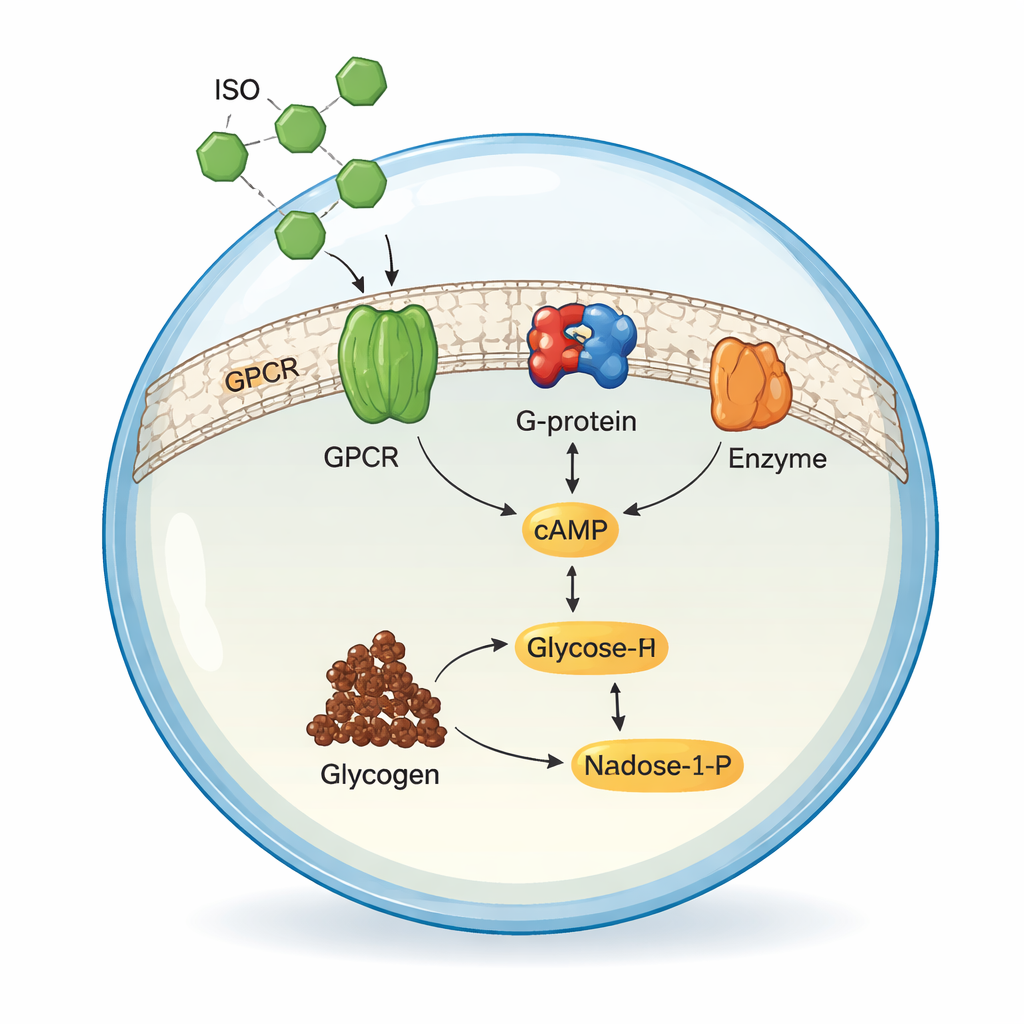
Die erste Signalkette nachbauen
Das Team rekonstruierte zunächst die frühen Stufen des Signalwegs in Lösung, also außerhalb jeder Membran. Sie stellten drei menschliche Proteine in Insektenzellen her: ADRB2, seine Partner‑G‑Protein‑Untereinheit (Gsα) und ein Enzym namens Adenylatcyclase V (ADCY5), das aus ATP cAMP erzeugt. Mischten sie diese Bausteine mit ISO unter sorgfältig abgestimmten Bedingungen, führte die Aktivierung des adrenergen Rezeptors dazu, dass ADCY5 ATP in cAMP umwandelte. Durch Messung von cAMP mittels Hochleistungsflüssigkeitschromatographie optimierten die Forscher pH‑Wert, Temperatur und Magnesiumkonzentration und fanden, dass ihr rekonstruiertes System so effizient oder effizienter arbeitete als viele frühere Präparate, was bestätigte, dass die Kernchemie der Signalübertragung funktionierte.
Echte Rezeptoren in künstlichen Membranen installieren
Als Nächstes betteten die Autoren die drei Proteine in die Membranen von Giant Unilamellaren Vesikeln ein—zellgroßen Lipidbläschen, die als Chassis für künstliche Zellen dienen. Sie markierten ADRB2 und ADCY5 fluoreszent, um zu verifizieren, dass die Proteine in der Membran saßen, sich frei bewegten und in großer Zahl vorhanden waren, mit ungefähr 1,8 Millionen Rezeptoren pro Vesikel. Enzymatische Tests zeigten, dass mehr als 94 % dieser Rezeptoren korrekt orientiert waren, mit ihren Bindungsstellen nach außen gerichtet. Eine fluoreszente GTP‑Sonde bestätigte, dass ISO‑Bindung an der Membran tatsächlich G‑Proteine im Inneren der Vesikel aktivierte. Das bedeutete, dass die künstlichen Zellen prinzipiell ein externes ISO‑Signal über ihre Membran übertragen konnten, so wie natürliche Zellen es tun.
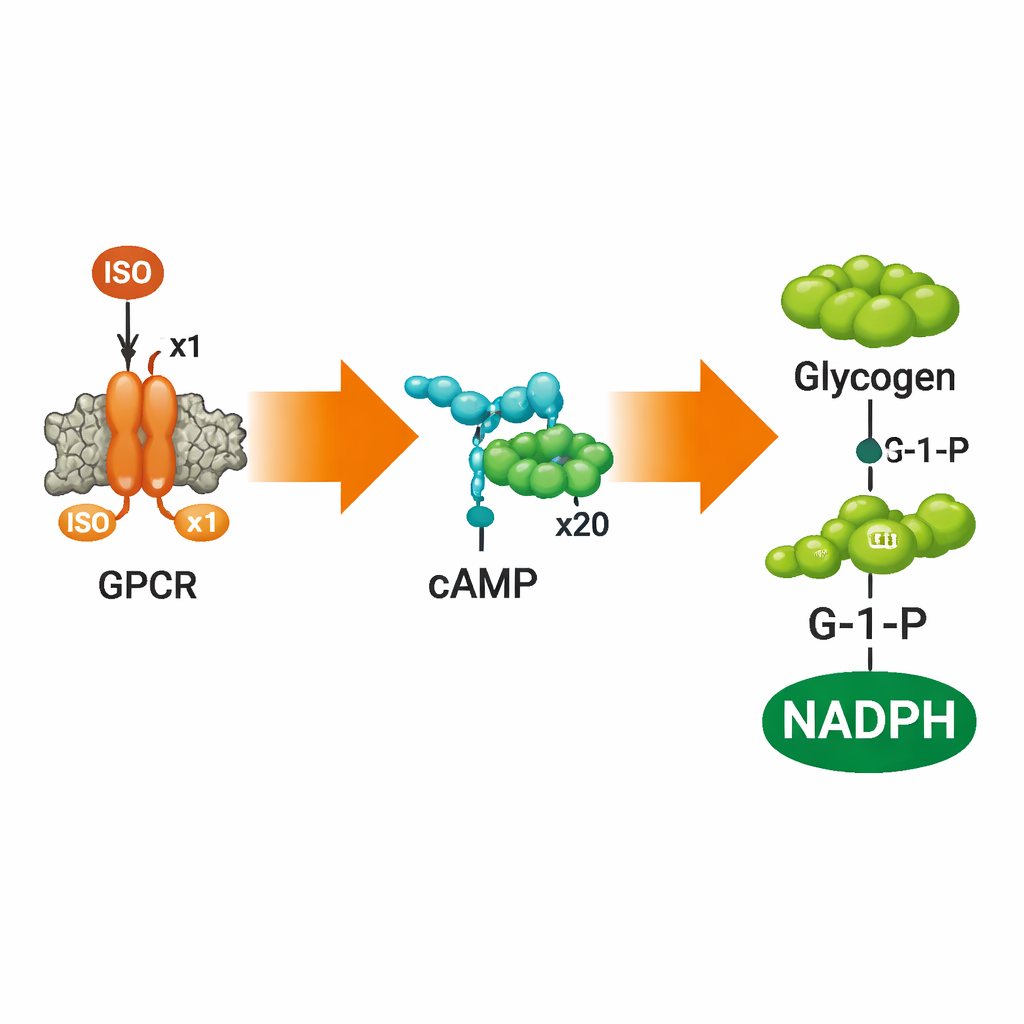
Signale in Brennstoffabbau umwandeln
Um zu prüfen, ob diese synthetischen Zellen mit dem Signal etwas Nützliches anstellen konnten, ergänzte das Team einen Sensor für cAMP und anschließend einen vollständigen Glykogenabbauweg im Inneren der Vesikel. Mithilfe einer FRET‑basierten cAMP‑Sonde zeigten sie, dass das Hinzufügen von ISO außerhalb der Vesikel zu einem dosisabhängigen Anstieg von cAMP im Inneren führte, der dann abflachte, als die Rezeptoren gesättigt waren—ein Verhalten, das klassische GPCR‑Reaktionen natürlicher Zellen widerspiegelt. Wirkstoffe, die ADRB2 blockieren oder stummschalten—Alprenolol und Carazolol—schalteten diese Reaktion erwartungsgemäß aus. Wenn die Autoren zusätzlich fünf Enzyme einschlossen, die normalerweise Glykogen in Glukose‑1‑phosphat (G‑1‑P) und dann in NADPH umwandeln, führte ISO‑Stimulation zu messbarer Produktion von sowohl G‑1‑P als auch NADPH innerhalb der künstlichen Zellen, nachgewiesen durch Massenspektrometrie, Chromatographie und Fluoreszenz.
Ein Flüstern in einen Schrei verstärken
Ein zentrales Ergebnis ist die starke Verstärkung der internen Antwort. Eine moderate Menge ISO außerhalb der Vesikel erzeugte etwa 22‑mal mehr cAMP‑Moleküle, als ISO‑Moleküle vorhanden waren, und diese Verstärkung nahm weiter im nachgeschalteten Weg zu. Bis das Signal den Glykogenabbau angestoßen und die Umwandlung in 6‑Phosphogluconolacton mit begleitendem NADPH bewirkt hatte, überstieg die Gesamtverstärkung den hundertfachen Wert. Diese stufenweise Verstärkung ist ein Kennzeichen natürlicher Hormon‑Signalübertragung und zeigt, dass das künstliche System mehr leistet als nur die Detektion von ISO—es verarbeitet und verstärkt die Nachricht zu einem robusten metabolischen Output.
Warum das für zukünftiges synthetisches Leben wichtig ist
Für Nicht‑Spezialisten lassen sich die technischen Details auf eine einfache Idee reduzieren: Die Forscher haben einer minimalen, menschengemachten Zelle beigebracht, wie eine lebende Zelle zuzuhören und zu reagieren. Ein äußeres Wirkstoffmolekül dockt an einen realistischen menschlichen Rezeptor, ein Signal wird über eine synthetische Membran weitergegeben und ein internes Enzymnetzwerk reagiert, indem es gespeicherte chemische Energie mobilisiert. Zu demonstrieren, dass diese gesamte Kette—von der Rezeptoraktivierung bis zur gesteuerten Metabolismusantwort—in einem reduzierten künstlichen System funktioniert, ist ein bedeutender Schritt hin zu autonomen synthetischen Zellen, die erkennen, entscheiden und nützlich handeln können, etwa ihre eigene Energieversorgung anpassen oder Therapien nur dann freisetzen, wenn sie die richtigen chemischen Signale wahrnehmen.
Zitation: Liu, Y., Zhao, W., Zhao, Y. et al. An artificial cell capable of signal transduction mediated by ADRB2 for the regulation of glycogenolysis. Nat Commun 17, 1795 (2026). https://doi.org/10.1038/s41467-026-68503-3
Schlüsselwörter: künstliche Zellen, Signalübertragung, GPCR, Glykogenolyse, synthetische Biologie