Clear Sky Science · de
Räumlich-zeitlich gesteuerte Wirkstofffreisetzung über ein Click-Release-System basierend auf Monoalkylhydroxylamin- und Cyclooctyn-Chemie
Starke Medikamente nur dort aktivieren, wo sie gebraucht werden
Viele moderne Medikamente sind extrem wirksam, was beim Kampf gegen Krebs oder zur Schmerzbekämpfung vorteilhaft ist — aber für den Rest des Körpers ein Risiko darstellt. Diese Studie beschreibt einen chemiebasierten "Ein-/Aus-Schalter", mit dem Forscher Wirkstoffe in einer inaktiven, harmlosen Form parken und sie dann nur an einem gewählten Ort und Zeitpunkt aktivieren können, etwa innerhalb eines Tumors oder in einem kleinen Bereich, der lokale Anästhesie benötigt.
Eine neue Art chemischen Schalters
Die Forscher bauen auf dem Konzept der „Click-Chemie“ auf, einer Reaktionsklasse, die geschätzt wird, weil sie schnell, präzise und sicher in lebenden Systemen ablaufen kann. Klassische Click-Reaktionen verbinden zwei Moleküle dauerhaft miteinander. Hier kehrt das Team diese Logik um: ihre Click-Reaktion ist direkt mit dem Aufbrechen einer Bindung und der Freisetzung eines Wirk- oder Signalmoleküls verknüpft. Die Schlüsselkomponenten sind ein ringförmiges Molekül namens Cyclooctyn und ein kleiner Partner, das Monoalkylhydroxylamin. Treffen diese beiden aufeinander, koppeln sie sich schnell und ordnen sich so um, dass eine angekoppelte „Nutzlast“ abgespalten wird. Durch das Anfügen verschiedener Wirkstoffe oder Fluoreszenzfarbstoffe als Nutzlast lässt sich dieselbe Grundreaktion für viele Zwecke nutzen. 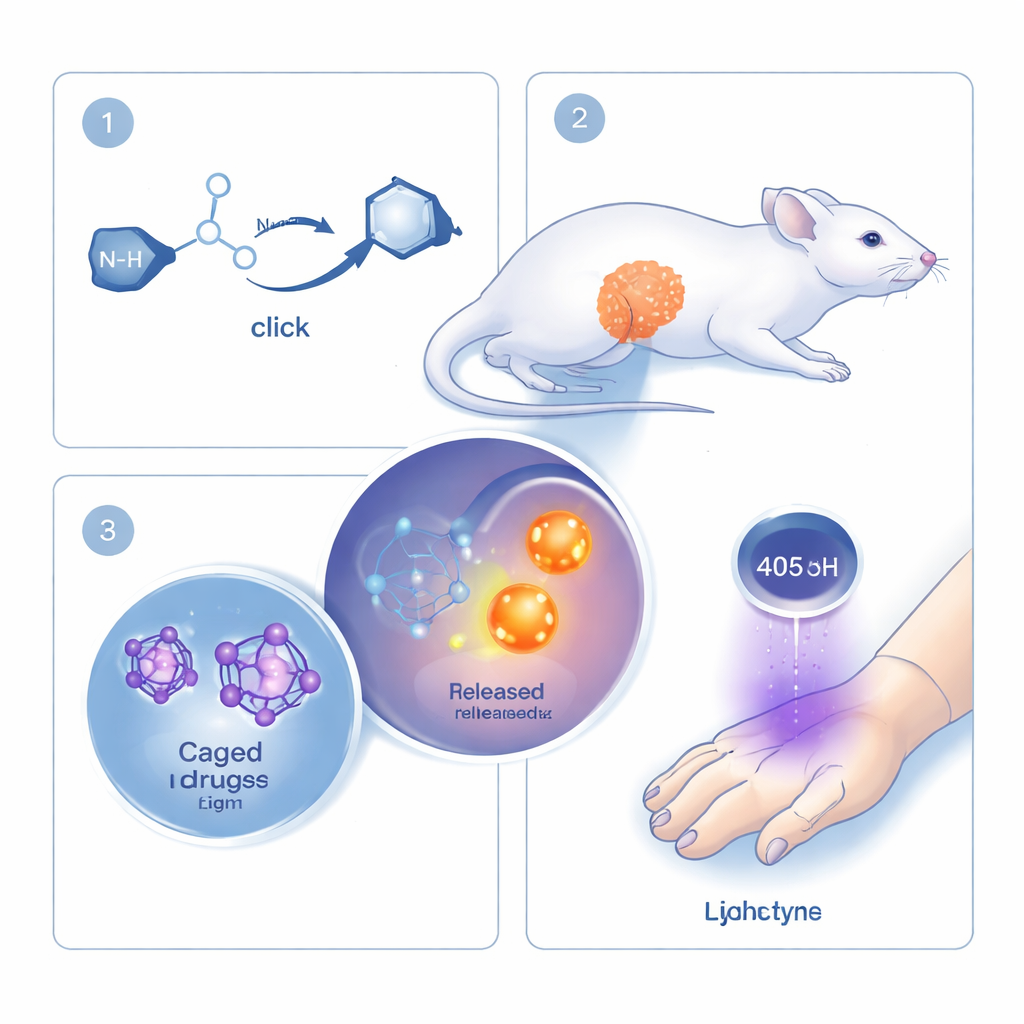
Schnelle, saubere Freisetzung innerhalb und außerhalb von Zellen
Um die Praxistauglichkeit des Schalters zu prüfen, bestimmten die Autoren, wie schnell die Reaktion abläuft und wie vollständig sie die gebundene Nutzlast freisetzt. Sie fanden heraus, dass sorgfältig ausgewählte Monoalkylhydroxylamine deutlich schneller reagieren als einfaches Hydroxylamin und je nach Struktur innerhalb von Minuten bis Stunden nahezu vollständige Umsetzung erreichen. Wichtig ist, dass die chemischen Schritte, die die Nutzlast tatsächlich freisetzen, so schnell und selektiv sind, dass fast das gesamte angekoppelte Molekül freigesetzt wird und nur sehr wenige Nebenprodukte entstehen. Die Autoren testeten eine Reihe von Ladungen, darunter Fluoreszenzfarbstoffe und sogar ein Fluoridion, und zeigten, dass das System mehrere in der Wirkstoffentwicklung übliche Bindungstypen spalten kann, etwa Carbamate und Ether.
Zellen zum Leuchten bringen und Krebsmedikamente bei Bedarf aktivieren
Als Nächstes gingen die Forscher zu lebenden Zellen über. Zuerst verblendeten sie leuchtstarke Fluoreszenzfarbstoffe mit dem chemischen Schalter und gaben diese „gecagten" Sonden an Krebszellen. Von allein blieben die Sonden dunkel, was zeigte, dass die Zellen sie nicht versehentlich aktivierten. Als der Monoalkylhydroxylamin-Partner zugegeben wurde, wurden die Farbstoffe freigesetzt und die Zellen leuchteten in Blau-, Grün- oder nahinfraroten Farben — ein Beleg dafür, dass die Reaktion verlässlich in einer biologischen Umgebung funktioniert. Anschließend wandten sie dasselbe Prinzip auf Doxorubicin an, ein weit verbreitetes Chemotherapeutikum. In seiner gecagten Form war das Doxorubicin-Prodrug deutlich weniger zelltoxisch. Lag jedoch der Click-Partner vor, wurde das aktive Medikament effizient freigesetzt und stellte seine Fähigkeit zur Abtötung von Krebszellen nahezu so stark wieder her wie freies Doxorubicin.
Intelligente Auslöser für Ort und Zeit konstruieren
Eine Einschränkung vieler bestehender Click-basierter Systeme ist, dass die reaktiven Komponenten ständig „an“ sind, wodurch sich schwer kontrollieren lässt, wo und wann sie zünden. Um das zu lösen, blockierte das Team vorübergehend die Reaktivität des Monoalkylhydroxylamins mit kleinen Schutzkappen, die nur von spezifischen Auslösern entfernt werden. Sie erzeugten Varianten, die auf hohe Glutathionspiegel (ein in vielen Tumoren reichlich vorhandenes kleines Molekül), auf Enzyme und auf violettes Licht ansprechen. In Zellen und in tumorbefallenen Mäusen blieb die glutathion-reaktive Version unter normalen Bedingungen stumm, schaltete sich aber in der chemisch reduzierenden Umgebung des Tumors ein und setzte dort Fluoreszenzfarbstoffe frei oder aktivierte das Doxorubicin-Prodrug genau an der Stelle, an der der Krebs wuchs. Mäuse, die mit der Kombination aus Prodrug plus Auslöser behandelt wurden, zeigten stärkeren Tumorrückgang als solche, die Standard-Doxorubicin erhielten, während die Belastung empfindlicher Organe wie des Herzens geringer war.
Per Fernsteuerung lokale Anästhesie mit Licht
Um die zeitliche Steuerung zu demonstrieren, entwarfen die Autoren eine zweite Anwendung: lichtgeführte lokale Anästhesie. Sie banden das schmerzlindernde Mittel Tetracain an ihr Cyclooctyn-Gerüst und machten es so inaktiv, und mischten dieses Prodrug mit einer lichtempfindlichen Version des Hydroxylamins in einem temperaturreaktiven Gel. In eine Rattenpfote injiziert, zeigte das Gemisch keine Wirkung, bis die Haut mit 405-Nanometer-Licht beleuchtet wurde. Die Beleuchtung löste die Click-Release-Reaktion aus, setzte Tetracain frei und erzeugte eine Taubheit, die mit einer direkten Tetracain-Injektion vergleichbar war. Durch Variation der Dauer und Intensität der Beleuchtung konnten die Forscher die Dauer der Nervenblockade einstellen, und sie waren sogar in der Lage, wiederholte Wellen von Anästhesie aus einer einzigen Injektion zu triggern. 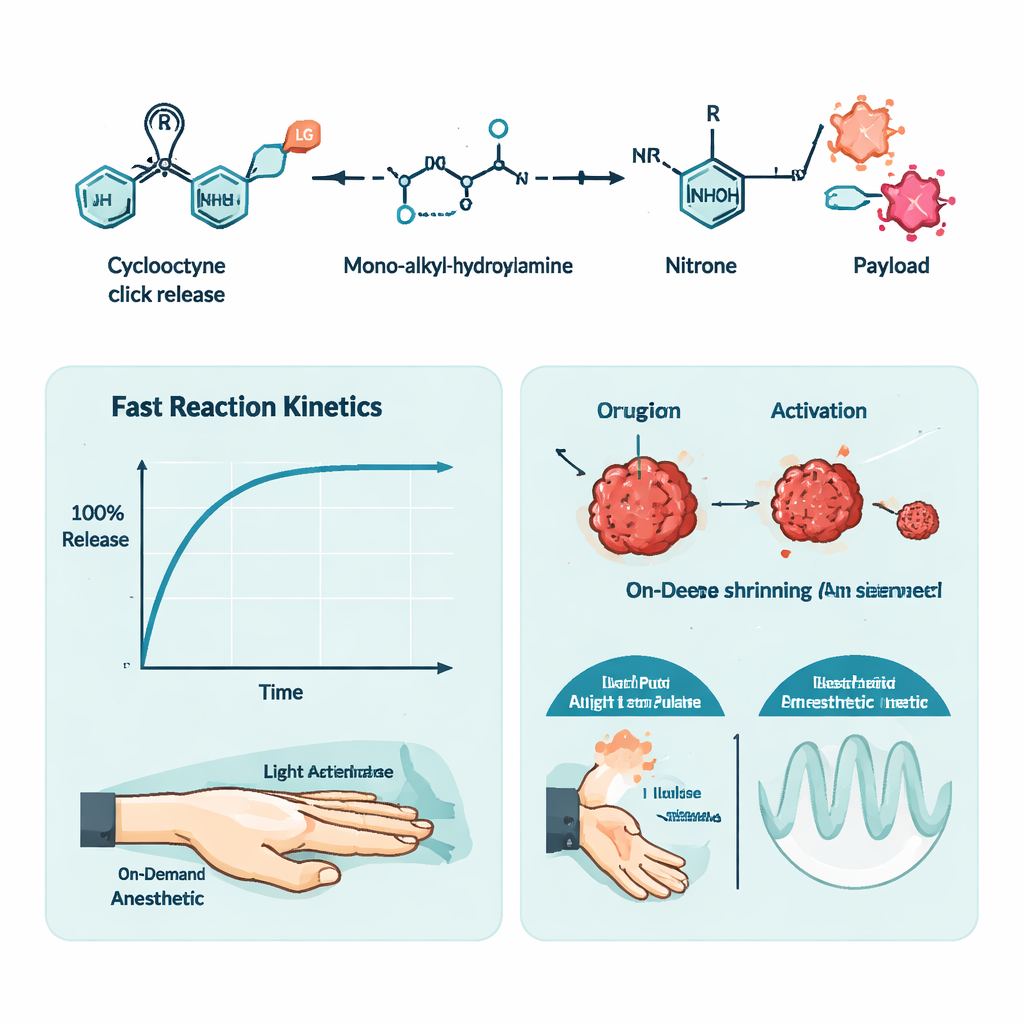
Was das für zukünftige Behandlungen bedeuten könnte
Für Nicht-Spezialisten ist die Kernbotschaft, dass diese Arbeit eine flexible chemische Fernsteuerung für Medikamente bietet: Wirkstoffe können in einer sicheren, ruhigen Form verabreicht und dann nur am richtigen Ort und zur richtigen Zeit aktiviert werden, unter Verwendung von Signalen, die entweder aus dem Körper selbst stammen oder von einer externen Lichtquelle kommen. Obwohl vor einer klinischen Anwendung noch weitere Tests nötig sind, könnte der Ansatz langfristig Krebsbehandlungen gezielter und weniger toxisch machen, individuell anpassbare Schmerzbehandlung nach Operationen ermöglichen und eine Reihe anderer Therapien unterstützen, die von präziser räumlich-zeitlicher Kontrolle profitieren.
Zitation: Xu, X., Tong, X., Shi, Y. et al. Spatiotemporally controlled drug release via a click-release system utilizing mono-alkyl-hydroxylamine and cyclooctyne chemistry. Nat Commun 17, 1794 (2026). https://doi.org/10.1038/s41467-026-68502-4
Schlüsselwörter: Click-Chemie, zielgerichtete Wirkstoffabgabe, Prodrugs, Tumormikroumgebung, lichtgesteuerte Anästhesie