Clear Sky Science · de
Selektive Elektrosynthese von Harnstoff aus Nitrat und Kohlendioxid bei niedriger Überspannung
Aus Abfall Dünger machen
Die moderne Landwirtschaft ist stark auf Harnstoffdünger angewiesen, doch die herkömmliche Herstellung verbraucht große Mengen fossiler Brennstoffe und setzt viel Kohlendioxid frei. Diese Studie untersucht einen saubereren Weg: mit Strom und speziell entworfenen Materialien Kohlendioxid und Nitrat – beide häufige Schadstoffe – direkt unter milden Bedingungen zu Harnstoff umzuwandeln. Bei Skalierung könnte ein solcher Prozess helfen, Menschen zu ernähren, gleichzeitig Treibhausgasemissionen zu reduzieren und Abwasser- bzw. Abfallströme besser zu nutzen.
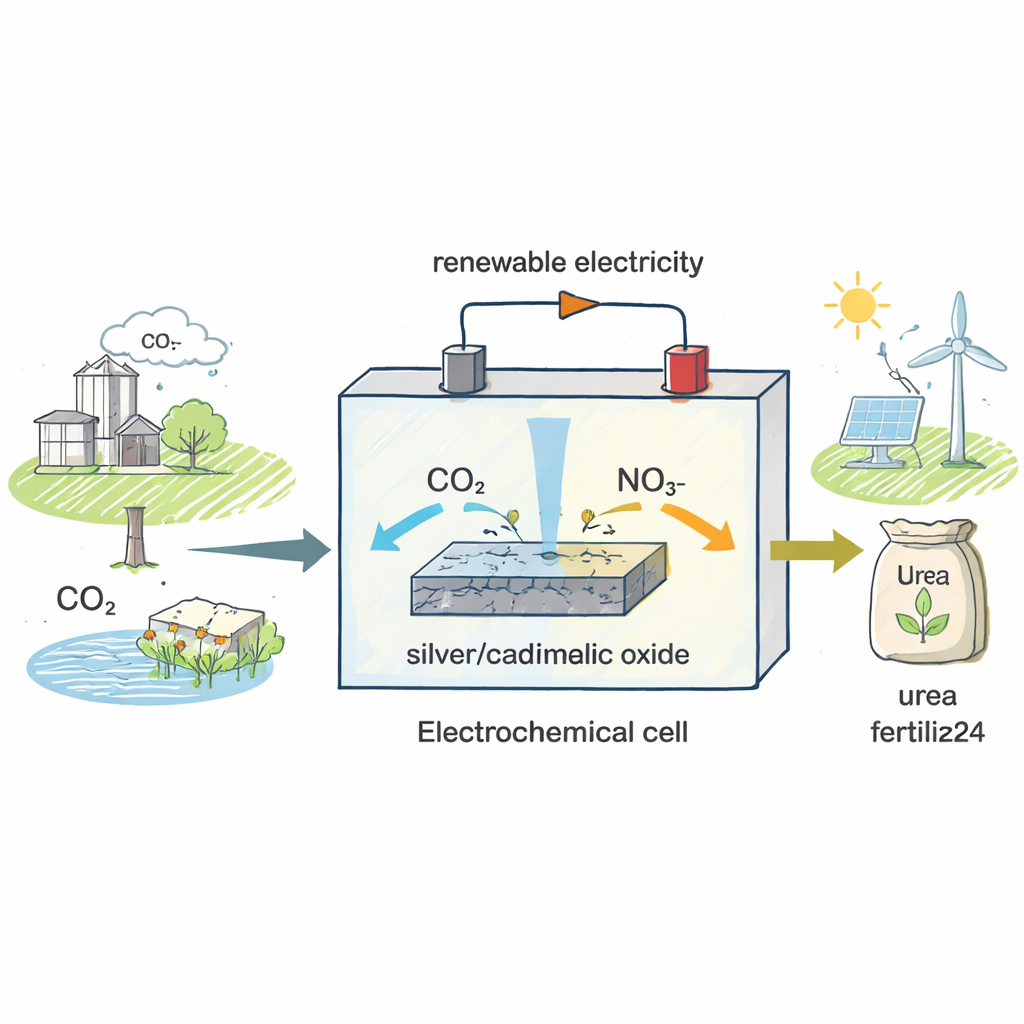
Ein neuer Weg, um einen alten Dünger herzustellen
Die heutigen Harnstofffabriken arbeiten bei hohen Temperaturen und Drücken und basieren darauf, dass zunächst Ammoniak aus Stickstoffgas hergestellt wird – ein Schritt, der alleine mehr als 2 % des globalen Energiebedarfs verbraucht. Die Autoren wollten diese energieintensive Route umgehen. Statt von Stickstoffgas auszugehen, verwenden sie Nitrat, eine Stickstoffverbindung, die in landwirtschaftlichem Abfluss und industriellen Abwässern vorkommt, und kombinieren sie mit Kohlendioxid, dem wichtigsten Treibhausgas. Beide Substanzen werden in eine elektrochemische Zelle eingespeist – ein Gerät, in dem Strom chemische Reaktionen antreibt – so dass sie mit dem richtigen Katalysator bei Raumtemperatur und relativ niedrigen Spannungen zu Harnstoff verknüpft werden können.
Entwurf einer hilfreichen Oberfläche
Das Herzstück des Geräts ist ein fester Katalysator aus winzigen Partikeln, die Silber (Ag) mit Kadmiumoxid (CdO) kombinieren. Mikroskopie- und Röntgentechniken zeigen, dass diese Partikel intime „Heterostrukturen“ bilden, in denen metallisches Silber und CdO im Nanomaßstab in Kontakt stehen und Elektronen austauschen. Diese elektronische Wechselwirkung verändert subtil, wie jede Komponente eingehende Moleküle bindet. Unter Betriebsbedingungen wandelt sich der CdO-Anteil in Cadmiumcarbonat (CdCO₃) um, das fehlende Sauerstoffatome enthält, sogenannte Sauerstoffvakanzstellen. Diese freien Plätze wirken wie kleine Andockstellen, die Kohlendioxid einfangen und aktivieren helfen, während benachbarte Silberregionen besonders gut darin sind, stickstoffhaltige Spezies aus Nitrat zu binden.
Harnstoff effizient und selektiv herstellen
Wenn Kohlendioxid und Nitrat über diesen Ag/CdO-Katalysator in einer Laborszelle strömen, wandelt das Material sie bei ungewöhnlich niedriger „Überspannung“ um – das heißt, die zusätzlich benötigte Spannung über dem thermodynamisch idealen Wert ist gering. In einer einfachen H-förmigen Zelle erreicht die optimierte Zusammensetzung, genannt Ag₀.₀₇/CdO, eine Harnstoffselektivität von etwa 50 % bei nur −0,10 Volt gegenüber einer Standardreferenz und erzeugt nur wenig Ammoniak oder Kohlenmonoxid als Nebenprodukte. In einer weiterentwickelten Flow-Zelle, in der Gase und Flüssigkeiten kontinuierlich zugeführt werden, erzielt derselbe Katalysator eine hohe Harnstoffproduktionsrate von rund 112 Millimol pro Gramm Katalysator und Stunde bei −0,15 Volt. Durch zusätzliche Optimierung von Reaktor-Design und Betriebsbedingungen steigert das Team die Harnstoffproduktionsrate auf etwa 427 Millimol pro Gramm und Stunde bei höheren Strömen, wobei die Leistung über 1.000 Stunden Dauerbetrieb aufrechterhalten wird – ein wichtiges Zeichen für Stabilität.
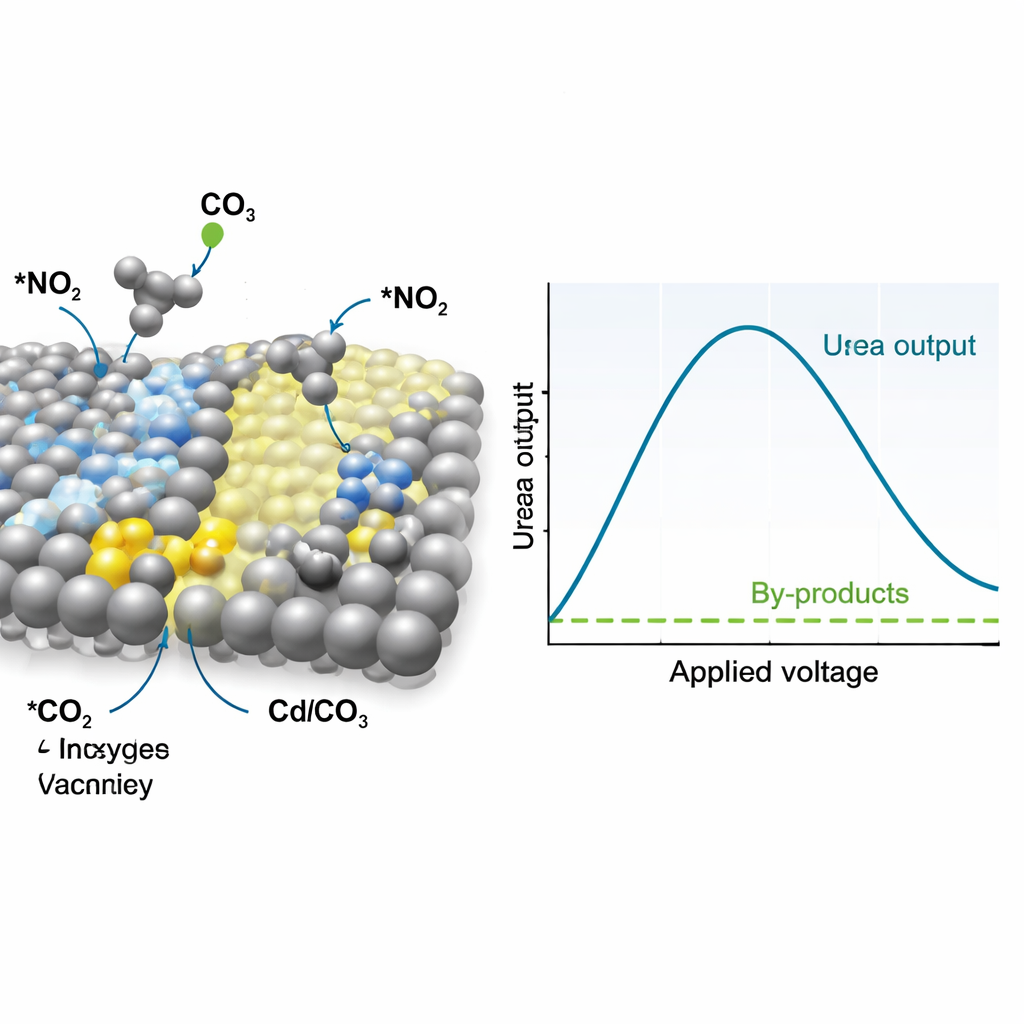
Wie der Katalysator die Reaktion lenkt
Um zu verstehen, warum dieses Material so gut funktioniert, verfolgten die Forschenden den Katalysator und Reaktionszwischenprodukte in Echtzeit mithilfe von Raman- und Infrarotspektroskopie sowie fortgeschrittenen Röntgenmethoden. Diese Messungen zeigen, dass Silberstellen bevorzugt Nitrat in ein reaktives Zwischenprodukt umwandeln, das oft als *NO₂ beschrieben wird, während das rekonstruierte CdCO₃ mit Sauerstoffvakanzstellen Kohlendioxid bindet und in *CO umwandelt, ein weiteres kurzlebiges Zwischenprodukt. Signale, die mit Kohlenstoff–Stickstoff-Bindungen assoziiert sind, treten bei den Betriebsvoltstärken auf und zeigen, dass *NO₂ und *CO früh im Prozess koppeln, um eine harnstoffähnliche Spezies zu bilden, anstatt getrennt Ammoniak oder Kohlenmonoxid zu ergeben. Computersimulationen stützen dieses Bild und legen nahe, dass die Schnittstelle zwischen Silber und vakanzreichem CdCO₃ die Energiebarriere für diesen entscheidenden C–N-Kopplungsschritt senkt und ihn gegenüber konkurrierenden Reaktionen begünstigt.
Was das für Dünger und Klima bedeuten könnte
Insgesamt zeigt die Arbeit, dass sorgfältig gestaltete Katalysatoroberflächen einfache Abfallmoleküle wie Kohlendioxid und Nitrat auf einem energieeffizienten Weg zu Harnstoff führen können, unter milden Bedingungen und mit langen Lebensdauern. Für Nicht-Fachleute ist die wichtigste Erkenntnis, dass das Team eine Art „elektronischen Filter“ gebaut hat, der es bevorzugt, Kohlenstoff und Stickstoff zu Harnstoff zu verbinden, anstatt sie als andere Produkte entweichen zu lassen. Obwohl eine reale Anwendung noch Fragen wie Materialkosten, Reaktortechnik und die sichere Beschaffung von Kadmium klären muss, bietet die Studie einen Entwurf für eine zukünftige Düngemittelproduktion, die mit erneuerbarem Strom betrieben werden kann und besser mit einem nachhaltigeren Kohlenstoff- und Stickstoffkreislauf vereinbar ist.
Zitation: Liu, S., Wang, T., Liu, J. et al. Selective electrosynthesis of urea from nitrate and carbon dioxide with low overpotential. Nat Commun 17, 1787 (2026). https://doi.org/10.1038/s41467-026-68497-y
Schlüsselwörter: Harnstoff-Elektrosynthese, Nutzung von Kohlendioxid, Nitrat-Reduktion, Design von Elektrokatalysatoren, grüner Dünger